Wissensblitze
Microbiome Center stellt regelmäßig Wissensblitze für alle angeschlossene Ärzte zur Verfügung.
Aufgrund der internationalen Leserschaft wird es in englischer Sprache erstellt.
Hier finden Sie einen Überblick über die bisher wichtigsten Wissensblitze.
#46: Die Methode des Microbiome Center: jetzt peer-reviewed und veröffentlicht
Jede Behandlerin und jeder Behandler ist bestrebt, für jeden Patienten die bestmögliche Behandlung zu finden. Dennoch kann es schwierig sein zu bestimmen, was „die beste“ Behandlung ist – insbesondere bei Patienten mit Multimorbidität, die heute die häufigste Situation darstellt (1). In vielen modernen Ansätzen der medizinischen Entscheidungsfindung spielt wissenschaftliche Evidenz eine zentrale Rolle. Es existieren verschiedene Rahmenwerke, die Behandelnde dabei unterstützen, Evidenz zu nutzen, um die am besten geeignete Behandlung auszuwählen. Zwei der bekanntesten sind Evidence-Based Medicine (EBM) und Personalized Medicine (PM).
Sowohl EBM als auch PM haben ihre eigenen Stärken, aber auch Grenzen. So verwendet die EBM randomisierte kontrollierte Studien (RCTs) als Goldstandard der Studienmethodik, da sie die beste Methode darstellen, um die meisten Quellen von Bias zu eliminieren (2). Andererseits lassen sich Ergebnisse aus RCTs nicht ohne Weiteres auf Patienten in der realen klinischen Praxis übertragen und liefern lediglich den durchschnittlichen Effekt, der den Effekt beim einzelnen Patienten nicht vorhersagt (3,4).
Diese verschiedenen Einschränkungen erschweren die Anwendung der EBM- oder PM-Methoden in der realen klinischen Praxis. Da chronische Patienten jeweils ein einzigartiges Profil haben und das Darmmikrobiom sowohl hochindividuell ist als auch an vielen chronischen Erkrankungen beteiligt ist, erkannte das Microbiome Center einen großen Bedarf an einem neuen Ansatz.
Die Methode des Microbiome Center: jetzt peer-reviewed und veröffentlicht
Im Jahr 2019 entwickelte das Microbiome Center gemeinsam mit einer Kooperation von Expertinnen und Experten aus den Bereichen Immunologie, Pharmakologie, Computational Sciences, Citizen Science sowie klinischer Praxis eine Methodik, um die Stärken von EBM und PM zu kombinieren. Seitdem haben wir diese Methode implementiert, verfeinert, verbessert und weiter ausgebaut. Als Behandler begegnen Sie ihr, wenn Sie unsere Beratungshilfe nutzen. Diese besteht nicht nur aus einer Reihe von Fragebögen und Schaltflächen; sie ist weit mehr als das: Sie ist eine konkrete Umsetzung einer umfassenden und sorgfältig entwickelten Philosophie und wissenschaftlichen Herangehensweise.
Kürzlich wurden die Philosophie und die wissenschaftliche Methode hinter unserem Ansatz peer-reviewt und in einem wissenschaftlichen Artikel veröffentlicht. Der Artikel wurde gemeinsam mit mehreren Co-Autorinnen und Co-Autoren aus verschiedenen Universitäten und Instituten verfasst und im wissenschaftlichen Journal Beneficial Microbes (5) publiziert. In dem Artikel werden die verschiedenen Stärken und Schwächen der EBM- und PM-Methoden diskutiert, und die Autoren treten einen Schritt zurück in die Wissenschaftsphilosophie, um diese beiden Paradigmen zu integrieren. Der neue Ansatz, Evidence-Based Personalized Medicine (EBPM) genannt, basiert auf dem philosophischen Weltbild des Pragmatismus.
Mit dieser Veröffentlichung ist der grundlegende Ansatz, den das Microbiome Center verwendet, nun peer-reviewt und wird als eine fundierte und innovative Methode zur Behandlung von Patienten angesehen.
Möchten Sie weitere Einblicke lesen?
Folgen Sie uns auf LinkedIn: https://www.linkedin.com/company/microbiome-center/
Oder lesen Sie frühere Insights-Flashes auf: https://microbiome-center.nl/de/wissensblitze/
Referenties:
#45: Erfolgreiche Pilotstudie mit Patienten mit Q-Fieber-Fatigue-Syndrom (QFS)
Kurz zusammengefasst
Bei Patienten mit postakuten Infektionssyndromen (PAIS), wie dem Q-Fieber-Fatigue-Syndrom (QFS), ME/CFS und Long-Covid wurde eine anhaltende Dysbiose des Darmmikrobioms festgestellt. In einem Pilotprojekt mit 85 QFS-Patienten (im Durchschnitt 16 Jahre Beschwerden) führte die personalisierte Mikrobiomtherapie zu einer Verbesserung des allgemeinen Wohlbefindens bei fast 50 % der Teilnehmer, mit einer starken Verbesserung sogar bei 1 von 7 Patienten. Wir sehen ähnliche Ergebnisse auch bei anderen PAIS-Patienten. Diese vielversprechenden Ergebnisse sind der Anlass für das Microbiome Center, PAIS in den kommenden Monaten mehr in den Fokus auf Forschung und Praxis zu legen
Das Mikrobiom bei QFS und anderen Postakute Infektionssyndrome (PAIS)
Es sind verschiedene Formen von Postakute Infektionssyndrome (PAIS) bekannt, darunter beispielsweise ME/CFS, Long Covid, Post-Treatment-Lyme-Disease-Syndrom (PTLDS), Post-Pfeiffer-Fatigue-Syndrom (Post-EBV), postinfektiöses Reizdarmsyndrom (RDS) und das Q-Fieber-Fatigue-Syndrom (QFS). Diese Formen von PAIS sind alle gekennzeichnet durch chronische Müdigkeit, Post-Exertional Malaise, neurokognitive Probleme wie Brain Fog, grippeähnliche Symptome, Gelenkschmerzen, RDS und eine Vielzahl weiterer Beschwerden (1).
Interessanterweise haben wissenschaftliche Studien bei all diesen unterschiedlichen Formen von PAIS eine Dysbiose des Darmmikrobioms festgestellt (1), und es wird spekuliert, dass die Dysbiose möglicherweise der zugrunde liegende Faktor bei allen PAIS-Formen ist. Als mögliche Mechanismen werden eine persistierende Infektion (mit dem Darm als Reservoir des Erregers), systemische und neuroinflammatorische Prozesse, Koinfektionen (d. h. ein Überwuchern von Pathogenen im Darm) sowie gestörte Mikrobiomfunktionen wie eine verminderte Butyrat- und Neurotransmitterproduktion diskutiert (1).
Q-Fieber-Fatigue-Syndrom (QFS) und personalisierte Mikrobiombehandlung
Q-Fieber wird durch eine Infektion mit dem Bakterium Coxiella burnetii verursacht (eine Zoonose). Der bislang größte registrierte Q-Fieber-Ausbruch ereignete sich in den Niederlanden in den Jahren 2007–2010, und viele Patienten entwickelten ein Q-Fieber-Fatigue-Syndrom (QFS). QFS ist eine Form von PAIS, und auch bei QFS wurde eine Darmdysbiose festgestellt. Tatsächlich wird die Theorie, dass das Darmmikrobiom der gemeinsame Faktor bei allen PAIS-Formen ist, durch eine Studie illustriert, die zeigte, dass sowohl ME/CFS als auch QFS die gleiche Art von Dysbiose aufweisen und sich in gleicher Weise von gesunden Personen unterscheiden (2).
Eine staatlich unterstützte Unterstützungsorganisation namens Q-support erkannte, dass die Prävalenz des Reizdarmsyndroms bei QFS-Patienten deutlich höher ist. In Kombination mit dem Wissen über das Mikrobiom als Faktor bei QFS war dies Anlass, gemeinsam mit dem Microbiome Center ein Pilotprojekt zu initiieren. Im Jahr 2024 wurden insgesamt 85 QFS-Patienten mit Lebensstil- und Ernährungsinterventionen in Kombination mit einer personalisierten Mikrobiombehandlung behandelt. Im Durchschnitt waren diese Patienten bereits 16 (!) Jahre erkrankt.
Das Projekt zeigte, dass viele Patienten mit der Behandlung zufrieden waren. Nach Abschluss des Pilotprojekts wurde eine Post-hoc-Analyse der medizinischen Beschwerden und der allgemeinen Wohlbefindensscores anhand der Daten von 69 Patienten durchgeführt. Diese Scores wurden alle drei Wochen auf der Plattform des Microbiome Center erfasst, was den Wert des Tools zur „Verlaufsdokumentation der Beschwerden“ zeigt. Fast 50 % der Patienten zeigten eine Verbesserung ihres allgemeinen Wohlbefindens, und jeder siebte Patient berichtete über eine deutliche Verbesserung. Einige Personen sagten buchstäblich, dass sie ihr Leben zurückerhalten hätten. Ebenso berichteten 57 % der Patienten über eine Verbesserung der Gesamtscores all ihrer Beschwerden. Wie erwartet verbesserten sich nicht alle Patienten, und einige berichteten über negative Effekte; glücklicherweise (und wie erwartet) zeigte sich jedoch, dass diese nach Absetzen der Behandlung verschwanden.
Bei einer durchschnittlichen Krankheitsdauer von 16 Jahren und Patienten, die bereits zahlreiche Behandlungen ausprobiert hatten, kann eine positive Reaktion bei nahezu der Hälfte der Patienten als großer Erfolg betrachtet werden.
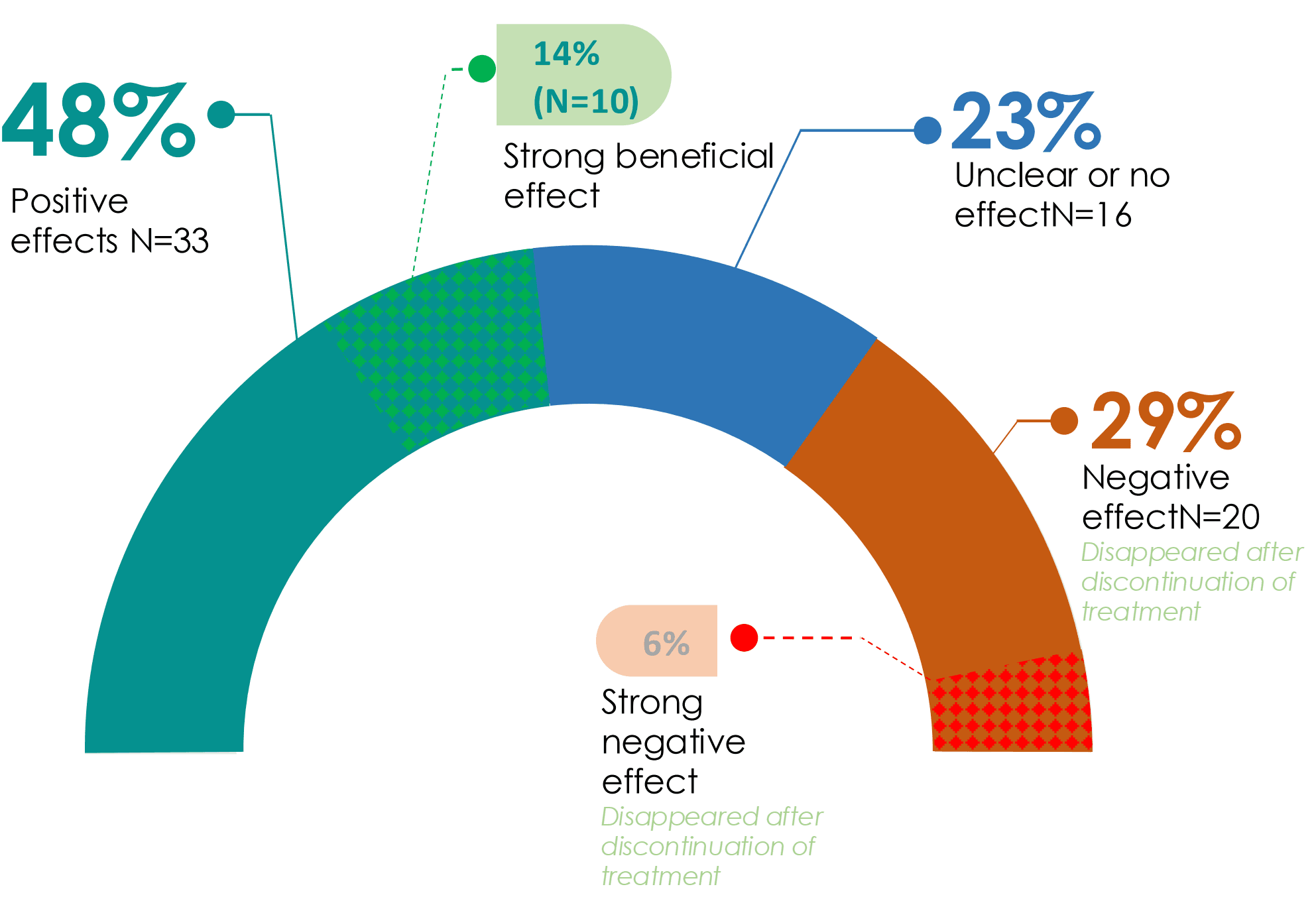
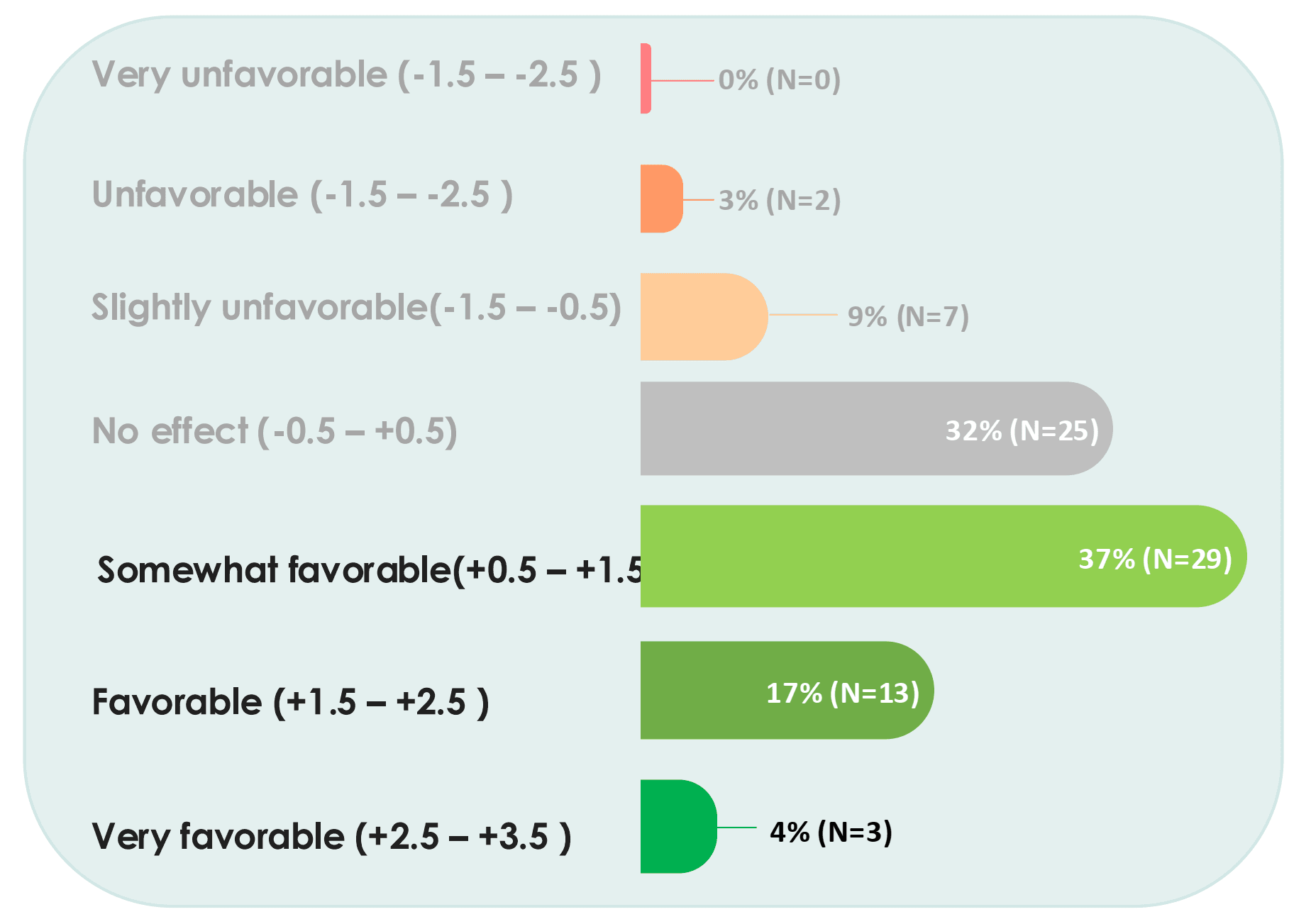
Microbiome Center macht PAIS in den kommenden Monaten zum Schwerpunktthema
Aufgrund dieser positiven Ergebnisse haben wir die anonymisierten Daten aller Patienten analysiert, die ihre Einwilligung gegeben und während ihrer Behandlung mit MyOwnBlend ihre medizinischen Beschwerden dokumentiert haben. Insgesamt gaben 82 Patienten in einem Kommentar an, an einer oder mehreren Formen von PAIS zu leiden. Die am häufigsten genannten PAIS-Formen sind ME/CFS und Long Covid. In den Daten dieser PAIS-Patienten sehen wir ähnliche Ergebnisse wie bei den QFS-Patienten, nämlich 59 %, die eine Verbesserung berichten, und jeder sechste Patient, der eine deutlich positive Veränderung seines allgemeinen Wohlbefindens angibt.
Angespornt durch diese positiven Ergebnisse hat das Microbiome Center beschlossen, PAIS in den kommenden Monaten als Schwerpunktthema zu behandeln. PAIS weist eine hohe Prävalenz auf, und es sind nur wenige Behandlungsmöglichkeiten bekannt, sodass viele Patienten auf eine Therapie warten, die ihnen helfen kann. Im Rahmen dieses Themenschwerpunkts werden wir in Forschungskooperationen eine methodisch strengere wissenschaftliche Studie initiieren, nach spezifischen Inhaltsstoffen suchen und die Daten weiter analysieren, um diese Ergebnisse noch weiter zu verbessern.
Sie können helfen!
Wenn Sie von diesen ersten Ergebnissen ebenso begeistert sind wie wir, können Sie helfen. Sie können die personalisierte Mikrobiombehandlung mit Ihren PAIS-Patienten als Option besprechen. Insbesondere wenn sie zusätzlich unter gastrointestinalen Beschwerden leiden, könnte dies eine Therapie sein, die ihnen helfen kann. Dies kann nicht nur potenziell ihnen helfen; wenn sie zudem bereit sind, den Verlauf ihrer Beschwerden auf unserer Plattform zu dokumentieren, kann dies auch anderen PAIS-Patienten zugutekommen. Denn gemeinsam können wir aus den gesammelten Erkenntnissen lernen und die Behandlung weiter optimieren. Mit einem Netzwerk von über 1000 Behandlern, die jeweils mehrere PAIS-Patienten in ihrer Praxis betreuen, können wir gemeinsam sehr schnell lernen und die Behandlung von PAIS-Patienten verbessern.
Möchten Sie weitere Einblicke lesen?
Folgen Sie uns auf LinkedIn: https://www.linkedin.com/company/microbiome-center/
Oder lesen Sie frühere Insights-Flashes auf: https://microbiome-center.nl/de/wissensblitze/
Referenzen:
#44: Zöliakie und Darmmikrobiom
Zöliakie ist nicht nur genetisch bedingt
Zöliakie wird oft als eine genetisch bedingte Krankheit angesehen. Sie ist eine chronische systemische Autoimmunerkrankung, die durch den Verlust der Toleranz gegenüber Nahrungs-Gluten gekennzeichnet ist. Obwohl sie bei genetisch veranlagten Personen auftritt, entwickelt nicht jeder mit dieser Veranlagung die Krankheit, und es gibt erhebliche Unterschiede sowohl im Erkrankungsalter als auch im Schweregrad der Symptome (1). Die einzige verfügbare Behandlung ist eine glutenfreie Ernährung (GFD), aber 30–40 % der Patienten, die eine GFD einhalten, haben weiterhin Symptome (1). Eine große Menge an Forschungsergebnissen zeigt, dass das Darmmikrobiom eine bedeutende Rolle bei der Entwicklung der Zöliakie spielt (1,2). So ist bekannt, dass eine Dysbiose des Darms dem Krankheitsbeginn vorausgeht, während genetisch veranlagte Personen ohne Dysbiose gesund bleiben (3,4). Außerdem ist bekannt, dass eine GFD einen positiven Einfluss auf die Zusammensetzung und Funktion des Mikrobioms hat, dieses jedoch nicht vollständig wiederherstellt (5). Es kann argumentiert werden, dass der positive Effekt der GFD zumindest teilweise auf ihre Wirkung auf das Darmmikrobiom zurückzuführen ist und nicht nur auf das Fehlen immunreaktiver Glutenproteine. Im Einklang damit kommen wissenschaftliche Studien zu dem Schluss, dass es sinnvoll ist, die Behandlung des Darmmikrobioms bei Patienten mit Zöliakie in Betracht zu ziehen.
Neue probiotische Stamm lindert Symptome von Zöliakie und Glutenunverträglichkeit
Leider wurden nur wenige Probiotika hinsichtlich ihrer Wirkung auf Zöliakie untersucht, mit nur wenigen Ausnahmen. Der derzeit am besten untersuchte probiotische Stamm bei Zöliakie ist Bifidobacterium longum ES1 (CETCT 7374). Etwa ein Dutzend In-vitro- und Tierstudien haben gezeigt, dass dieser Stamm Gliadin abbauen und Immunreaktionen auf Gluten modulieren kann (siehe z. B. 6–8). Darüber hinaus zeigte eine kleine randomisierte kontrollierte Studie bei Kindern mit neu diagnostizierter Zöliakie, die GFD mit GFD + B. longum ES1 verglich, dass in der Probiotika-Gruppe wichtige Verbesserungen in spezifischen Immunzellen gefunden wurden, die an den Krankheitssymptomen beteiligt sind (9). Zudem waren die proinflammatorischen Zytokine in der Gruppe, die B. longum ES1 erhielt, deutlich niedriger (9). Eine offene Studie bei Patienten mit Nicht-Zöliakie-Glutenunverträglichkeit zeigte außerdem, dass im Vergleich zu nur GFD die Gruppe mit GFD + B. longum ES1 eine stärkere Verbesserung der gastrointestinalen Symptome aufwies (10). Dieser Stamm ist nun auf der Microbiome Center-Plattform verfügbar. Obwohl er eine GFD nicht ersetzen kann, kann er Patienten mit Zöliakie oder Glutenunverträglichkeit dabei unterstützen, Symptome weiter zu lindern. Dieser interessante probiotische Stamm weist außerdem qualitativ hochwertige Evidenz für eine Wirkung bei Reizdarmsyndrom (RDS) einschließlich Durchfall und Bauchschmerzen (11,12) sowie bei verschiedenen anderen Indikationen auf. Weitere Informationen finden Sie in der detaillierten Beschreibung hinter dem i-Button auf der Microbiome Center-Plattform.
Möchten Sie weitere Einblicke lesen?
Folgen Sie uns auf LinkedIn: https://www.linkedin.com/company/microbiome-center/
Oder lesen Sie frühere Insights-Flashes auf: https://microbiome-center.nl/de/wissensblitze/
Referenzen:
- https://doi.org/10.3389/fmedt.2024.1413637
- https://doi.org/10.1007/s00430-017-0496-z
- https://doi.org/10.1073/pnas.2020322118
- https://doi.org/10.1128/spectrum.01468-24
- https://doi.org/10.3390/nu14102083
- https://doi.org/10.1021/jf201212m
- https://doi.org/10.1016/j.ijbiomac.2010.06.015
- https://doi.org/10.1189/jlb.1111581
- https://doi.org/10.1017/S0007114514000609
- https://doi.org/10.23736/S1121-421X.20.02673-2
- https://doi.org/10.1080/19490976.2024.2338322
- https://doi.org/10.3390/jcm9082353
#43: Neue einzigartige Stamm, B. adolescentis SH001, ein Kreuzernährer von Fecalibacterium prausnitzii und Laktoseverwerter
Einführung eines neuen und einzigartigen Stammes: B. adolescentis SH001
Es gibt mehrere Bifidobacterium-Arten, die als Probiotika auf dem Markt sind, zum Beispiel B. lactis, B. longum oder B. breve. Eine weniger bekannte Bakterienart der Gattung Bifidobacterium ist Bifidobacterium adolescentis. Diese Art ist jedoch eine der am häufigsten vorkommenden Bifidobacterium-Arten im Darmmikrobiom von Erwachsenen (1). Sie wird mit gesundem Altern in Verbindung gebracht und kommt in größerer Menge bei gesunden Hundertjährigen (>100 Jahre alt) vor als bei typischen älteren Menschen (1). Interessanterweise ist bekannt, dass B. adolescentis ein wichtiger Kreuzernährer für Fecalibacterium prausnitzii ist, die häufigste butyratproduzierende Art im Darmmikrobiom (2). Daher spielt sie eine wichtige Rolle bei der Fähigkeit des Darmökosystems, Butyrat zu produzieren.
Vor einigen Wochen hat das Microbiome Center den Stamm B. adolescentis SH001 verfügbar gemacht. Dieser Stamm ist genetisch identisch mit dem am besten untersuchten Stamm, iVS-1. Er wurde von einem gesunden Individuum isoliert, das eine Ernährung mit zunehmenden Mengen an Galaktooligosacchariden (GOS) erhielt (3). Interessanterweise wird GOS durch β-Galaktosidase, auch bekannt als Laktase, hydrolysiert. Durch die Isolierung dieses Stammes aus einer GOS-angereicherten Umgebung stellten die Forscher fest, dass er mehr Laktase-Gene besitzt als jeder andere getestete Probiotikastamm.
Laktase kann auch Laktose verdauen, und in-vitro-Studien zeigen tatsächlich, dass dieser Stamm ein ausgezeichneter Verwerter von Laktose ist (4). Wichtig ist, dass er dies mit der geringsten Gasproduktion im Vergleich zu Dutzenden anderer Probiotikastämme tut, und eine kleine randomisierte kontrollierte Studie (RCT) bestätigte, dass er die Symptome von Laktoseintoleranz signifikant reduziert (4). Dieselbe Studie liefert zudem Hinweise darauf, dass er Bauchschmerzen, Blähungen und Flatulenzen verringert. Darüber hinaus zeigte eine weitere RCT, dass dieser Stamm die Darmbarrierefunktion verbessert (5).
Zusammenfassend lässt sich sagen, dass dieser einzigartige neue Probiotikastamm als wichtiger Kreuzernährer für Butyratproduzenten wirken, die Verdauung von Laktose unterstützen und Symptome von Laktoseintoleranz reduzieren sowie einen „leckenden Darm“ verbessern kann. Wie immer wurde die Evidenz im Advice Aid berücksichtigt und weitere Informationen finden Sie hinter dem (i)-Symbol auf unserer Plattform.
Möchten Sie weitere Einblicke lesen?
Folgen Sie uns auf LinkedIn: https://www.linkedin.com/company/microbiome-center/
Oder lesen Sie frühere Insights-Flashes auf: https://microbiome-center.nl/de/wissensblitze/
Referenzen:
#42: Unser erster eigener Stamm, einsetzbar bei Colitis ulcerosa, Prostatitis, Divertikulitis und verschiedenen anderen Erkrankungen
Einführung des ersten eigenen Stammes des Microbiome Centers: E. coli MC231
Vor zwei Wochen haben wir mit einer kleinen feierlichen Zeremonie unseren ersten eigenen Stamm vorgestellt. Dieser Stamm, Escherichia coli MC231, wurde aus einer großen Anzahl potenzieller Stämme ausgewählt und hat eine Entwicklungszeit von anderthalb Jahren durchlaufen. Dazu gehörten die Genomsequenzierung, Charakterisierung, Entwicklung des Produktionsprozesses und Stabilitätstests.

Das Kernteam des Microbiome Centers feiert die Einführung von E. coli MC231
Der Stamm E. coli MC231 wurde aus zwei Hauptgründen ausgewählt: Erstens spielt die Bakterienart Escherichia coli eine wichtige Rolle im menschlichen Darmmikrobiom. Zweitens ist dieser spezielle Stamm genetisch nahezu identisch mit dem gut untersuchten E. coli Nissle 1917 (auch bekannt als Mutaflor©). Das bedeutet, dass die wissenschaftlichen Erkenntnisse zu E. coli Nissle 1917 auch auf E. coli MC231 anwendbar sind. Im Gegensatz zu Nissle ist unser MC231 jedoch bei Raumtemperatur stabil.
Dieser Stamm wurde unter anderem ausführlich im Zusammenhang mit Colitis ulcerosa untersucht und zeigt in Meta-Analysen randomisierter, kontrollierter Studien eine deutlich höhere Wirksamkeit als Placebo sowie eine vergleichbare Wirkung mit dem Standardmedikament 5-ASA (siehe z. B. 1). Diese Studien weisen auch auf eine deutliche entzündungshemmende Wirkung hin (1). Eine kleine Studie liefert sogar Hinweise darauf, dass dieser Stamm bei Morbus Crohn wirksam sein könnte (2) – eine Seltenheit unter Probiotika. Darüber hinaus gibt es umfassende Belege für eine positive Wirkung bei verschiedenen Darmproblemen, darunter beispielsweise Divertikulitis (3).
Interessanterweise zeigt dieser Stamm auch eine Wirksamkeit bei bestimmten Erkrankungen außerhalb des Darms. Ein Beispiel ist eine deutliche Reduktion der Rückfallrate bei chronischer bakterieller Prostatitis (4). Ein weiteres Beispiel sind Erkenntnisse aus einer randomisierten, kontrollierten Studie mit Teilnehmern, die an Akne, Rosazea oder seborrhoischem Ekzem litten und sich im Vergleich zur Placebo-Gruppe signifikant verbesserten (5).
Der E. coli MC231 ist verfügbar und selbstverständlich in der Beratungshilfe aufgenommen. Weitere Informationen zur wissenschaftlichen Evidenz finden Sie über das „i“-Symbol hinter dem Stamm.
Möchten Sie weitere Einblicke lesen?
Folgen Sie uns auf LinkedIn: https://www.linkedin.com/company/microbiome-center/
Oder lesen Sie frühere Insights-Flashes auf: https://microbiome-center.nl/de/wissensblitze/
Referenzen:
- https://doi.org/10.15403/jgld.2014.1121.244.ecn
- https://doi.org/10.1097/00004836-199712000-00021
- https://doi.org/10.1097/01.meg.0000049998.68425.e2
- https://doi.org/10.1007/s00345-021-03773-8
- https://doi.org/10.3748/wjg.v22.i23.5415
#41: Neuer Stamm: Lacticaseibacillus paracasei Lpc-37
Forschung zu Lacticaseibacillus paracasei Lpc-37 und seine klinischen Anwendungen
Lacticaseibacillus paracasei Lpc-37 wurde vor mehreren Jahrzehnten aus einem Milchprodukt isoliert und seither in zahlreichen präklinischen und klinischen Studien untersucht. Diese Studien haben den Stamm entweder isoliert oder in Kombination mit anderen probiotischen Stämmen erforscht.
Ein gesundheitlicher Aspekt, der in der wissenschaftlichen Forschung bisher relativ wenig Beachtung gefunden hat und bei dem dieser Stamm untersucht wurde, ist die Schlafqualität. Zwei randomisierte, Placebo-kontrollierte Studien (RCTs), in denen Lpc-37 als Monostamm getestet wurde, zeigten einen positiven Effekt auf die Schlafqualität (1,2). Diese Studien wurden bei Studierenden in der Prüfungsphase sowie bei gesunden Erwachsenen durchgeführt. In beiden Gruppen wurde im Vergleich zur Placebogruppe eine Reduktion von Schlafstörungen beobachtet. Darüber hinaus wurde in denselben Studien auch der Einfluss auf Stress untersucht, wobei die erste Studie (1) keine signifikanten Unterschiede feststellte, während die zweite Studie (2) einen positiven Effekt berichtete.
Eine weitere bemerkenswerte Indikation, die untersucht wurde, ist Autismus. Hier wurde Lpc-37 als Bestandteil einer Formulierung mit mehreren probiotischen Stämmen und einem Präbiotikum verabreicht (3). Obwohl diese Pilotstudie einige Einschränkungen aufweist (darunter eine geringe Teilnehmerzahl und eine relativ hohe Abbruchquote), sind die Ergebnisse relevant. Es wurde eine Verbesserung auf einer Skala zur Quantifizierung der Schwere von Autismus-Spektrum-Störungen (ASS) festgestellt. Dies ist besonders bemerkenswert, da nur wenige Interventionen diesen Effekt zeigen. Die Studie unterstützt das Konzept, dass mikrobiomorientierte Interventionen eine Rolle bei Autismus spielen können, was mit aktuellen Forschungen zur Rolle des Darmmikrobioms bei Autismus übereinstimmt – darunter eine multikohortale Studie, die in Scientific Reports veröffentlicht wurde (4). Um diese Erkenntnisse weiter zu beleuchten, veranstalten wir ein Webinar zu diesem Thema, in dem wir auch Fallbeispiele aus der Praxis besprechen. Dieses Themen-Webinar zu Autismus findet am 17. März (Englisch) und 1. April (Deutsch) von 19:30 bis 21:00 Uhr statt.
Darüber hinaus zeigt eine groß angelegte RCT mit Lpc-37 als Monostamm einen positiven Effekt auf die Prävention von Durchfall und Fieber (5) sowie auf verschiedene andere Indikationen wie antibiotikaassoziierten Durchfall, kognitive Funktionen und Pathogene. Weitere Informationen zu diesem Stamm und den wissenschaftlichen Erkenntnissen finden Sie in der ergänzenden Dokumentation über das i-Symbol neben dieser Zutat.
Möchten Sie weitere Einblicke lesen?
Folgen Sie uns auf LinkedIn: https://www.linkedin.com/company/microbiome-center/
Oder lesen Sie frühere Insights-Flashes auf: https://microbiome-center.nl/de/wissensblitze/
Referenzen:
- https://doi.org/10.1016/j.bbih.2023.100673
- https://doi.org/10.1016/j.ynstr.2020.100277
- https://doi.org/10.1016/j.phrs.2020.104784
- https://doi.org/10.1038/s41598-023-50601-7
- https://doi.org/10.9734/EJNFS/2014/8280
#40: Die ökologische Realität des Mikrobioms und phasenweise Behandlung
In einer Ökologie geschieht alles gleichzeitig
Es gibt verschiedene Beispiele für Behandlungsprotokolle, die einen phasenweisen oder schrittweisen Ansatz verwenden. Ein Beispiel dafür ist der sogenannte „5R“-Ansatz, bei dem die Behandlung der Darmgesundheit in fünf Phasen erfolgt: „remove“ (entfernen), „replace“ (ersetzen), „reinoculate“ (wiederansiedeln), „repair“ (reparieren) und „rebalance“ (ins Gleichgewicht bringen) (1). Der erste Schritt (entfernen) umfasst das Entfernen von Pathogenen, während Probiotika erst im dritten Schritt (wiederansiedeln) eingesetzt werden.
Häufig wird die Frage gestellt, ob Pathogenen nicht zuerst entfernt werden müssen, bevor mit personalisierten Probiotika begonnen wird. Die Antwort ist einfach: nein. Das Darmmikrobiom ist eine Ökologie, und in einer Ökologie geschieht alles gleichzeitig. Wenn Pathogenen entfernt werden, werden auch andere Mikroben beeinflusst. Selbst wenn antimikrobielle Behandlungen nur unerwünschte Mikrobenarten abtöten würden (was nicht der Fall ist, auch nicht bei Phytotherapeutika), hinterlässt ihre Entfernung eine offene Nische, die von anderen Arten besetzt wird. Dies geschieht sehr schnell, da sich Bakterien innerhalb von Minuten bis Stunden replizieren (2).
Werfen wir einen genaueren Blick auf die Tatsache, dass viele Protokolle ein oder zwei Monate mit dem Wiederansiedeln warten, obwohl bekannt ist, dass sich Bakterien innerhalb von Minuten bis Stunden replizieren. Wir können ein bekanntes Beispiel aus der Ökologie als Metapher verwenden: einen Wald. Ein oder zwei Monate zwischen dem Entfernen und dem Wiederansiedeln bei Behandlungen des Darmmikrobioms zu warten, ist vergleichbar mit dem Abbrennen eines Waldes, um unerwünschte Bäume zu entfernen, und dann Jahrzehnte zu warten, um neue Bäume zu pflanzen. Die offenen Nischen werden lange vor dem Wiederansiedeln von neuen Arten besetzt.
Zurück zu den personalisierten Probiotika. Neben der Tatsache, dass es keinen Sinn ergibt, ein oder zwei Monate zwischen dem Entfernen und dem Wiederansiedeln zu warten, wenn es sich um eine Ökologie handelt, in der sich die Arten innerhalb von Minuten bis Stunden replizieren, ist es auch nicht logisch, wenn man die Wirkungen von Probiotika betrachtet. Die meisten probiotischen Stämme, die im Microbiome Center erhältlich sind, haben nämlich nicht nur eine Wirkung. Oft können die Stämme sowohl Pathogenen hemmen als auch die gewünschten Mikrobiom-Funktionen verbessern, wie z. B. die Buttersäureproduktion, sowie spezifische klinische Ergebnisse fördern. Es handelt sich also nicht um ein „Entweder-oder“.
Viele Protokolle, die einen phasenweisen oder schrittweisen Ansatz verwenden, wurden von Nahrungsergänzungsmittelherstellern entwickelt. Obwohl dies ihnen helfen kann, Produkte für jede Phase zu verkaufen, unterstützt die biologische Realität dieses Vorgehen nicht. Ein realistischeres Konzept ist es, das Mikrobiom als eine Ökologie zu betrachten und zu erkennen, dass in einer Ökologie alles gleichzeitig geschieht. Es ist also sinnvoll, auch alles gleichzeitig und personalisiert zu behandeln.
Möchten Sie weitere Einblicke lesen?
Folgen Sie uns auf LinkedIn: https://www.linkedin.com/company/microbiome-center/
Oder lesen Sie frühere Insights-Flashes auf: https://microbiome-center.nl/en/medici/kennisflits/
Referenzen:
#39: Den blühenden Markt für personalisierte Beratung im Griff
Die vielen Fallstricke personalisierter Beratung
Im Zeitalter der KI entstehen mehrere Unternehmen, die personalisierte Ernährungsberatung und/oder Nahrungsergänzungsmittel-Empfehlungen auf der Basis von Stuhlanalyseergebnissen und manchmal auch auf Basis eines Fragebogens anbieten. Obwohl wir von dem Konzept der Personalisierung begeistert sind, scheint es leider so, dass die meisten dieser Unternehmen in einige wichtige Fallstricke geraten.
Die Steuerung anhand relativer Häufigkeit funktioniert nicht
Erstens verwenden Unternehmen häufig einfach die relative Häufigkeit von Bakterienarten oder -gattungen und vergleichen diese mit der relativen Häufigkeit, die in gesunden Kohorten beobachtet wird, um eine Steuerung der relativen Häufigkeit zu erreichen. Dies ignoriert jedoch die Tatsache, dass es bisher niemandem gelungen ist, gesunde Grenzen für die relative Häufigkeit einzelner Arten zu definieren, da verschiedene Mikrobiom-Zusammensetzungen gesund sein können (1). Stattdessen verhält sich das Darmmikrobiom wie eine Ökologie, in der die Zusammensetzung von den Umständen abhängt, wie der genetischen Veranlagung des Wirts, dem Lebensstil, der Ernährung usw. (2). Daher ist es besser, funktionelle Aspekte des Mikrobioms zu betrachten (z. B. die Gesamtproduktion von Butyrat, die Hemmung von Krankheitserregern oder die Funktion der Darmbarriere). Im Gegensatz zur bloßen Verwendung der relativen Häufigkeit bieten diese funktionellen Aspekte tatsächlich Behandlungsziele, weshalb dies die Methode ist, die das Microbiome Center und Biovis verwenden.
Die meisten Ernährungsempfehlungen basieren auf falschen Annahmen und schwachen Evidenz
Zweitens ist die Beweiskraft hinter vielen Arten von Ernährungsratschlägen äußerst schwach. Vieles basiert auf Beobachtungsstudien, die anfällig für zahlreiche Verzerrungen und Störfaktoren sind. Auch hier spielt die oft eher reduktionistische Herangehensweise eine Rolle. In Beobachtungsstudien wird beispielsweise typischerweise angenommen, dass es möglich ist, eine einzelne Ernährungs-komponente isoliert zu untersuchen, was jedoch die stark interaktive Natur von Diäten ignoriert. Darüber hinaus wird dabei auch ignoriert, dass bekannt ist, dass beispielsweise eine Person einen Spitzenblutzuckeranstieg auf ein Keks zeigt und nicht auf eine Banane, während eine zweite Person das Gegenteil erlebt (3). Mit anderen Worten, es ist unmöglich zu schließen, dass zum Beispiel eine Banane ungesund ist, weil sie einen Blutzuckerspitzenwert verursacht, da jede Person unterschiedlich reagiert. Daher ist jeder Ernährungsrat, der vereinfacht einen bestimmten Nahrungsbestandteil mit bestimmten Effekten verknüpft, nicht im Einklang mit der Realität unserer Physiologie. Daher argumentieren wir, dass ein besserer Ansatz darin besteht, zunächst anzuerkennen, dass bei den extrem komplexen und personenspezifischen Reaktionen auf Diäten das einzige verallgemeinerbare Wissen über Diäten Logik ist: Essen Sie Lebensmittel, die nahe an dem liegen, worauf sich unsere Physiologie entwickelt hat. Das bedeutet echte Lebensmittel, die minimal verarbeitet sind, einschließlich Gemüse, Fisch, Obst, Fleisch, Nüssen, Samen, Wasser, Kräutern usw. Zweitens ist es für jeden nützlich zu lernen, seine persönliche Reaktion auf verschiedene Lebensmittel und Ernährungsmuster zu erkennen – persönlicher geht es nicht!
Vermeiden Sie Nahrungsergänzungsmittel-Empfehlungen, die auf Annahmen basieren, nur auf Artniveau gemacht werden oder keine Referenzen haben
Drittens werben viele dieser Unternehmen oft damit, personalisierte Vorschläge für probiotische Nahrungsergänzungsmittel anzubieten. Leider basieren diese Vorschläge in vielen Fällen nicht auf direkten klinischen Evidenz für die Produkte, sondern auf verschiedenen Annahmen über die Stimulation von Taxa, die in der Stuhlanalyse niedrig sind. Hier gilt die erste Fallgrube: Gesundheit kann nicht einfach mit relativer Häufigkeit verknüpft werden. Darüber hinaus basieren die Vorschläge für Probiotika auf den Bakterienarten in diesen Produkten, was ignoriert, dass die Effekte stamm-spezifisch sind (verschiedene Stämme derselben Bakterienart können unterschiedliche Effekte haben). Ein Produkt basierend auf der Art vorzuschlagen, ist wie ein Tiergeschäft, das vorschlägt, „einen Hund“ zu kaufen, ohne die Unterschiede zwischen beispielsweise einem Bulldog und einem Labrador zu berücksichtigen (beide dieselbe Art). Darüber hinaus ist diese Denkweise ziemlich reduktionistisch, und das funktioniert in einer komplexen Ökologie wie dem Darmmikrobiom nicht. Deshalb ist es besser, Probiotika auf der Grundlage direkter klinischer Evidenz mit dem genauen Stamm auszuwählen. Dies umgeht Annahmen über Mechanismen und konzentriert sich direkt auf klinische Ergebnisse. Schließlich offenbaren viele Anbieter nicht, auf welchen Evidenz ihre Empfehlungen basieren, was es schwierig macht zu beurteilen, ob die Ratschläge realistisch sind.
Fazit: Verwenden Sie evidenzbasierte personalisierte Beratung
Wir glauben, dass jede personalisierte Mikrobiom-Behandlungsberatung auf (1) direktem mechanistischem und klinischem Evidenz, (2) Studien mit genau dem gleichen Stamm, (3) Dosierungen wie in den Studien verwendet, und (4) vollständiger Transparenz über die zugrundeliegenden Evidenz basieren muss.
Möchten Sie weitere Einblicke lesen?
Folgen Sie uns auf LinkedIn: https://www.linkedin.com/company/microbiome-center/
Oder lesen Sie frühere Insights-Flashes auf: https://microbiome-center.nl/en/medici/kennisflits/
Referenzen:
#38 Neue glutathionproduzierende Bakterienstamm, neue Indikationen
Limosilactobacillus fermentum ME-3
Kürzlich wurde ein neuer probiotischer Stamm, Limosilactobacillus fermentum ME-3, in die Liste der verfügbaren Bausteine aufgenommen. Dieser probiotische Stamm wurde aus dem Stuhl eines gesunden Kindes isoliert und gehört zu den seltenen Laktobazillen, die über ein vollständiges Glutathionsystem verfügen, mit dem sie dieses leistungsstarke Antioxidans produzieren können (1,2). Interessanterweise zeigen in-vitro-, präklinische und klinische Studien, dass dieser Stamm in verschiedenen Darreichungsformen (wie Nahrungsergänzungsmittel, Kefir, fermentierte Ziegenmilch und Käse) tatsächlich oxidativen Stress auf systemischer Ebene reduziert (2-5). Zudem gibt es Hinweise darauf, dass er zur Verringerung der Insulinresistenz beitragen kann (6-8). Darüber hinaus wurde nachgewiesen, dass L. fermentum ME-3 verschiedene Pathogene hemmt, darunter Helicobacter pylori (9-10).
Dieser Stamm ist nun als Baustein mit einer typischen Tagesdosis von 2×10¹⁰ KBE/Tag (bei 3 g/Tag) verfügbar. Für weitere Informationen und alle Studien können Sie den i-Button auf unserer Online-Plattform konsultieren.
Oxidativer Stress und H. pylori-Infektion
Aufgrund der einzigartigen Fähigkeit von L. fermentum ME-3, oxidativen Stress zu reduzieren und H. pylori zu hemmen, wurden zwei neue Fragen in Schritt zwei der Advice Aid (Medizinischer Hintergrund) hinzugefügt. Vermuten Sie, dass Ihr Kunde unter oxidativem Stress leidet? Oder gibt es Hinweise darauf aus der Biovis-Mitochondrien-Diagnostik? Dann können Sie dies nun in der Advice Aid angeben, wodurch der neue L. fermentum ME-3-Baustein empfohlen werden könnte. Gibt es Hinweise auf eine H. pylori-Infektion? Auch dies kann nun in der Advice Aid berücksichtigt werden.
Möchten Sie weitere Einblicke lesen?
Folgen Sie uns auf LinkedIn: https://www.linkedin.com/company/microbiome-center/
Oder lesen Sie frühere Insights-Flashes auf: https://microbiome-center.nl/de/wissensblitze/
References
https://doi.org/10.1080/08910600902815561
https://doi.org/10.1134/S0003683810050030
https://doi.org/10.1186/1475-2891-4-22
https://doi.org/10.1515/biol-2015-0021
https://doi.org/10.2478/s11536-008-0022-1
https://doi.org/10.1186/s12937-016-0213-6
https://doi.org/10.31038/EDMJ.2019324
https://doi.org/10.1002/mnfr.201901018
https://doi.org/10.1111/j.1365-2672.2006.02857.x
https://doi.org/10.1080/08910600802408178
#37: L. crispatus in vaginalen Präparaten
Letzten Monat brachte das US-amerikanische Unternehmen Seed Health ein vaginales Probiotikum auf den Markt, das mehrere Stämme von Lactobacillus crispatus enthält (1). Ihr neues vaginales Produkt, VS-01™ (99 $ für 8 Tabletten), wurde auf vielen Social-Media-Kanälen vorgestellt (2). Auch andere vaginale Produkte auf Basis von L. crispatus befinden sich in der Entwicklung. So arbeiten die Unternehmen MGH und Biose Industrie an einem Produkt (LBP), das mehrere L. crispatus-Stämme enthält (3).
Diese Beispiele zeigen deutlich, dass die Behandlung von vaginalen Gesundheitsproblemen mit L. crispatus-Präparaten als vielversprechender Ansatz angesehen wird. Unternehmen investieren erhebliche Ressourcen in die Entwicklung vaginaler Lösungen. Dies steht im Einklang mit wissenschaftlichen Erkenntnissen, die belegen, dass L. crispatus eine Schlüsselrolle für die vaginale Gesundheit spielt (4).
Mit diesen Entwicklungen verfolgen die genannten Produkte (die in Europa nicht verfügbar sind) ein Konzept, das das Microbiome Center bereits vor zwei Jahren umgesetzt hat. Als Vorreiter in der Wissenschaft entwickelte das Microbiome Center zusammen mit einem niederländischen Apotheker im Jahr 2022 vaginale Zäpfchen, die zwei verschiedene L. crispatus-Stämme enthalten. Diese Zäpfchen sind als magistrale Rezeptur erhältlich (30 Zäpfchen für 88 €). Sie können diese direkt verschreiben (d.h. ohne die Advice Aid zu nutzen), indem Sie in Ihrem Konto auf die Schaltfläche „Rezepte“ auf der Startseite klicken und dann im Bestellformular „Magistrales Produkt“ auswählen.
Möchten Sie weitere Einblicke lesen?
Folgen Sie uns auf LinkedIn: https://www.linkedin.com/company/microbiome-center/
Oder lesen Sie frühere Insights-Flashes auf: https://microbiome-center.nl/de/wissensblitze/
References
- https://seed.com/vaginal-synbiotic
- https://www.instagram.com/thealist.us/reel/C7PJXuGpstc/
- https://www.microbiometimes.com/the-clinical-journey-of-a-novel-lbp-for-bacterial-vaginosis-developed-by-mgh-biose-industrie/
- https://doi.org/10.3389/fcimb.2021.631972
- https://www.youtube.com/watch?v=FHGtPdBsLv4
36: Added acacia fiber and option to limit prebiotics
Acacia Senegal fiber
On popular request, we have added acacia fibers as new ingredient. This fiber is often used as part of microbiome treatments, typically because it is considered to stimulate butyrate-producing bacteria. Acacia fiber (also known as gum Arabic) is sold as food supplement in typical daily doses of 5-10g/d and, for practical purposes, the nominal daily dose in the MyOwnBlend is set to 5g/d as well. Interestingly, however, most scientific studies have used daily doses of 25g/d or higher. This means that for the typically used daily dose, the strength of evidence for most indications is relatively low.
That said, some of the indications for which scientific studies suggest that acacia fiber can be effective are constipation (e.g. 1,2) and bloating (3). One study shows a trend towards a benefit for IBS, although it did not reach statistical significance (1). Moreover, several studies have shown an effect of acacia fiber for metabolic dysfunction (i.e. insulin resistance) (e.g. 4,5), and there is some evidence for ulcerative colitis (5) and periodontitis (6). In addition, there is some clinical evidence that high-dose acacia fibers can increase butyrate production (7). You can find more indications and information about this new ingredient behind the i-button on our platform.
Limit prebiotics in Advice Aid
Some patients may respond quite strongly to prebiotics. When this is expected, the amounts can be lowered and alternatives can be added manually when making the prescription. Doctors have requested us to include this in the Advice Aid too. We have now implemented this for all non-probiotics, including prebiotics such as PHGG or 2’fucosyllactose, as well as other non-probiotic ingredients such as glutamine.
In step 2 of the Advice Aid (medical background), you can find the new question “Limit non-probiotics”. if you score 1, 2, or 3, the maximum daily dose of non-probiotics in the proposed MyOwnBlend is limited to 5g/d, 3g/d, or 1g/d respectively. If you select the maximum score of 4, non-probiotics will be excluded completely and the proposed MyOwnBlend will contain only probiotic ingredients.
References
1. https://doi.org/10.1007/s00394-024-03398-8
2. https://pesquisa.bvsalud.org/portal/resource/pt/emr-140096
3. https://doi.org/10.3390/nu13010194
4. https://doi.org/10.4236/fns.2022.134031
5. https://doi.org/10.31989/ffhd.v7i3.325
6. https://doi.org/10.1016/j.sdentj.2017.10.006
7. https://doi.org/10.1038/sj.ki.5000028
35: Harnwegsinfektionen
Probiotika bei Harnwegsinfektionen
Lange Zeit wurde angenommen, dass die Harnwege steril sind. Doch Forschungen des letzten Jahrzehnts haben gezeigt, dass es ein Mikrobiom der Harnwege gibt – das sogenannte Urobiom (1). Harnwegsinfektionen (HWI) gehören zu den häufigsten Infektionen, insbesondere bei Frauen. Tatsächlich haben in den USA eine von drei Frauen unter 24 Jahren bereits Antibiotika gegen HWI verschrieben bekommen (1). Die Rückfallrate ist hoch – bis zu 30 % innerhalb von sechs Monaten. Der hohe Einsatz von Antibiotika führt zur Entwicklung von Antibiotikaresistenzen und kann die Zusammensetzung sowohl des Darm- als auch des Urobioms verändern, was das Risiko für wiederkehrende Infektionen und andere Erkrankungen erhöht (1,2).
Besonders Frauen leiden häufig unter HWI, wobei sowohl die Darm-Blasen- als auch die Vaginal-Blasen-Achse eine Rolle spielen. Denn sowohl das Darm- als auch das Vaginalmikrobiom können eine Quelle für Krankheitserreger sein, die HWI verursachen (2). Die Gesundheit dieser beiden Mikrobiome ist entscheidend, um das Überwachsen opportunistischer Pathogene, die HWI auslösen können, zu verhindern. Klinische Studien zeigen, dass bestimmte orale und vaginale Probiotika das Risiko für HWI senken können (2).
Während die Behandlung des Darmmikrobioms zunehmend bekannter wird und Stuhlanalysen helfen können, potenzielle Krankheitserreger für personalisierte Mikrobiomtherapien zu identifizieren, ist das Vaginalmikrobiom weniger gut erforscht. Im Gegensatz zum Darmmikrobiom ist ein gesundes Vaginalmikrobiom durch eine sehr geringe Diversität gekennzeichnet. Eine hohe Diversität hingegen wird mit Dysbiose und einem Überwachsen von Krankheitserregern in Verbindung gebracht (3). Ein Vaginalmikrobiom, das von Laktobazillen (insbesondere Lactobacillus crispatus) dominiert wird, gilt als gesund und kann das Wachstum von HWI-Erregern wie E. coli hemmen (4). Eine randomisierte kontrollierte Studie (RCT) mit einem vaginal verabreichten Probiotikum, das eine L. crispatus-Stamm enthielt, zeigte ein verringertes Risiko für wiederkehrende HWI – insbesondere dann, wenn der probiotische Stamm das Vaginalmikrobiom erfolgreich besiedelte (5).
Aus diesem Grund enthalten die magistral hergestellten vaginalen Zäpfchen, die vom Microbiome Center in Zusammenarbeit mit unserem Apotheker entwickelt wurden, zwei verschiedene L. crispatus-Stämme. Je nach Vorliegen einer Dysbiose im Darm oder in der Vagina können Patienten mit HWI entweder mit einer personalisierten Darmmikrobiomtherapie und/oder mit vaginalen Zäpfchen behandelt werden. Die personalisierte Darmmikrobiomtherapie kann über Advice Aid auf unserer Plattform verordnet werden, während die vaginalen Zäpfchen direkt über die Schaltfläche „Neu“ verschrieben werden können, indem die Kategorie „Magistrales Produkt“ oben ausgewählt wird.
Möchten Sie weitere Einblicke lesen?
Folgen Sie uns auf LinkedIn: https://www.linkedin.com/company/microbiome-center/
Oder lesen Sie frühere Insights-Flashes auf: https://microbiome-center.nl/de/wissensblitze/
References:
https://doi.org/10.1016/j.micres.2022.127010
https://doi.org/10.3390/diagnostics11010007
https://doi.org/10.1097/LGT.0000000000000643
https://doi.org/10.1128/microbiolspec.UTI-0025-2016
https://doi.org/10.1093/cid/cir183
34: Sporenbildende Bakterien
Sporenbildende Bakterien als Probiotika
In letzter Zeit haben mehrere Unternehmen, die probiotische Produkte vermarkten, sporenbildende probiotische Bakterien in den Fokus gerückt. Doch was sind Sporenbildner und welche Vorteile bieten sie?
Die meisten Probiotika auf dem Markt bestehen aus Lactobacilli und/oder Bifidobacteria, darunter bekannte Stämme wie Lactobacillus rhamnosus GG und Bifidobacterium animalis subsp. lactis BB-12. Probiotische Stämme werden typischerweise aufgrund ihrer Überlebensfähigkeit im Magen-Darm-Trakt (GI) und ihrer Haltbarkeit ausgewählt, da dies die größten Herausforderungen für die Bakterien sind.
Im Gegensatz zu Lactobacilli und Bifidobacteria können einige Bakterienarten sogenannte Endosporen bilden. Dabei handelt es sich um metabolisch inaktive Zellen mit einer extrem widerstandsfähigen Außenhülle, die extremen Bedingungen standhalten und sogar Millionen von Jahren überleben können (1). Dies verdeutlicht direkt einen der größten Vorteile sporenbildender Bakterien: Sie haben eine exzellente Haltbarkeit, sind hitzebeständig (manche sporenbildenden Probiotika werden sogar in Tee oder Gebäck verwendet) und überleben besonders gut im Magen-Darm-Trakt. Die Endosporen werden im Darm reaktiviert und können dort ihre positiven Effekte entfalten. Darüber hinaus gehören diese Sporenbildner zu anderen Bakteriengattungen als herkömmliche Probiotika und weisen spezifische Eigenschaften auf.
Die bekanntesten und am besten untersuchten sporenbildenden Bakterienarten sind Bacillus subtilis, B. coagulans und B. clausii (1). Die Sammlung des Microbiome Centers enthält gut untersuchte Stämme dieser Spezies, darunter B. subtilis R-179, B. coagulans Unique IS-2 und B. clausii UBBC-07. Diese Stämme wurden unter anderem auf ihre Wirksamkeit bei Colitis ulcerosa und SIBO (2,3), Verstopfung und Reizdarmsyndrom (IBS) (4,5) sowie Durchfall und Atemwegsinfektionen (6,7) untersucht.
Weniger bekannte sporenbildende probiotische Bakterien sind B. mesentericus und Clostridium butyricum, die beide Teil des Butyrate Generator-Bausteins sind. C. butyricum kann Butyrat (Buttersäure) produzieren, und dieser Wirkmechanismus verleiht diesem Baustein eine starke entzündungshemmende Wirkung, was ihn besonders wirksam bei Colitis ulcerosa macht (8). Darüber hinaus wird vermutet, dass dieser Mechanismus auch der Grund dafür ist, dass unsere eigenen Datenanalysen konsequent gezeigt haben, dass dieser Baustein bei Allergien effektiv ist. Allergien stehen im Zusammenhang mit dysregulierten Immunreaktionen, und Butyrat kann diese modulieren.
Fazit
Es gibt verschiedene sporenbildende probiotische Spezies. Die am besten untersuchten Stämme der bekannten Bacillus-Arten sowie einige weniger verbreitete Stämme sind als Bausteine auf der Microbiome Center-Plattform verfügbar.
Möchten Sie weitere Einblicke lesen?
Folgen Sie uns auf LinkedIn: https://www.linkedin.com/company/microbiome-center/
Oder lesen Sie frühere Insights-Flashes auf: https://microbiome-center.nl/de/wissensblitze/
References:
https://doi.org/10.3390/ijms23063405
https://doi.org/10.12998/wjcc.v6.i15.961
https://doi.org/10.1155/2020/4181748
https://doi.org/10.1007/s12602-019-09542-9
https://doi.org/10.3920/BM2017.0129
https://doi.org/10.3920/BM2012.0034
https://doi.org/10.2147/tcrm.2007.3.1.13
https://doi.org/10.3748/wjg.v21.i19.5985
33: Neue Zutat, neue Fragen
Bifidobacterium lactis HN019
Kürzlich wurde ein neuer Baustein zur Liste der Optionen hinzugefügt, die für personalisierte Mikrobiom-Behandlungen verwendet werden können. Dieser Baustein enthält Bifidobacterium lactis HN019, einen umfassend untersuchten probiotischen Stamm, der ursprünglich aus Joghurt isoliert wurde. Mehrere hochwertige RCTs haben gezeigt, dass dieser Stamm gegen Parodontitis wirksam ist (1-3).
Darüber hinaus hat eine Meta-Analyse klinischer Studien ergeben, dass HN019 auch die zelluläre Immunität bei älteren Menschen stärkt (4). Dies umfasst die phagozytische Kapazität polymorphkerniger Zellen (die Eindringlinge durch Phagozytose zerstören) und die tumorzerstörende Aktivität natürlicher Killerzellen (die Tumorzellen eliminieren). Zudem haben groß angelegte klinische Studien gezeigt, dass HN019 Atemwegsinfektionen und Eisenmangel bei Kindern vorbeugen kann (5-7).
Dieser Stamm wurde auch auf weitere Effekte untersucht, darunter Verstopfung, Blähungen und entzündungshemmende Wirkungen. Alle Informationen über die wissenschaftlichen Erkenntnisse zu diesem Stamm findest du auf unserer Webplattform, indem du auf den i-Button hinter diesem Baustein klickst.
Aktualisierte Advice Aid-Fragen
Mit der Einführung des B. lactis HN019-Bausteins wurden neue Indikationen in die Liste der medizinischen Hintergründe aufgenommen. Dazu gehören Parodontitis, zelluläre Immunität und Eisenmangel.
Zusätzlich wurde die Frage zu Blähungen/Völlegefühl in der Beschwerdeliste in zwei separate Fragen aufgeteilt. Obwohl diese Beschwerden miteinander verbunden sind, sind sie nicht identisch, und die wissenschaftlichen Erkenntnisse zu verschiedenen Bausteinen rechtfertigen diese Trennung. So zeigt das vorhandene Evidenzmaterial für B. lactis HN019, dass dieser Stamm eine Wirkung auf Blähungen hat, jedoch nicht auf Völlegefühl.
Durch die kontinuierliche Bewertung wissenschaftlicher Daten und die Optimierung der Advice Aid-Fragen stellt das Microbiome Center sicher, dass ein fortlaufender Verbesserungsprozess stattfindet. So kannst du deinen Patienten die bestmögliche Behandlung bieten.
References:
https://doi.org/10.1111/jcpe.12995
https://doi.org/10.1371/journal.pone.0238425
https://doi.org/10.1007/s00784-022-04744-y
https://doi.org/10.3390/nu9030191
https://doi.org/10.1371/journal.pone.0012164
https://doi.org/10.3920/BM2022.0041
https://doi.org/10.1097/MPG.0b013e3181d98e45
32: Migräne
Die Rolle des Darmmikrobioms bei Migräne
Viele Gesundheitsprobleme werden mit dem Darmmikrobiom in Verbindung gebracht, selbst wenn sich diese Probleme an anderen Stellen im Körper manifestieren und keine direkte Verbindung zum Darm vermutet wird. Migräne ist ein gutes Beispiel dafür. Die Tatsache, dass das Reizdarmsyndrom (RDS) bei Migränepatienten zwei- bis viermal häufiger vorkommt als bei gesunden Kontrollpersonen, ist ein erster Hinweis darauf, dass das Darmmikrobiom eine Rolle spielt (1,2).
Ein Mechanismus, der sowohl bei Migräne als auch beim Darmmikrobiom eine Rolle zu spielen scheint, ist die Fehlfunktion verschiedener anatomischer Barrieren, darunter die Darm-Blut-Schranke, die Blut-Hirn-Schranke und die Blut-Hirnflüssigkeits-Schranke. Das Mikrobiom kann all diese Barrieren beeinflussen (3,4). Interessanterweise besteht die Blut-Hirn-Schranke aus Endothelzellen, und Studien an Kindern haben gezeigt, dass eine Endothel-Dysfunktion bei Migränepatienten vorkommt (5). Da das Mikrobiom auch die Blut-Hirnflüssigkeits-Schranke beeinflusst, ist es relevant, dass Migräne durch eine meningeale Entzündung gekennzeichnet ist, bei der sich Entzündungssignale über die Hirnflüssigkeit ausbreiten (6).
Die wichtigsten pharmakologischen Behandlungen der Migräne sind Serotonin-Agonisten. Dies basiert auf überzeugenden mechanistischen Studien seit den 1950er Jahren, die gezeigt haben, dass Serotonin eine entscheidende Rolle bei Migräne spielt (7). Serotonin wird im Körper aus der Aminosäure Tryptophan synthetisiert, und es ist bekannt, dass das Darmmikrobiom den Tryptophan-Stoffwechsel beeinflusst (8,9). Ein gestörtes Gleichgewicht anderer Tryptophan-Metaboliten, wie Kynurenin, wird mit Migräne und RDS in Verbindung gebracht (9).
Eine Überwucherung von Helicobacter pylori und anderen pathogenen Keimen wird ebenfalls mit Migräne assoziiert (8-10). Sowohl diese Faktoren als auch die bereits erwähnten Dysbalancen können durch Probiotika positiv beeinflusst werden, und mehrere randomisierte kontrollierte Studien (RCTs) haben gezeigt, dass spezifische Probiotika bei der Behandlung von Migräne wirksam sein können (11).
All diese Erkenntnisse zeigen, dass es sich lohnt, das Darmmikrobiom bei der Behandlung von Migränepatienten in Betracht zu ziehen. Eine einfache Möglichkeit, schnell herauszufinden, ob ein gestörtes Mikrobiom bei einem bestimmten Patienten eine Rolle spielen könnte, ist die Verwendung der Bristol-Stuhlskala (BSS) und eines Fragebogens zu gastrointestinalen Beschwerden. Oft ist es notwendig, gezielt nachzufragen, da viele Patienten zurückhaltend sind, über ihren Stuhlgang zu sprechen und den Zusammenhang zwischen Darm und Migräne nicht sofort erkennen.
Interessieren Sie sich für dieses einfache Tool? Dann können Sie die BSS und den Fragebogen kostenlos auf Deutsch, Niederländisch oder Englisch erhalten, indem Sie auf diese E-Mail antworten. Falls gastrointestinale Beschwerden vorliegen, kann eine Stuhlanalyse Aufschluss darüber geben, welche Mikrobiom-Funktionen gestört sind (z. B. eine durchlässige Darmbarriere, pathogene Keime, Entzündungen usw.). Basierend darauf kann eine evidenzbasierte, personalisierte Mikrobiom-Therapie eingesetzt werden, um diese Störungen gezielt zu behandeln.
References:
https://doi.org/10.1002/brb3.2291
https://doi.org/10.1155/2022/8690562
https://doi.org/10.1177/1535370217743766
https://doi.org/10.1111/ejn.15878
https://doi.org/10.1111/ped.14946
https://doi.org/10.1186/s10194-021-01353-0
https://doi.org/10.1152/physrev.00034.2015
https://doi.org/10.1186/s10194-020-1078-9
https://doi.org/10.3390/ijms221810134
https://doi.org/10.2147/NDT.S144955
https://doi.org10.1080/1028415X.2020.1764292
31: Evidenzaktualisierungen
Evidenz wird kontinuierlich aktualisiert
Um die bestmöglichen Behandlungsoptionen anzubieten, aktualisiert das Microbiome Center kontinuierlich die Evidenz aller verfügbaren Inhaltsstoffe.
Ein aktuelles Beispiel ist die Hinzufügung von Evidenz für Bacillus clausii UBBC-07. Neue Studien wurden zu seinen Auswirkungen auf Infektionen der oberen Atemwege, die Prävention von durch Strahlentherapie induzierter Mukositis und Colitis ulcerosa veröffentlicht (1-3). Eine gut durchgeführte RCT mit 90 Kindern zeigte, dass die Behandlung mit B. clausii UBBC-07 im Vergleich zu Placebo zu einer erheblichen Reduzierung der durchschnittlichen Anzahl, Dauer und Schwere von Infektionen der oberen Atemwege führte (1). Eine weitere RCT untersuchte, ob dieser Stamm die Nebenwirkungen der Strahlentherapie bei Patienten mit Kopf- und Halskrebs, insbesondere Mukositis, reduzieren kann (2). Es wurde festgestellt, dass die Zeit bis zum Auftreten von Mukositis länger war, die Dauer der Mukositis kürzer war und vor allem, dass die Schwere der Mukositis deutlich geringer war. Eine dritte RCT bei IBD-Patienten zeigte einen Vorteil von B. clausii UBBC-07 bei der Krankheitsaktivität und Entzündungsmarkern im Vergleich zu Placebo bei Patienten mit Colitis ulcerosa, jedoch nicht bei Patienten mit Morbus Crohn. Dies zeigt die Bedeutung der Unterscheidung zwischen diesen beiden verschiedenen Krankheiten innerhalb des IBD-Klusters.
Ein weiteres Beispiel für einen Stamm mit kürzlich hinzugefügter Evidenz ist Bacillus coagulans Unique IS-2. Dieser Stamm wurde ebenfalls auf seine Wirkung bei Colitis ulcerosa untersucht, mit ähnlichen Ergebnissen wie die zuvor genannte B. clausii UBBC-07-Studie (4). Interessanterweise gab es bereits Evidenz dafür, dass B. coagulans Unique IS-2 bei Verstopfung wirksam ist, und eine neue gut durchgeführte RCT bestätigt, dass dieser Stamm eine große Wirkung auf Verstopfung hat (5).
Diese und andere Evidenzaktualisierungen werden kontinuierlich verarbeitet und zum Advice Aid hinzugefügt, sodass die vorgeschlagenen personalisierten Präparate immer auf dem besten verfügbaren Wissen und dem umfassendsten Überblick über die wissenschaftliche Evidenz basieren. Alle Studien sind unter der i-Schaltfläche jedes Inhaltsstoffs zu finden.
References:
30: Vaginale Zäpfchen
Die Rolle des vaginalen Mikrobioms bei vaginalen Beschwerden
Vaginale Beschwerden sind in der Hausarztpraxis weit verbreitet. Eine niederländische Veröffentlichung aus dem Jahr 2002 besagt, dass 40% der befragten Frauen in der vergangenen Woche vaginale Ausfluss hatten (1). Internationale Forschungen zeigen, dass die Prävalenz von bakterieller Vaginose in westlichen Ländern zwischen 5-20% variiert, obwohl es große Unterschiede zwischen den Ländern gibt (2).
Wie der Darm, die Haut oder die Lunge hat die Vagina ihr eigenes, spezifisches Mikrobiom, und viele vaginale Beschwerden stehen im Zusammenhang mit einer gestörten vaginalen Mikrobiota. So ist die häufigste Ursache für abnormen vaginalen Ausfluss, bakterielle Vaginose, durch vaginale Dysbiose gekennzeichnet, die den Beschwerden vorausgeht (3). Wenn bakterielle Vaginose zu Beschwerden führt, wird sie typischerweise mit Antibiotika behandelt, was jedoch eine hohe Rückfallrate hat (2). Dies ist nicht überraschend, da Antibiotika das vaginale Mikrobiom noch weiter stören können.
Neben vaginalen Beschwerden spielt das vaginale Mikrobiom auch eine Rolle bei der Fruchtbarkeit. Die Chance auf eine erfolgreiche Schwangerschaft ist höher, wenn ein gesundes, von Lactobacillus dominiertes vaginales Mikrobiom vorhanden ist (4,5).
Da viele vaginale Beschwerden mit vaginaler Dysbiose in Verbindung stehen, ist eine Intervention, die auf das vaginale Mikrobiom abzielt, erwünscht. Aus diesem Grund hat das Microbiome Center zusammen mit dem Apotheker und einer Reihe von Ärzten in unserem Netzwerk vaginale Zäpfchen entwickelt. Diese enthalten drei probiotische Stämme in hoher Dosis, darunter zwei Lactobacillus crispatus-Stämme. Diese Bakterienart wird stark mit einem gesunden vaginalen Mikrobiom in Verbindung gebracht (3). Die Zäpfchen können online als Set von 30 Stück verschrieben werden und werden magistral vom Apotheker hergestellt.
Wenn Sie mehr über das vaginale Mikrobiom, seine Rolle bei vaginalen Beschwerden wie bakterieller Vaginose und vulvovaginaler Candidiasis sowie bei der Fruchtbarkeit erfahren möchten und wie vaginale Zäpfchen verwendet werden können, können Sie an unserem Online-Webinar (auf Deutsch) am 20. April 2023 von 19:30 bis 21:00 Uhr teilnehmen.
References:
1. https://www.henw.org/artikelen/vaginale-klachten
2. https://doi.org/10.1016/j.ejogrb.2019.12.035
3. https://doi.org/10.3389/fcimb.2021.631972
29: Die Mikrobiom-Migraine-Verbindung
Das Darmmikrobiom spielt eine Rolle bei Migräne
Migräne ist eine invalidisierende, weit verbreitete Erkrankung, die etwa 15% der Bevölkerung betrifft. Es ist allgemein bekannt, dass viele Migränepatienten unter Übelkeit oder Erbrechen leiden, aber auch andere gastrointestinale Beschwerden kommen häufig vor. Migränepatienten haben beispielsweise 2-4 Mal häufiger Reizdarmsyndrom (IBS) als gesunde Menschen (1,2). Dies ist ein starker Hinweis darauf, dass die Darmgesundheit mit Migräne in Verbindung steht.
In den letzten Jahren wurden verschiedene Mechanismen identifiziert, die eine Rolle in der Mikrobiom-Migräne-Verbindung spielen könnten. So werden bei Migränepatienten gestörte anatomische Barrieren, wie die Darm-Blut- und Blut-Hirn-Schranke, beobachtet, was zu systemischen und neuroinflammatorischen Reaktionen führen kann (3,4). Auch die Insulin-Signalisierung ist bei Migränepatienten gestört, und es ist bekannt, dass das Mikrobiom diese direkt beeinflussen kann (4,5).
Darüber hinaus ist allgemein bekannt, dass eine gestörte Serotonin-Signalisierung eine wichtige Rolle in der Pathogenese der Migräne spielt (6). Es ist wichtig, dass der Stoffwechsel des Vorläufers Tryptophan über die Serotonin-, Indol- oder Kynurenin-Wegen vom Darmmikrobiom beeinflusst wird (7). Es ist zum Beispiel bekannt, dass Metaboliten aus dem Kynurenin-Weg den NMDA-Rezeptor beeinflussen, der eine Rolle bei der kortikalen Spread Depression der Migräne spielt. Interessanterweise sind auch verschiedene Tryptophan-Metaboliten bei IBS-Patienten gestört.
Ein weiterer potenzieller Mechanismus, der identifiziert wurde, ist das Überwachsen von pathogenen Mikroben. So wird eine Helicobacter pylori-Infektion mit Migräne in Verbindung gebracht (7). Zudem wurde auch ein Überwachsen anderer pathogener Bakterien und Hefen bei Migränepatienten festgestellt (8). Da viele pathogene Bakterienarten in der Lage sind, Histamin zu synthetisieren, ist es interessant, dass auch Histaminempfindlichkeit eine Rolle bei Migräne spielt (9).
Zusammenfassend lässt sich sagen, dass die Identifizierung dieser Mechanismen darauf hindeutet, dass, wenn ein Migränepatient auch gastrointestinale Beschwerden hat, eine funktionelle fäkale Analyse helfen kann, die betroffenen Wege bei dieser Person zu identifizieren. Auf dieser Basis und unter Berücksichtigung anderer Beschwerden und medizinischer Probleme kann eine gezielte Intervention zusammengestellt werden.
References:
- https://doi.org/10.1002/brb3.2291
- https://doi.org/10.1155/2022/8690562
- https://doi.org/10.1177/1535370217743766
- https://doi.org/10.1111/ped.14946
- https://doi.org/10.1016/j.molcel.2020.03.005
- https://doi.org/10.1152/physrev.00034.2015
- https://doi.org/10.3390/ijms221810134
- https://doi.org/10.2147/NDT.S144955
- https://doi.org/10.1186/s10194-019-0984-1
28: Neuer Inhaltsstoff: Pasteurisierte Akkermansia muciniphila
Pasteurisierte Akkermansia muciniphila, ein Postbiotikum
Bei etwa einem von acht Stuhlprobenanalysen ist Akkermansia muciniphila stark vermindert (weniger als 1×10^5 CFU/g), und in einer größeren Gruppe ist sie erheblich reduziert. Dies ist ein Hinweis auf eine gestörte Schleimschicht, die einen wichtigen Bestandteil der Darmbarriere darstellt. A. muciniphila ist dafür bekannt, die Integrität der Darmepithelzellen und die Dicke der Schleimschicht zu verbessern und spielt eine Rolle in der Immunregulation des Wirts, wodurch es die Darmgesundheit fördert (1). Interessanterweise können wesentliche Teile der positiven Effekte von A. muciniphila auf Amuc_1100 zurückgeführt werden, ein spezifisches pili-ähnliches Protein, das aus der äußeren Membran von A. muciniphila isoliert wurde (2). Aus diesem Grund ist pasteurisierte A. muciniphila genauso effektiv wie lebende Zellen, wie in der ersten humanen Studie bis heute gezeigt wurde (3). Da A. muciniphila pasteurisiert ist und der aktive Inhaltsstoff daher nicht aus lebenden Bakterien besteht, wird es als Postbiotikum bezeichnet (4).
Die zuvor erwähnte RCT zeigt, dass die Supplementierung mit pasteurisierter A. muciniphila zu einer Verringerung der Insulinresistenz sowie zu Gewichts- (und Körperfett-)verlust führt (3). Diese Wirkung wird durch Beweise aus zahlreichen Tierstudien gestützt, wie sie beispielsweise in einer systematischen Übersichtsarbeit von zehn Tierstudien gezeigt wird (5). Diese und andere therapeutische Effekte (z. B. bei Colitis oder Allergien) werden mit den entzündungshemmenden und darmbarrierewiederherstellenden Effekten in Verbindung gebracht, die sowohl in der RCT als auch in vielen Tierstudien gezeigt wurden (3, und z. B. 6, 7). Dazu gehört auch die Stimulation der Schleimproduktion und eine erhöhte Dicke der Schleimschicht (6).
Ab dem 1. Februar ist pasteurisierte A. muciniphila als neuer Baustein verfügbar, den du als Inhaltsstoff für MyOwnBlend auswählen kannst. Weitere Informationen über dieses Postbiotikum und seine Wirkungen findest du unter dem (i)-Button auf unserer Plattform.
Wir organisieren ein Webinar, um weiterführende Hintergrundinformationen zur Rolle von A. muciniphila in Gesundheit und Krankheit am 23. Februar und 21. März von 19:30 bis 21:00 Uhr zu geben. Wenn du interessiert bist, kannst du auf diese E-Mail antworten und dein bevorzugtes Datum angeben.
References:
- https://doi.org/10.1111/1751-7915.13410
- https://doi.org/10.1371/journal.pone.0173004
- https://doi.org/10.1038/s41591-019-0495-2
- https://doi.org/10.1038/s41575-021-00440-6
- https://doi.org/10.3390/microorganisms9051098
- https://doi.org/10.12182/20220160304
- https://doi.org/10.3389/fmicb.2019.02259
27: Neue Stamm effektiv bei Akne und Karies
Neuer Stamm: Lacticaseibacillus rhamnosus SP1
Wenn wir interessante Inhaltsstoffe für Mikrobiom-Behandlungen entdecken, versuchen wir, diese verfügbar zu machen, um die Behandlungsmöglichkeiten für Patienten weiter auszubauen. Wir haben nun den Stamm Lacticaseibacillus rhamnosus SP1 hinzugefügt, der unter anderem auf seine Wirkung bei Akne und Karies untersucht wurde. Es ist wichtig zu erwähnen, dass viele Wirkungen stammspezifisch sind und es viele verschiedene Stämme innerhalb der L. rhamnosus-Art gibt. Es muss beachtet werden, dass nicht alle Stämme dieser Art dieselbe Wirkung haben werden wie dieser Stamm, der als SP1 bezeichnet wird.
Eine kleine, aber gut durchgeführte randomisierte kontrollierte Studie (RCT) mit L. rhamnosus SP1 zeigt, dass dieser Stamm zu einer Verbesserung oder merklichen Verbesserung der Akne-Symptome im Vergleich zu einem Placebo führt (1). Darüber hinaus zeigte diese Studie, dass die Verwendung von L. rhamnosus SP1 eine deutliche Abnahme der Expression von Insulin-like Growth Factor 1 (IGF1) in Hautproben der probiotischen Gruppe im Vergleich zum Placebo verursachte, was einen Effekt auf die Insulin-Signalisierung belegt. Tatsächlich zeigt zunehmendes Beweismaterial, dass eine gestörte Darmmikrobiota mit Akne in Verbindung steht, teilweise aufgrund der Wirkung auf die Insulin-Signalisierung, aber klinische Studien mit probiotischen Interventionen sind selten (2). Das macht L. rhamnosus SP1 bereits zu einer interessanten Ergänzung.
Eine andere Studie, die mit diesem Stamm durchgeführt wurde, ist eine große RCT (und eine Subgruppenanalyse davon), die den Effekt dieses Stammes auf die Prävention von Karies bei Kleinkindern untersuchte. Die Ergebnisse zeigen, dass L. rhamnosus SP1 im Vergleich zum Placebo effektiv Karies verhindert (3,4). Eine andere RCT zur Mundgesundheit liefert Beweise für eine Wirkung auf Candida-assoziierte Zahnprothesenstomatitis (5). Diese Studie liefert auch direkten Beweis für eine hemmende Wirkung auf (orale) Candida.
Weitere Informationen zu diesem Stamm und seinen Wirkungen sind unter der (i)-Schaltfläche auf unserer Plattform zu finden.
References:
- https://doi.org/10.3920/BM2016.0089
- https://doi.org/10.3390/microorganisms10071303
- https://doi.org/10.1177/0022034515623935
- https://doi.org/10.1007/s00784-020-03712-8
- https://doi.org/10.1111/adj.12692
26: : Korrelation zwischen Depression und Enterobacter
Datenanalyse: Enterobacter und Depression
Vor allem ist Microbiome Center eine Netzwerkorganisation mit dem Ziel, den Lernzyklus drastisch zu verkürzen. Das bedeutet, dass du, die Ärzte in unserem Netzwerk, evidenzbasierte personalisierte Mikrobiom-Behandlungen verschreiben kannst und gleichzeitig neues Wissen generierst. Die Analyse anonymisierter Daten (z. B. Ergebnisse der Stuhlanalyse) mit Zustimmung des Patienten kann neue Erkenntnisse liefern, die zukünftigen Patienten zugutekommen und noch bessere Behandlungen ermöglichen. Unsere kürzlich durchgeführte Datenanalyse hat solche Erkenntnisse geliefert, nämlich eine Korrelation zwischen dem Überwachsen von Enterobacter spp. und der Anfälligkeit für Traurigkeit (d.h. Depression oder eine gedrückte Stimmung).
In der gesamten Klientenpopulation liegt die Prävalenz einer gedrückten Stimmung bei etwa 18%. Bei Klienten, die hohe Werte von möglicherweise pathogenen Enterobacter-Arten in ihren Stuhlanalyse-Ergebnissen haben, liegt die Prävalenz einer gedrückten Stimmung jedoch fast doppelt so hoch, nämlich bei 29%. Dies deutet darauf hin, dass dieser potenzielle Krankheitserreger mit Depressionen assoziiert ist.
Eine Literaturrecherche zeigt ähnliche Ergebnisse, wenn auch weniger explizit, wobei sich herausstellt, dass Patienten mit bipolarer Depression höhere Werte von Enterobacter spp. haben im Vergleich zu gesunden Kontrollen (1). Dies wurde auch bei Patienten mit später Depression (2) festgestellt. Die Forscher der ersten Studie beschreiben auch eine Assoziation zwischen erhöhter Entzündungsaktivität und Überwachsen von Enterobacter spp. Entzündungen werden mit Depressionen in Verbindung gebracht (3). Zusammenfassend deuten unsere Befunde und die Literatur darauf hin, dass erhöhte Enterobacter spp. Entzündungen verursachen können und damit Depressionen hervorrufen können. Dies ist eine nützliche Erkenntnis, da spezifische probiotische Stämme dafür bekannt sind, potenzielle Krankheitserreger wie Enterobacter spp. zu hemmen und Entzündungen zu reduzieren, was bei Klienten mit Depressionen hilfreich sein könnte.
Dies ist nur ein Beispiel dafür, wie wir Erkenntnisse gewinnen, während wir den Klienten helfen. Gemeinsam lernen wir aus der Praxis und verbessern kontinuierlich die Behandlungen. Wenn du mehr wissen möchtest, lass es uns wissen oder nimm an den Webinaren zur Datenanalyse (14. November, auf Niederländisch) oder Depression (14. Dezember, auf Niederländisch) teil. Diese Webinare werden Anfang 2023 auf Englisch wiederholt.
References:
https://doi.org/10.3389/fpsyt.2019.00784
https://doi.org/10.3389/fnagi.2022.885393
https://doi.org/10.1111/ejn.14631
https://doi.org/10.1016/j.clnu.2018.09.010
25: L. plantarum DR7, Arthritis und Mikrobielles Butyrat
Neuer Stamm: Lactiplantibacillus plantarum DR7
Ein neuer Stamm wurde zur Liste hinzugefügt, aus der du wählen kannst: L. plantarum DR7. Dieser Stamm wurde aus frischer Kuhmilch in Malaysia isoliert (1). Er hat entzündungshemmende Effekte, die sowohl in präklinischen als auch in klinischen Studien nachgewiesen wurden (2-4), und stimuliert die AMPK-Aktivität (5). AMPK (Adenosin-5′-monophosphat-aktivierte Proteinkinase) ist ein zellulärer Energiemesser, und eine reduzierte AMPK-Aktivität wird unter anderem mit Insulinresistenz in Verbindung gebracht (6). Tatsächlich ist ein Wirkmechanismus des bekannten Antidiabetikums Metformin die Aktivierung von AMPK (7). Die Behandlung mit Metformin hat Auswirkungen auf viele Erkrankungen, einschließlich der Reduktion von Angstzuständen, was vermutlich mit der Wirkung auf AMPK zusammenhängt (8). Interessanterweise zeigt eine qualitativ hochwertige randomisierte kontrollierte Studie (RCT), dass dieser AMPK-stimulierende Stamm L. plantarum DR7 tatsächlich Stress und Angst reduziert (4). Darüber hinaus kann dieser Stamm Atemwegs-Pathogene in vitro hemmen und hat sich in einer RCT als wirksam erwiesen, um die Inzidenz und Schwere von oberen Atemwegsinfektionen zu verringern (4,9). Weitere Beweise und Informationen zu diesem Stamm sind in der Beschreibung dieses Inhaltsstoffs in unserem System zu finden.
Rheumatoide Arthritis in Verbindung mit niedrigen Mikrobiellen Butyrat-Spiegeln
Eine sehr ausgeklügelte Studie, die im Februar dieses Jahres in Science Advances veröffentlicht wurde, hat gezeigt, dass Darmbutyrat-metabolisierende Arten eine Rolle bei rheumatoider Arthritis spielen (10). Der Begriff „butyrat-metabolisierend“ bezieht sich sowohl auf die Produktion als auch den Verbrauch von Butyrat, und die Forscher fanden heraus, dass die Anzahl der Butyrat-verbrauchenden Arten bei rheumatoiden Arthritis-Patienten, die noch nicht behandelt wurden, viel höher war als bei gesunden Kontrollen. Tatsächlich waren 51 von 55 rheumatoide Arthritis-assoziierte Butyrat-Metabolisierer Butyrat-Konsumenten, von denen 46 in höheren Zahlen bei den rheumatoiden Arthritis-Patienten vorhanden waren. Dies deutet darauf hin, dass bei rheumatoider Arthritis das verfügbare Niveau an mikrobiellem Butyrat für den Wirt signifikant gesenkt wird. Anschließend validierten die Forscher die Entdeckung des unausgewogenen Verhältnisses zwischen Butyrat-produzierenden und -konsumierenden Arten in einer unabhängigen Kohorte. In dieser zweiten Kohorte wurde ebenfalls gezeigt, dass sowohl die fecalen als auch die Serumspiegel von Butyrat bei rheumatoiden Arthritis-Patienten im Vergleich zu gesunden Kontrollen gesenkt waren. Schließlich zeigten die Forscher, dass Butyrat-Supplementierung in einem Tierversuchsmodell für Arthritis zu einer deutlich niedrigeren Inzidenz (11 % vs. 85 %) und Schwere der Arthritis im Vergleich zur Kontrollgruppe führte. Zusammen liefern diese Ergebnisse starke Beweise für eine Rolle von Butyrat-metabolisierenden Arten bei rheumatoider Arthritis. Dies deutet darauf hin, dass Interventionen mit Butyrat-produzierenden Arten wie Anaerobutyricum soehngenii oder Clostridium butyricum, die beide über unsere Plattform verfügbar sind, möglicherweise vorteilhaft sein können.
References:
- https://doi.org/10.1089/jmf.2007.0144
- https://doi.org/10.3920/BM2019.0200
- https://doi.org/10.3920/BM2018.0135
- https://doi.org/10.3168/jds.2018-16103
- https://doi.org/10.3920/BM2019.0058
- https://doi.org/10.1152/ajpendo.1999.277.1.E1
- https://doi.org/10.1007/s00125-017-4342-z
- https://doi.org/10.1007/s11011-015-9677-x
- https://doi.org/10.3390/microorganisms9030528
- https://doi.org/10.1126/sciadv.abm1511
24: Internationalisierung, Sommerbrise, Fibromyalgie
Internationalisierung
Bei der Gründung im Jahr 2018 begann das Microbiome Center seinen Dienst in den Niederlanden. Seitdem haben immer mehr Ärzte aus anderen Ländern uns gefunden und wollten personalisierte Mikrobiombehandlungen in ihrer Praxis einsetzen. Ab 2021 haben wir unseren Service daher auf andere europäische Länder ausgeweitet. Heute ist der Service des Microbiome Centers für Ärzte in sechs Ländern verfügbar, darunter Deutschland, Schweiz und Belgien. Um alle neuen Kollegen in unserem Netzwerk bedienen zu können, werden die „Wissensblitze“, die wir regelmäßig verschicken, ab sofort auf Englisch verfasst und heißen jetzt „Insights Flash“.
Sommerbrise: Haben Furze ein Mikrobiom?
Die Sommerzeit bietet Raum für ein wenig Spaß, und deshalb stellten wir uns die Frage, ob Furze ein Mikrobiom haben könnten. In dieser Frage steckt auch etwas Ernstes, denn es ist bekannt, dass eine Mikrobiota-Übertragung zwischen Menschen, die eng zusammenleben, stattfindet, aber wenig ist über die tatsächlichen Übertragungswege bekannt (1-3). Angesichts der Tatsache, dass jeder von uns durchschnittlich etwa zehnmal pro Tag furzt (4), ist überraschend wenig Forschung zur mikrobiellen Zusammensetzung von Furzen vorhanden. Tatsächlich konnten wir nur eine Veröffentlichung finden, die kaum als Studie bezeichnet werden kann. Ein Forscher testete, ob er Bakterien aus den Furzen eines Kollegen züchten konnte, und das konnte er tatsächlich (5). Angesichts der Tatsache, dass viele Bakterien nicht kultivierbar sind, wäre es nicht überraschend, wenn Furze viel mehr lebende Mikroben enthalten und möglicherweise eine Rolle bei der mikrobiellen Übertragung spielen.
Mikrobiom und Fibromyalgie
Obwohl die Anzahl und Qualität der Studien noch relativ niedrig sind, ist bekannt, dass das Darmmikrobiom und das Profil der mikrobiellen Metaboliten bei Fibromyalgiepatienten (FM) im Vergleich zu gesunden Individuen verändert sind (6,7). Eine kürzlich veröffentlichte Studie fügt neue Erkenntnisse zu diesem selten untersuchten Thema hinzu. Forscher fanden Veränderungen in den Konzentrationen sekundärer Gallensäuren und der Häufigkeit von Bakterienarten, die bekannt dafür sind, Gallensäuren zu metabolisieren, bei FM-Patienten im Vergleich zu gesunden Kontrollen (8). Die sekundäre Gallensäure namens Alpha-Muricholsäure wurde bei FM-Patienten fünfmal weniger gefunden als bei gesunden Kontrollen, und ein niedrigerer Wert war mit einer erhöhten Schwere der Symptome wie Schmerzen, Müdigkeit, unruhigem Schlaf und kognitiven Beschwerden verbunden. Diese Erkenntnisse könnten neue Wege zur Behandlung von FM-Patienten eröffnen, beispielsweise mit probiotischen Stämmen, die in der Lage sind, Alpha-Muricholsäure zu produzieren.
References:
- https://doi.org/10.1038/
s41564-019-0409-6 - https://doi.org/10.1038/
s41559-020-1220-8 - https://doi.org/10.1126/
science.aaz3834 - https://doi.org/10.1007/
BF02087912 - https://doi.org/10.1136/bmj.
323.7327.1449 - https://doi.org/10.1186/
s12891-020-03201-9 - https://pubmed.ncbi.nlm.nih.
gov/32116215/ - https://doi.org/10.1097/j.
pain.0000000000002694
23: SIBO Behandlung und Erfahrungen
Was ist SIBO?
In einem früheren Wissensblitz haben wir bereits über SIBO (Small Intestinal Bacterial Overgrowth, bakterielle Fehlbesiedlung des Dünndarms) gesprochen – ein für viele noch relativ unbekanntes Phänomen, das in der Praxis jedoch sehr häufig vorkommt. Es handelt sich um gastrointestinale (und systemische) Beschwerden, die durch eine übermäßige Anzahl atypischer Bakterien im Dünndarm verursacht werden (1,2).
Betroffene Patienten klagen über ein Völlegefühl und Bauchschmerzen, die sich nach dem Essen meist verschlimmern. Auch anhaltendes Aufstoßen und Blähungen, Durchfall oder Verstopfung, gestörte Fettaufnahme, Vitaminmängel (u. a. B12), eine beeinträchtigte Darmbarriere sowie eine gestörte Immunaktivität können auftreten (2).
Der häufige Rat, bei chronischen Bauchbeschwerden zusätzliche Ballaststoffe einzunehmen, verschlechtert bei SIBO die Symptome, da dies das bakterielle Überwachstum fördert. Auch viele klassische probiotische Stämme wirken in diesem Fall oft kontraproduktiv.
Was kann man bei SIBO tun?
Dank des personalisierten Ansatzes von MiBlend ist es möglich, gezielt jene probiotischen Stämme einzusetzen, für die Studien eine lindernde Wirkung bei SIBO gezeigt haben (3). Für mehrere MiBlend-Stämme liegen klinische Daten mit positiven Effekten bei SIBO vor.
Als Behandler können Sie dies ganz einfach nutzen: Wenn Sie bei der Rezeptauswahl die SIBO-Variante wählen (für 1 oder 2 Monate), erhält der Patient eine speziell abgestimmte MiBlend-Kombination inklusive Thermosflasche und einer angepassten Anwendungsempfehlung, die die Wirksamkeit im oberen Dünndarm erhöht.
Erfahrungen mit der SIBO-Behandlung
Letztlich zählt die Praxis – und daher haben wir erste Erfahrungen eingeholt. Schon jetzt gibt es viele positive Rückmeldungen von Patienten. Besonders auffällig war der Fall einer Frau, die trotz gesunder Lebensweise weiterhin unter Müdigkeit, Verstopfung und Hautproblemen litt. Erst nach der gezielten SIBO-Behandlung zeigte sich eine deutliche Besserung. Weitere Informationen finden Sie in der beigefügten Fallbeschreibung.
Referenties:
https://doi.org/10.1016/j.gtc.2017.09.008
https://doi.org/10.1016/j.advms.09.001
https://doi.org/10.1097/MCG.0000000000000814
22: Neuer Stamm, neues Präbiotikum
Neuer Stamm: L. sakei probio65
Kürzlich konnten wir einen einzigartigen Stamm in unser Sortiment aufnehmen: Latilactobacillus sakei probio65. Dieser Bakterienstamm wurde aus Kimchi isoliert und weist eine ausgezeichnete Überlebensfähigkeit im Magen-Darm-Trakt auf (1). Es gibt zahlreiche Studien über die Wirkung von L. sakei probio65 bei atopischer Dermatitis. Dazu gehören in-vitro- und präklinische Untersuchungen (siehe z. B. 1–3), aber auch zwei gut durchgeführte randomisierte kontrollierte Studien (RCTs) (4,5). Letztere zeigen deutliche positive Effekte auf verschiedene Aspekte der atopischen Dermatitis.
Darüber hinaus zeigen in-vitro-Studien eine starke hemmende Wirkung gegenüber verschiedenen Pathogenen (1). Interessant ist außerdem, dass dieser Stamm die Aktivität von α-Glukosidase und α-Amylase hemmen kann (6,7). Diese Enzyme sind für den Abbau von Kohlenhydraten verantwortlich, und ihre Hemmung gilt als therapeutischer Ansatz zur Behandlung von Diabetes – sie ist beispielsweise der Wirkmechanismus des Diabetesmedikaments Acarbose (6). Ein Tiermodell zeigte tatsächlich eine Verbesserung des Blutzuckerspiegels nach Gabe von L. sakei probio65 (6), was darauf hinweist, dass dieser Stamm auch beim metabolischen Syndrom und bei Diabetes nützlich sein könnte. Weitere Nachweise und Informationen zu diesem „Building Block“ finden Sie in der Beschreibung dieses Inhaltsstoffs in unserem System.
Am 28. Juni werden wir die Effekte bei atopischer Dermatitis in unserem Webinar zum Thema Allergie ausführlicher erläutern.
Neuer Stamm: L. sakei probio65
Kürzlich konnten wir einen einzigartigen Stamm in unser Sortiment aufnehmen: Latilactobacillus sakei probio65. Dieser Bakterienstamm wurde aus Kimchi isoliert und weist eine ausgezeichnete Überlebensfähigkeit im Magen-Darm-Trakt auf (1). Es gibt zahlreiche Studien über die Wirkung von L. sakei probio65 bei atopischer Dermatitis. Dazu gehören in-vitro- und präklinische Untersuchungen (siehe z. B. 1–3), aber auch zwei gut durchgeführte randomisierte kontrollierte Studien (RCTs) (4,5). Letztere zeigen deutliche positive Effekte auf verschiedene Aspekte der atopischen Dermatitis.
Darüber hinaus zeigen in-vitro-Studien eine starke hemmende Wirkung gegenüber verschiedenen Pathogenen (1). Interessant ist außerdem, dass dieser Stamm die Aktivität von α-Glukosidase und α-Amylase hemmen kann (6,7). Diese Enzyme sind für den Abbau von Kohlenhydraten verantwortlich, und ihre Hemmung gilt als therapeutischer Ansatz zur Behandlung von Diabetes – sie ist beispielsweise der Wirkmechanismus des Diabetesmedikaments Acarbose (6). Ein Tiermodell zeigte tatsächlich eine Verbesserung des Blutzuckerspiegels nach Gabe von L. sakei probio65 (6), was darauf hinweist, dass dieser Stamm auch beim metabolischen Syndrom und bei Diabetes nützlich sein könnte. Weitere Nachweise und Informationen zu diesem „Building Block“ finden Sie in der Beschreibung dieses Inhaltsstoffs in unserem System
References:
- https://doi.org/10.1089/jmf.2007.0144
- https://doi.org/10.1111/jam.12229
- https://doi.org/10.5021/ad.2014.26.2.150
- https://doi.org/10.1016/j.anai.2010.01.020
- https://doi.org/10.1007/s12602-020-09654-7
- https://doi.org/10.3390/biology10040348
- https://doi.org/10.1111/jfbc.12230
- https://doi.org/10.1007/s10620-005-2713-7
- https://doi.org/10.1111/j.1464-5491.1987.tb00843.x
- https://doi.org/10.5144/0256-4947.1990.525
- https://doi.org/10.3390/nu11092170
- https://doi.org/10.4318/tjg.2010.0121
- https://doi.org/10.1111/j.1365-2036.2010.04436.x
21: SIBO - Small Intestinal Bacterial Overgrowth
Jeder Behandler begegnet ihr früher oder später: der Small Intestinal Bacterial Overgrowth (SIBO), also der bakteriellen Fehlbesiedlung des Dünndarms. Sie verursacht gastrointestinale (und systemische) Beschwerden aufgrund einer erhöhten Anzahl atypischer Bakterien im Dünndarm (1,2). Doch oft wird SIBO nicht als solche erkannt.
Patienten mit SIBO klagen häufig über ein aufgeblähtes Gefühl und Bauchschmerzen, die sich nach dem Essen verschlimmern. Auch anhaltendes Aufstoßen und Blähungen, Durchfall oder Verstopfung, gestörte Fettaufnahme, Vitaminmängel (z. B. B12), eine geschwächte Darmbarriere sowie eine gestörte Immunaktivität können auftreten (2).
Bei chronischen Bauchbeschwerden wird häufig geraten, zusätzliche Ballaststoffe in Form von Nahrungsergänzungsmitteln oder ballaststoffreicher Kost aufzunehmen. Bei SIBO kann dies jedoch die Beschwerden verschlimmern, da das bakterielle Überwachstum dadurch gefördert wird. Aus der Praxis weiß man, dass viele klassische probiotische Stämme sogar kontraproduktiv wirken können. Vor diesem Hintergrund wird SIBO mitunter mit Antibiotika wie Rifaximin behandelt (2,3). Diese Therapie kann zwar Linderung verschaffen, jedoch auch das Mikrobiom weiter stören und das Risiko für C. difficile-Infektionen und Antibiotikaresistenzen erhöhen.
Deshalb wird empfohlen, die Ursachen gezielt anzugehen: Verbesserung der Darmmotilität, Reduktion der Aufnahme kurzkettiger Kohlenhydrate und der Einsatz von Fastenzeiten (1,4,5).
Auch gezielt ausgewählte Probiotika können hilfreich sein: Eine Meta-Analyse klinischer Studien zeigt, dass bestimmte probiotische Stämme die SIBO-Symptome lindern können (6). Allerdings sind nicht alle Stämme geeignet. Im Rahmen der MiBlend-Zusammenstellungen stehen mehrere probiotische Stämme zur Verfügung, für die klinische Wirksamkeit bei SIBO nachgewiesen wurde – darunter Bacillus coagulans Unique IS-2 (7) sowie Enterococcus faecium in Kombination mit Bacillus subtilis (8). Die wissenschaftlichen Grundlagen zu den jeweiligen Stämmen finden Sie in der Beschreibung der Inhaltsstoffe in unserem System.
Mehrere Kolleginnen und Kollegen haben in den letzten sechs Monaten gezielt Kombinationen bestimmter Stämme zur Behandlung von SIBO eingesetzt – mit zahlreichen positiven Rückmeldungen. Wenn Sie in der MiBlend-Beratungshilfe angeben, dass Beschwerden auf SIBO hindeuten, erscheinen diese spezifischen Stämme in der empfohlenen Rezeptur.
Neu ist außerdem die Möglichkeit, Probiotika in teilfermentierter Form einzunehmen, um die Wirksamkeit im oberen Dünndarm zu verbessern. Der Patient erhält dann zusammen mit MiBlend eine Thermosflasche und eine angepasste Gebrauchsanleitung. Die ersten praktischen Erfahrungen damit sind sehr positiv.
References:
- https://doi.org/10.1016/j.gtc.
2017.09.008 - https://doi.org/10.1016/j.
advms.09.001 - https://doi.org/10.1007/
s11894-019-0671-z - https://doi.org/10.1586/
17474124.2016.1110017 - https://doi.org/10.1146/
annurev-nutr-071816-064634 - https://doi.org/10.1097/MCG.
0000000000000814 - https://www.ncbi.nlm.nih.gov/
pmc/articles/PMC4311312/ - https://doi.org/10.3748/wjg.
v25.i17.2110
20: Probiotika bei Angst und Anspannung
Probiotika bei Angst und Anspannung
Kürzlich haben wir Lactiplantibacillus plantarum P-8 in unser Portfolio aufgenommen. Eine gut durchgeführte randomisierte, kontrollierte Studie (RCT) zeigt, dass dieser Stamm wirksam gegen Angst und Anspannung ist (1). In derselben Studie wurde auch ein positiver Effekt auf Stress beobachtet, wenn auch etwas weniger ausgeprägt (1). Dass dieses Probiotikum einen günstigen Einfluss auf Angst und Anspannung hat, passt zu der wachsenden Zahl an Studien, die belegen, dass das Mikrobiom eine Rolle bei Angst, Anspannung und Depression spielt (2) und dass Probiotika diesen Zustand verbessern können (3). Vermutet wird, dass dieser Effekt unter anderem mit dem Einfluss des Mikrobioms und von Probiotika auf Entzündungsaktivität zusammenhängt (2,4). Auch für L. plantarum P-8 wurden antiinflammatorische Effekte nachgewiesen – sowohl in Studien mit dem Einzelstamm als auch in Kombination mit anderen Stämmen (1,5,6). Darüber hinaus gibt es Hinweise aus Tiermodellen, dass dieser Stamm oxidative Stressreaktionen reduziert (7,8) – ein Aspekt, der ebenfalls mit Angst, Anspannung und Depression in Verbindung gebracht wird (9,10). Interessant ist auch, dass Studien mit L. plantarum P-8 zeigen, dass dieser Stamm die Sekretion von sekretorischem IgA (sIgA) erhöhen kann (11,12), da bekannt ist, dass Stress die sIgA-Ausscheidung senken kann (13). Zusammenfassend lässt sich sagen, dass das Mikrobiom mehrere Mechanismen beeinflusst, die bei Angst und Anspannung eine Rolle spielen – und dass Probiotika diese Prozesse modulieren können.
Weitere wissenschaftliche Nachweise und Informationen zu diesem Stamm finden Sie in der Beschreibung dieses Inhaltsstoffs in unserem System.
References:
https://doi.org/10.1016/j.clnu.2018.09.010
https://doi.org/10.1016/j.cpr.2020.101943
https://doi.org/10.1016/j.neubiorev.2019.03.023
https://doi.org/10.1002/jnr.24476
https://doi.org/10.1007/s00394-020-02437-4
https://doi.org/10.1111/1751-7915.13661
https://doi.org/10.1007/s00394-020-02437-4
https://doi.org/10.3390/ani10040548
https://doi.org/10.1080/10715762.2018.1475733
https://doi.org/10.4161/oxim.2.2.7944
https://doi.org/10.1016/j.nut.2013.11.018
https://doi.org/10.1016/j.intimp.2015.07.024
https://doi.org/10.3389/fnint.2013.00086
19: Ernährung & Probiotika und Einladung Long-Covid
Ernährung und/oder Probiotika: Wann ist der Einsatz am vielversprechendsten?
Immer wieder werden wir gefragt, ob die Anpassung von Ernährung und Lebensstil nicht ausreicht, um das Mikrobiom zu regenerieren. Tatsächlich ist bekannt, dass eine Ernährungsumstellung innerhalb von ein bis wenigen Tagen die Zusammensetzung des Mikrobioms verändern kann – ähnlich wie etwa Stressbelastung (1,2).
Studien zeigen jedoch auch, dass die Effekte individuell sehr unterschiedlich ausfallen. So wie ein gesundes Mikrobiom widerstandsfähig gegenüber Störungen ist, kann auch ein gestörtes Mikrobiom stabil bleiben und nur schwer durch Interventionen verändert werden (3). Dies wird als Stabilität oder Resilienz bezeichnet (3,4,5).
Das Mikrobiom ist ein komplexes Ökosystem, vergleichbar mit einem Wald. Regen, ein Insektenbefall oder ein Waldbrand beeinflussen die Zusammensetzung der Vegetation, aber das Ökosystem als Ganzes erholt sich in der Regel. In manchen Fällen sind die Störungen jedoch so gravierend, dass das System nicht mehr in seinen ursprünglichen gesunden Zustand zurückfindet. Das Mikrobiom erreicht dann einen neuen stabilen, aber dysbiotischen Gleichgewichtszustand, der nur schwer in ein gesundes Gleichgewicht zurückgeführt werden kann (3).
Wenn Ernährung und Lebensstil allein nicht ausreichen, kann eine personalisierte probiotische Intervention in Betracht gezogen werden, um den Übergang von einem ungesunden zu einem gesunden Gleichgewicht zu unterstützen (4,6).
PASC (Long Covid) und das Mikrobiom: Einladung zur Zusammenarbeit
In Wissensblitz #10 haben wir bereits auf den Zusammenhang zwischen COVID-19 und dem Darmmikrobiom hingewiesen (7). Inzwischen wurde weitere Forschung veröffentlicht, die die wichtige Rolle des Mikrobioms und der Darmpermeabilität unterstreicht (8). Es wird sogar vermutet, dass das Mikrobiom eine Rolle bei der Abwehr von Viren wie SARS-CoV-2 spielen könnte (9).
In den letzten Monaten wurde deutlich, dass viele COVID-Patienten langanhaltende, postinfektiöse Beschwerden entwickeln. Auch wenn meist von Long Covid gesprochen wird, ist der Begriff „Post-Acute Sequelae of COVID-19“ (PASC) präziser (10).
Postinfektiöse Beschwerden sind nicht einzigartig für COVID-19 – auch nach vielen bakteriellen oder viralen Infektionen treten bei einem Teil der Patienten chronische Symptome auf (10). Es gibt eine Vielzahl von Mechanismen, die bei PASC eine Rolle spielen könnten (eine ausgezeichnete Übersicht liefert Referenz 8). Einer dieser Mechanismen ist ein gestörtes Darmmikrobiom.
Wir vermuten, dass Mikrobiom-Interventionen in bestimmten Fällen den Genesungsprozess unterstützen können. Wir sind neugierig auf Ihre Erfahrungen und möchten gemeinsam mit Ihnen herausfinden, ob und wie eine Mikrobiom-Therapie zur Erholung von PASC beitragen kann.
Haben Sie PASC-Patientinnen oder -Patienten in Ihrer Praxis, bei denen auch eine Mikrobiom-Dysbiose oder gastrointestinale Beschwerden eine Rolle spielen? Dann laden wir Sie herzlich ein, sich mit uns in Verbindung zu setzen und Ihre Erfahrungen mit uns zu teilen. Wenn Sie keine Zeit haben, etwas schriftlich zusammenzufassen, rufen wir Sie gerne an.
Wir erstellen eine Übersicht über die Fallberichte und Erfahrungen von Ihnen und Ihren Kolleginnen und Kollegen, um daraus neue Erkenntnisse zu gewinnen und mit allen Beteiligten zu teilen. Auf diese Weise können wir gemeinsam den Zyklus von Erfahrung → Wissen → Anwendung möglichst kurz halten.
Auch wenn Sie Anregungen haben, wie wir dieses Thema weiterverfolgen oder mit welchen Partnern wir zusammenarbeiten könnten, freuen wir uns auf Ihre Nachricht. Wir sind sehr gespannt, ob wir gemeinsam etwas in Bewegung bringen können.
References:
- https://doi.org/10.1038/
nature12820 - https://doi.org/10.1371/
journal.pone.0129996 - https://doi.org/10.1038/
nrmicro.2017.58 - https://doi.org/10.1136/
gutjnl-2020-321747 - https://doi.org/10.1038/
nature11550 - https://doi.org/10.3389/fmicb.
2020.572921 - https://www.microbiome-center.
nl/Medici/Kennisflits/ - https://doi.org/10.3389/fimmu.
2021.708149 - https://www.
nationalgeographic.nl/ darmflora-zou-ingezet-kunnen- worden-in-strijd-tegen- virussen - https://doi.org/10.3389/fmicb.
2021.698169
18: Praktische Neuigkeiten: Neue Verpackungsform, neue Funktion
Neue Verpackungsform
Wir erhalten regelmäßig Anfragen zur Anschlussbehandlung nach einer MiBlend-Therapie. Unser bisheriger Rat war, ein zuvor verschriebenes Rezept zu wiederholen und nach Bedarf anzuwenden. Da das Produkt jedoch nur drei Monate haltbar war, war eine längerfristige Nutzung für viele Patient*innen schwierig.
Zur Lösung dieses Problems haben wir eine neue Verpackungsform entwickelt: 12 vakuumversiegelte Beutel (Pouches) mit jeweils 100 g Inhalt. Diese Pouches können bis zu einem Jahr eingefroren und bei Bedarf einzeln aus dem Gefrierschrank entnommen werden.
Bitte weisen Sie Ihre Patient*innen darauf hin, die Auftauhinweise in der Packungsbeilage sorgfältig zu beachten, um sicherzustellen, dass die probiotischen Bakterien das Auftauen gut überstehen (z. B. keine Feuchtigkeit durch zu schnelles Öffnen). Nach dem Öffnen ist ein Beutel noch zwei Monate haltbar.
Diese Option steht Ihnen ab sofort zur Verfügung. Die Pouches können jedoch nur für Folgebehandlungen nach einer vorangegangenen MiBlend-Therapie verschrieben werden. Weitere Informationen finden Sie in der beiliegenden Packungsbeilage.
Wiederholungsanfragen durch Patient*innen
Aus unseren Servicegesprächen mit Patient*innen wissen wir, dass viele sich eine einfache Möglichkeit wünschen, ihre behandelnde Fachperson um ein Wiederholungsrezept zu bitten.
Um diesem Wunsch entgegenzukommen, haben wir auf der Startseite des Patient*innenportals einen Button hinzugefügt, über den ein Wiederholungsrezept angefragt werden kann. Anschließend liegt es an Ihnen als behandelnder Fachperson, diesem Antrag zuzustimmen oder ihn abzulehnen.
Wenn ein solcher Antrag eingeht, erscheint auf Ihrer Startseite ein orangefarbener Benachrichtigungs-Button. Über diesen können Sie den Antrag annehmen oder ablehnen und geben damit Ihre digitale Unterschrift für das Rezept.
Auch für Sie haben wir den Vorgang vereinfacht: In der Übersicht aller Rezepte (über den Menüpunkt „Rezepte“ auf der linken Seite erreichbar) sehen Sie bei allen geeigneten Rezepten ein Wiederholungs-Symbol.
Auch auf der Detailseite eines Rezepts wird nun ein Wiederholen-Button angezeigt. Wenn Sie diesen anklicken, gelangen Sie zur bekannten Rezeptseite, auf der alle Zutaten bereits vorausgefüllt sind. Dort können Sie aus allen verfügbaren Verpackungsformen wählen – einschließlich der oben beschriebenen Pouches – und bei Bedarf die Rezeptur anpassen.
17: 17: Neue Stämme, Mechanismen
Zwei neue Stämme in einem Building Block
Kürzlich haben wir einen neuen Building Block hinzugefügt, der diesmal aus zwei neuen Stämmen besteht: einem Enterococcus faecium– und einem Bacillus subtilis-Stamm. Diese beiden Stämme sind die aktiven Inhaltsstoffe eines Medikaments, das in Asien auf dem Markt ist und dort intensiv untersucht wurde.
Eine Metaanalyse von 53 randomisierten kontrollierten Studien (RCTs) zeigt, dass diese Kombination bei Colitis ulcerosa wirksam ist (1). Darüber hinaus liefert die Metaanalyse direkte Evidenz für eine entzündungshemmende Wirkung. Weitere RCTs belegen unter anderem eine Wirkung bei Bauchschmerzen und Reizdarmsyndrom (IBS) (2,3), sowie beim Small Intestinal Bacterial Overgrowth (SIBO) (4). Eine retrospektive Studie liefert außerdem Hinweise auf eine Wirksamkeit bei antibiotika-assoziiertem Durchfall (5). Weitere Informationen und Evidenz zu diesem Building Block finden Sie in der Beschreibung dieses Inhaltsstoffs in unserem System.
Wichtige Mechanismen bei chronischen Erkrankungen
In der letzten „Wissensblitz“-Ausgabe wurde erwähnt, dass fast 10 Millionen Niederländer*innen an einer oder mehreren chronischen Erkrankungen leiden. Zwei zentrale Mechanismen bei chronischen Leiden sind Insulinresistenz und systemische niedriggradige Entzündungen.
Diese Mechanismen sind besonders bekannt im Zusammenhang mit dem metabolischen Syndrom und Typ-2-Diabetes, aber sie spielen bei nahezu allen chronischen Erkrankungen eine Rolle. Einige (vielleicht unerwartete) Beispiele dafür sind Depressionen (6–8), Rheuma (9,10) und ME/CFS (11,12).
Sowohl Insulinresistenz als auch niedriggradige Entzündungen stehen in direktem Zusammenhang mit dem Mikrobiom (13–16). Daher kann geschlossen werden, dass es sinnvoll ist, diese beiden zentralen Mechanismen und die Rolle des Mikrobioms in jedem therapeutischen Ansatz bei chronischen Erkrankungen zu berücksichtigen.
References:
https://doi.org/10.12998/wjcc.v6.i15.961
https://doi.org/10.1111/nmo.12544
http://www.kjg.or.kr/journal/view.html?uid=3648&vmd=Full
https://doi.org/10.3748/wjg.v25.i17.2110
https://doi.org/10.1097/MD.0000000000020631
https://doi.org/10.1016/j.expneurol.2019.01.016
https://doi.org/10.3389/fpsyt.2019.00057
https://doi.org/10.1017/S0033291719001454
https://doi.org/10.1002/art.38986
https://doi.org/10.1038/nrrheum.2016.136
https://doi.org/10.1073/pnas.1607571113
https://doi.org/10.3389/fnbeh.2018.00078
https://doi.org/10.1016/j.ar2017.10.003
https://doi.org/10.1177/0884533615609896
https://doi.org/10.1016/j.cmet.2017.09.008
https://doi.org/10.4049/jimmunol.1601621
16: Bauchbeschwerden, gesundes Altern
Bauchbeschwerden bei chronischen Erkrankungen
Die Mehrheit der niederländischen Bevölkerung – fast 10 Millionen Menschen – leidet an einer oder mehreren chronischen Erkrankungen (1). Über 3,7 Millionen Niederländer*innen sind mit einer Magen-Darm-Erkrankung (MDL) beim Hausarzt bekannt, und der Großteil davon (2,5 Millionen) betrifft Beschwerden wie Bauchschmerzen oder Verstopfung (2).
In vielen Fällen gehen chronische Erkrankungen mit Bauchbeschwerden einher – dies kann ein Hinweis darauf sein, dass das Mikrobiom eine Rolle spielt. So treten Symptome wie Verstopfung, Reflux oder Durchfall häufiger bei Menschen mit Kopfschmerzen auf (3), haben Migränepatientinnen überdurchschnittlich oft Reizdarmsyndrom (IBS) (4), und etwa die Hälfte aller Diabetespatientinnen klagt über Bauchbeschwerden (5,6).
Viele Patient*innen zögern, über Verdauungsbeschwerden zu sprechen oder empfinden Symptome wie Bauchschmerzen, Durchfall oder Verstopfung durch jahrelange Gewöhnung als „normal“. Es lohnt sich, gezielt nach Bauchbeschwerden zu fragen – dies kann schnell Aufschluss darüber geben, ob das Mikrobiom möglicherweise eine Rolle spielt, und eine Richtung für die Behandlung chronischer Beschwerden weisen. Fragen zu Bauchbeschwerden lassen sich in jedes ärztliche Gespräch integrieren. Einfache Hilfsmittel wie die Bristol-Stuhlformen-Tabelle und eine Checkliste mit Fragen stellt das Microbiome Center (MC) zur Verfügung.
Am 23. Februar organisierte das Microbiome Center ein gut besuchtes Webinar zu diesem Thema. Aufgrund der hohen Teilnehmerzahl und des positiven Feedbacks wird das Webinar am 22. April (19:30–21:00 Uhr) wiederholt. Anmelden können Sie sich per E-Mail an: office@microbiome-center.nl
Gesundes Altern und das Mikrobiom
Eine kürzlich veröffentlichte Studie zeigt, dass ein individuelleres (einzigartigeres) Mikrobiom mit besserer Gesundheit im Alter korreliert (7). Verschiedene Kohortenstudien zeigten, dass die Einzigartigkeit des Mikrobioms mit zunehmendem Alter steigt.
Bemerkenswert war, dass das Maß an Einzigartigkeit auch mit bestimmten Metaboliten korrelierte, die in früheren Studien mit einem sehr hohen Alter assoziiert wurden. Darüber hinaus bestand eine direkte Korrelation zwischen der Einzigartigkeit des Mikrobioms und verschiedenen Gesundheitsindikatoren bei älteren Menschen (z. B. Medikamentengebrauch, subjektives Gesundheitsempfinden, Lebensraumgröße, Gehgeschwindigkeit).
Insgesamt liefert diese Studie starke Hinweise darauf, dass das Mikrobiom eine entscheidende Rolle für gesundes Altern spielt.
References:
https://www.volksgezondheidenzorg.info/onderwerp/chronische-voorwaarden-en-multimorbiditeit/ Figures-context/current-situation
https://www.volksgezondheidenzorg.info/onderwerp/maag-intestine-en-livervoorwaarden/prevalence#node-nummer-persons-met-mdl-aandoening-known-bij-huisarts
https://doi.org/10.1111/j.1468-2982.2007.01486.x
https://doi.org/10.5056/jnm.2013.19.3.301
https://doi.org/10.1046/j.1464-5491.1999.00135.x
https://doi.org/10.1080/003655200750024317
https://doi.org/10.1038/s42255-021-00348-0 (available as a preprint at https://doi.org/10.1101/2020.02.26.966747)
15: Neue Zutat, Psoriasis
Neue Zutat
Auf Wunsch mehrerer Kolleginnen und Kollegen haben wir 2′-Fucosyllactose (2’FL) zur Liste der auswählbaren Zutaten hinzugefügt. 2’FL ist ein sogenanntes „Human Milk Oligosaccharide“ und kommt natürlicherweise in Muttermilch vor. Solche Oligosaccharide aus der Muttermilch tragen zur Entwicklung des Mikrobioms und zur Modulation des Immunsystems bei. Es wird angenommen, dass diese Effekte auch bei Erwachsenen auftreten, und 2′-Fucosyllactose wurde bei Erwachsenen als sicher eingestuft (1). Ein interessanter Aspekt dieser Substanz ist, dass präklinische Hinweise zeigen, dass Akkermansia muciniphila auf 2’FL wachsen kann (2–4), was darauf hindeutet, dass 2’FL eine der wenigen Substanzen ist, die diese wichtige Bakterienart stimulieren können. Akkermansia muciniphila ist ein gesundheitsfördernder Bakterienstamm, der Mucin abbaut, dadurch eine gesunde Darmwand unterstützt und bei Krankheiten oft stark vermindert ist (5,6). Es ist daher nicht überraschend, dass präklinische Studien zeigen, dass 2’FL die Barrierefunktion des Darms verbessert (7,8). Darüber hinaus gibt es einige Hinweise aus Humanstudien auf eine entzündungshemmende Wirkung (9), auf Allergien (10) und Atemwegsinfektionen (11). Weitere Nachweise und Informationen finden Sie in der Beschreibung dieser Zutat in unserem System.
Rolle des Darmmikrobioms bei Psoriasis
Obwohl Psoriasis als Hautkrankheit bekannt ist, gibt es mehrere Hinweise darauf, dass das Darmmikrobiom eine Rolle spielt (12,13). Dies hängt vermutlich mit der gestörten Immunregulation und der niedriggradigen systemischen Entzündung bei Psoriasis zusammen (14,15). Viele der bei Psoriasis beobachteten Komorbiditäten – wie Typ-2-Diabetes, nicht-alkoholische Fettleber, Depression, Herz-Kreislauf-Erkrankungen und Morbus Crohn (14,15) – stehen im Zusammenhang mit den Kernfaktoren des metabolischen Syndroms: systemische niedriggradige Entzündung und Insulinresistenz. Auch Insulinresistenz wurde bei Psoriasis festgestellt (16,17). Es ist bekannt, dass das Darmmikrobiom eine wichtige Rolle bei diesen zugrundeliegenden Mechanismen spielt, unter anderem durch seinen Einfluss auf die Darmpermeabilität. Dies passt zur Beobachtung, dass die Barrierefunktion des Darms bei Psoriasis vermindert ist (18). All dies deutet darauf hin, dass eine Mikrobiomtherapie – wie etwa Probiotika – bei Psoriasis hilfreich sein kann. Pilotstudien zeigen tatsächlich günstige Effekte auf Entzündungsmarker und die Schwere der Symptome bei Psoriasispatienten (19,20).
References:
https://doi.org/10.1017/S0007114516003354
https://doi.org/10.3920/BM2016.0185
https://doi.org/10.3390/nu12051284
https://doi.org/10.1038/s41598-020-71113-8
https://doi.org/10.26355/eurrev_201909_19024
https://doi.org/10.1016/j.micpath.2016.02.005
https://doi.org/10.3389/fcimb.2018.00372
https://doi.org/10.3390/nu12092808
https://doi.org/10.3945/jn.116.236919
https://doi.org/10.1007/s00394-016-1180-6
https://doi.org/10.1097/MPG.0000000000001520
https://doi.org/10.1016/j.berh.2020.101494
https://doi.org/10.3390/pathogens9060463
https://doi.org/10.1016/S0140-6736(14)61909-7
https//doi.org/10.3390/ijms20061475
https//doi.org/10.3390/ijerph15071486
https//doi.org/10.1016/j.jaad.2015.01.004
https//doi.org/10.3390/microorganisms7110550
https//doi.org/10.4161/gmic.25487
https//doi.org/10.2340/00015555-3305
14: Neue Stämme, Multiple Sklerose (MS)
Zwei neue Stämme
Das Microbiome Center sucht weltweit kontinuierlich nach interessanten neuen Substanzen und Bakterienstämmen, die Sie in der Mikrobiomtherapie einsetzen können. Wir haben zwei neue, sporenbildende probiotische Stämme zu unserem Angebot hinzugefügt.
Der erste ist ein Bacillus clausii, der aufgrund seiner Sporenbildung sehr stabil ist und eine ausgezeichnete Magen-Darm-Passage übersteht (1). Dieser Stamm wurde klinisch bei Durchfall untersucht (2,3). Es gibt zudem erste Hinweise auf eine mögliche Wirkung bei Urämie (4) sowie auf eine hemmende Wirkung gegenüber dem pathogenen Bakterium Bacillus cereus (5).
Der zweite Stamm ist ein Bacillus coagulans. Dieser zeigte in einer gut durchgeführten randomisierten kontrollierten Studie eine deutliche Wirkung bei Verstopfung (6). Zudem gibt es mehrere klinische Studien, die einen positiven Effekt bei Reizdarmsyndrom (IBS) nahelegen (7–9). Für das damit häufig verbundene Symptom Bauchschmerzen gibt es ebenfalls Hinweise auf eine positive Wirkung, wenngleich die Datenlage weniger einheitlich ist (7–12). Darüber hinaus gibt es einige Hinweise aus klinischen Studien auf eine Wirksamkeit bei u.a. SIBO (13) und bakterieller Vaginose (bei oraler Anwendung) (14).
Weitere Informationen zu diesen und allen anderen Inhaltsstoffen finden Sie im MC-Behandlungsnetzwerk unter dem (i)-Symbol bei den Zutaten.
Weitere Hinweise auf die Rolle des Mikrobioms bei Multipler Sklerose
Es gab bereits verschiedene Hinweise darauf, dass das Darmmikrobiom bei der Entstehung der Multiplen Sklerose (MS) eine Rolle spielt, etwa durch bakterielle Substanzen im Blut und das Vorhandensein von Bakterien im Gehirn verstorbener Patienten (15). Eine kürzlich veröffentlichte Studie liefert nun einen weiteren Hinweis: Bei MS-Patienten wurde Immunglobulin A (IgA) in der Liquorflüssigkeit nachgewiesen (16). Außerdem fand man B-Zellen mit IgA-Expression im Gehirn verstorbener Patienten, vor allem in Bereichen mit Läsionen. Auffällig war, dass die IgA-exprimierenden B-Zellen in der Liquorflüssigkeit zwar auf Darmbakterien, nicht jedoch auf Antigene des Gehirns reagieren. Dies deutet darauf hin, dass diese B-Zellen aus dem Darm stammen und in die Liquorflüssigkeit migriert sind.
Diese Studie legt nahe, dass in der aktiven Phase der MS B-Zellen, die auf Darmbakterien reagieren, in die Liquorflüssigkeit und das Gehirn einwandern und dort aktiv sind. Es erscheint plausibel, dass die Darmbarriere hier eine zentrale Rolle spielt. Immunmodulierende probiotische Stämme könnten möglicherweise Einfluss auf diesen Prozess nehmen, und erste Tier- und Humanstudien mit Probiotika zeigen erste vorsichtig positive Effekte (17).
References:
https://doi.org/10.3389/fmicb.2020.01010
https://doi.org/10.3920/BM2018.0094
https://doi.org/10.3920/BM2012.0034
https://doi.org/10.1007/s12602-019-09540-x
https://doi.org/10.4014/mbl.1903.03005
https://doi.org/10.1007/s12602-019-09542-9
https://doi.org/10.3920/BM2017.0129
https://doi.org/10.1038/s41598-019-48554-x
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4129566/
https://doi.org/10.5812/ircmj.17(4)2015.23844
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4285933/
https://www.researchgate.net/publication/282188545_Efficacy_of_Bacillus_coagulans_strain_unique_IS-2_in_the_treatment_of_patients_with_acute_diarrhea
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4311312/
https://doi.org/10.1007/s12088-011-0233-z
https://microbiome-center.nl/Medici/MS-Parkinson-Alzheimer/
https://doi.org/10.1126/sciimmunol.abc7191
https://doi.org/10.1186/s12974-019-1611-4
13: Kostenerstattung durch Krankenkassen
in dem Monat, in dem die meisten Niederländer ihre Krankenversicherung noch einmal überprüfen, möchten wir Ihnen gerne Informationen zur Kostenerstattung durch die Krankenkassen für Mikrobiomtherapie geben.
Nachfolgend finden Sie einen allgemeinen Überblick über die Erstattungsregelungen der Krankenkassen für das Jahr 2021. Die Hauptlinie lässt sich wie folgt zusammenfassen:
- Die größeren Krankenkassen bieten ein oder mehrere Zusatzversicherungen an, die Raum für die Erstattung „alternativer Heilmethoden“ lassen.
- Der jährlich verfügbare Erstattungsbetrag steigt mit dem Umfang und Preis der Zusatzversicherung.
- Häufig wird die Behandlung durch eine approbierte Ärztin oder einen approbierten Arzt als Voraussetzung genannt.
- Medikamente sind in der Regel ausgeschlossen.
Das bedeutet, dass Klienten – sofern sie die passende Zusatzversicherung abgeschlossen haben und ihr Erstattungslimit noch nicht ausgeschöpft ist – in der Regel mit einer Erstattung der Kosten für Beratung und Stuhlanalyse rechnen können (ausgenommen ONVZ), jedoch nicht für Medikamente. Hier ein Überblick nach Krankenkasse:
CZ mit „Aanvullend 5“: 250 € pro Jahr für alternative und/oder psychosoziale Behandlungen (25 € pro Tag) und Medikamente (100 %) zusammen
Zilveren Kruis mit „Aanvullend 2 Sterne“ oder höher: maximal 40 € pro Tag bis zu 250 € pro Kalenderjahr für alternative Behandlungen wie orthomolekulare Therapie
Menzis mit „Extra Verzorgd 2“ oder höher: maximal 400 € pro Kalenderjahr (40 € pro Tag für Behandlungen, 100 % für Medikamente) für alternative Versorgung
VGZ mit „Aanvullend Goed“ oder höher: alternative Versorgung: 200 € pro Jahr, maximal 40 € pro Tag
DSW mit „AV Compact“ oder höher: Erstattung für ärztliche Konsultationen in der Naturheilkunde, maximal 25 € pro Behandlungstag, maximal 250 € pro Kalenderjahr
Zorg en Zekerheid mit „AV-Sure“ oder höher: Erstattung für Behandlungen durch naturheilkundliche oder orthomolekulare Ärzte, maximal 250 € pro Kalenderjahr, bestehend aus max. 25 € pro Tag für Behandlungen oder 50 % Erstattung für Medikamente
ASR mit „Start“ oder höher: Erstattung für Behandlungen durch einen Arzt, max. 100 € pro Kalenderjahr (höhere Zusatzversicherung = höherer Gesamtbetrag)
ONVZ mit „Startfit“ oder höher: Erstattung für alternative Heilmethoden durch einen Arzt, d.h. Konsultationen und Behandlungen im Zusammenhang mit der Heilung einer Erkrankung. Keine Laborkosten. Höhere Zusatzversicherungen = auch Erstattung für registrierte Medikamente und höherer Gesamtbetrag
Ditzo, Anderzorg, Hema, Interpolis und Just erstatten keine alternativen Heilmethoden.
Hinweis: Diese Übersicht vermittelt einen allgemeinen Eindruck; es können keine Rechte daraus abgeleitet werden.
12: Stämme und Inhaltsstoffe
Welche Stämme können Sie anwenden?
Manchmal erhalten wir die Frage, welche Inhaltsstoffe aus unserem Portfolio Ihnen für individuelle Zubereitungen zur Verfügung stehen. Daher hier ein kurzer Überblick über eine Auswahl verfügbarer Inhaltsstoffe:
- Das Portfolio enthält beispielsweise einen Clostridium butyricum-Stamm, der Buttersäure produziert, antiinflammatorische Eigenschaften besitzt und unter anderem wirksam bei Colitis ulcerosa ist.
- Auch können Sie den bekannten Hefestamm Saccharomyces boulardii verwenden, der gegen pathogene Keime und Parasiten wirkt und daher unter anderem bei Durchfall nützlich ist.
- Ein weiterer Stamm ist Propionibacterium freudenreichii, der unter anderem Vitamin K2 produziert.
- Es stehen spezifische Stämme von Bifidobacterium bifidum, B. breve und Lactobacillus acidophilus zur Verfügung, die gezielt aufgrund ihrer Wirkung auf die Reduzierung der Darmpermeabilität und ihrer antiinflammatorischen Effekte ausgewählt wurden – zudem können sie die Insulinresistenz verbessern.
- Einer der Inhaltsstoffe enthält die Aminosäure L-Glutamin, die die Darmbarrierefunktion stärkt und unter anderem zur Minderung von Nebenwirkungen einer Chemotherapie untersucht wurde.
- Auch der bekannte Stamm LGG (Lactobacillus rhamnosus GG) ist verfügbar – er ist wirksam bei Reizdarmsyndrom (IBS) und Durchfall, wurde aber auch in Studien zu Manie und ADHS untersucht.
Neben diesen und weiteren Inhaltsstoffen suchen wir weltweit kontinuierlich nach interessanten neuen Substanzen und Stämmen, die Sie in der Mikrobiomtherapie einsetzen können:
- Demnächst erweitern wir das Portfolio z. B. um einen Bacillus coagulans– und einen Bacillus clausii-Stamm, die unter anderem bei bakterieller Vaginose, IBS und SIBO untersucht wurden.
- Zudem arbeiten wir an der Aufnahme eines Bacillus subtilis– und Enterococcus faecium-Stamms, die gemeinsam in zahlreichen klinischen Studien bei Colitis ulcerosa, aber auch bei beatmungsassoziierter Pneumonie erforscht wurden.
Weitere Informationen zu den verfügbaren Inhaltsstoffen und Literaturverweise finden Sie im MC-Behandlungsnetzwerk unter dem (i)-Symbol bei den Zutaten.
11: Diabetes
Forschung zum Mikrobiom bei Typ-1-Diabetes
Es ist kaum jemandem entgangen, dass Professor Max Nieuwdorp vom Amsterdam UMC über eine Million Euro Fördermittel von der Diabetes-Stiftung für Mikrobiomforschung bei Patientinnen und Patienten mit Typ-1-Diabetes (T1DM) erhalten hat (1). Frühere Studien haben bereits gezeigt, dass sich das Mikrobiom von T1DM-Patienten von dem gesunder Personen unterscheidet – unter anderem durch eine geringere Anzahl butyratbildender Bakterien (2,3). Darüber hinaus gibt es vorsichtige Hinweise darauf, dass die Einnahme von Probiotika mit einem geringeren Risiko für T1DM sowie einer besseren glykämischen Kontrolle bei Betroffenen assoziiert sein könnte (4,5). Auch das Amsterdam UMC hat bereits eine explorative Studie zur Stuhltransplantation bei T1DM-Patienten durchgeführt und wird die Ergebnisse diesen Monat im Fachjournal Gut veröffentlichen (1). Die Vergabe dieser Förderung ist eine klare Bestätigung dafür, dass die wachsenden Erkenntnisse über den Zusammenhang zwischen chronischen Krankheiten und Darmgesundheit wertvoll für Patienten und Behandler sind.
Mikrobiom bei Insulinresistenz und Typ-2-Diabetes
Es gibt zahlreiche überzeugende Hinweise darauf, dass das Mikrobiom bei Insulinresistenz und Typ-2-Diabetes mellitus (T2DM) eine Rolle spielt (6,7). Auffällig ist zum Beispiel, dass Metformin – das Mittel der ersten Wahl bei T2DM – nur bei oraler Einnahme wirkt (8). Metformin scheint (auch) über den Darm zu wirken und ist mit einer Zunahme der mucinverwertenden Akkermansia muciniphila sowie butyratbildender Bakterienarten assoziiert (9–11). Typ-2-Diabetes und Insulinresistenz gehen mit einer systemischen niedriggradigen Entzündung einher (12). Es gibt Hinweise darauf, dass das Stoffwechsel- und Immunsystem eng miteinander verwoben sind – vermutlich, weil eine starke Immunabwehr evolutionär vorteilhaft, aber sehr energieaufwendig ist (13). So gibt es beispielsweise Evidenz dafür, dass Zytokine direkt als metabolische Hormone wirken (13). Angesichts der Effekte, die probiotische Stämme auf das Immunsystem, die Darmpermeabilität und die Butyratproduktion haben können, ist es wenig überraschend, dass Metaanalysen von RCTs zu dem Schluss kommen, dass Probiotika unter anderem HbA1c und HOMA-IR senken können (14,15).
References
https://www.diabetesfonds.nl/over-diabetes/nieuws/miljoen-euro-voor-onderzoek-poep transplant-bij-diabetes-type-1
https://doi.org/10.1155/2020/3936247
https://doi.org/10.3389/fendo.2020.00125
https://doi.org/10.1001/jamapediatrics.2015.2757
https://doi.org/4172/2329-8901.1000188
https://doi.org/10.1210/er.2017-00192
https://doi.org/10.1172/JCI129194
https://doi.org/10.1111/j.1464-5491.1992.tb01716.x
https://doi.org/10.1007/s00125-015-3844-9
https://doi.org/10.1038/nature15766
https://doi.org/10.2337/dc16-1324
http://www.njmonline.nl/njm/getarticle.php?v=71&i=4&p=174
https://doi.org/10.1038/nature21363
https://doi.org/10.20452/pamw.3156
https://doi.org/10.1186/s12967-020-02213-2
10: Covid-19, Alzheimer
Interaktion zwischen Bakterien und SARS-CoV-2
Aus verschiedenen Studien sowie aus Daten des niederländischen RIVM ist bekannt, dass Adipositas, Diabetes und Herz-Kreislauf-Erkrankungen das Risiko für einen schweren Verlauf von Covid-19 erhöhen (1,2). Vor einigen Wochen wurde eine aufschlussreiche Übersichtsarbeit veröffentlicht (3), die auf eine synergistische Wirkung zwischen dem neuen Coronavirus und Lipopolysaccharid (LPS, ein bakterielles Endotoxin) hinweist. Beide senken die Expression des ACE2-Rezeptors in der Lunge, wodurch das Renin-Angiotensin-System gestört wird. Aus Studien mit einem Schweine-Coronavirus ist bekannt, dass die Kombination dieses Virus mit LPS bei Schweinen zu einem schweren akuten Atemnotsyndrom (SARS) führt, während die Exposition gegenüber einem der beiden Erreger allein deutlich mildere Symptome verursacht.
Bei Diabetes und anderen Erkrankungen wird zudem eine erhöhte Darmpermeabilität beobachtet (4), was zu erhöhtem LPS im Blutkreislauf und damit verbundener Insulinresistenz führt (5). Die genannte Übersichtsarbeit (3) liefert somit neue Hinweise darauf, dass eine Stärkung der Darmbarriere ein sinnvoller therapeutischer Ansatz sein könnte, um Patienten mit kardiometabolischen Erkrankungen vor schweren Verläufen zu schützen.
Mykobiom bei Alzheimer
Frühere Studien haben bereits gezeigt, dass es Unterschiede in der Zusammensetzung des Mikrobioms zwischen Alzheimer-Patienten und gesunden Personen gibt (6,7). Diese Untersuchungen konzentrierten sich ausschließlich auf Bakterien, doch das menschliche Mikrobiom umfasst auch viele andere Mikroorganismen wie Pilze, Archaeen, Protisten und Viren.
Eine neue Publikation kommt zu dem Schluss, dass bei Menschen mit leichter kognitiver Beeinträchtigung auch Unterschiede im Pilzspektrum (Mykobiom) vorliegen (8). Zudem verglichen die Forschenden den Einfluss zweier Ernährungsformen miteinander. Nur eine modifizierte mediterran-ketogene Diät zeigte eine Wirkung auf das Mykobiom bei Patienten mit leichter kognitiver Beeinträchtigung. Dies stimmt mit früheren Studien überein, die zeigten, dass diese Diät Marker der Alzheimer-Erkrankung verbessern kann.
Eine weitere aktuelle Studie mit einem Alzheimer-Tiermodell belegt überzeugend, dass eine Stuhltransplantation von gesunden auf erkrankte Mäuse zu einer Reduktion von Amyloid-β-Plaques, niedrigeren Entzündungswerten und weniger kognitivem Abbau führt (9). Diese beiden Studien ergänzen die wachsende Evidenzbasis dafür, dass der Krankheitsverlauf von Alzheimer über den Darm beeinflusst werden kann.
References
https://doi.org/10.1016/j.dsx.2020.04.044
https://www.rivm.nl/documents/weekly-update-epidemiologische-gedrag-covid-19-in-nederland
https://doi.org/10.7554/eLife.61330
https://doi.org/10.1186/1475-2891-13-60
https://doi.org/10.2337/db06-1491
https://doi.org/10.1038/s41598-017-13601-y
https://doi.org/10.1038/s41598-018-38218-7
https://doi.org/10.1016/j.ebiom.2020.102950
https://doi.org/10.1136/gutjnl-2018-317431
9: Migräne, LGG, Namensänderung Lactobacillus
Probiotika bei Migräne
Es gibt mehrere Hinweise auf einen Zusammenhang zwischen dem Darmmikrobiom und Migräne (1). Eine aktuelle systematische Übersichtsarbeit zu placebokontrollierten Studien identifizierte zwei geeignete Studien, von denen eine einen deutlichen positiven Effekt und die andere keinen Effekt von Probiotika zeigte (2). Auch aus der Praxis ist bekannt, dass manche Migränepatienten deutlich von Probiotika profitieren. Einige berichten, dass ihre Migräneattacken nahezu verschwunden sind, nachdem sie mit der Einnahme von Probiotika begonnen haben – selbst wenn sie zuvor schon viele andere Therapien ausprobiert hatten. Ein schönes Beispiel für eine Studie, die solche Beobachtungen beschreibt, ist diese mit über 1000 Patient:innen, bei der die Symptomschwere signifikant reduziert wurde (3).
Neuer Stamm: LGG
Das Probiotika-Portfolio, das Sie verschreiben können, wurde um einen neuen Stamm erweitert: Lacticaseibacillus rhamnosus GG, der weltweit am besten untersuchte probiotische Bakterienstamm. Falls Sie sich fragen, ob ein Schreibfehler im Gattungsnamen vorliegt, lesen Sie bitte den letzten Abschnitt dieser Wissensmitteilung.
Dass dieser Stamm – auch bekannt als LGG – in über 1100 Veröffentlichungen auf PubMed untersucht wurde, bedeutet nicht, dass er für alle Indikationen wirksam ist. So wurde LGG beispielsweise häufig bei Ekzemen untersucht, jedoch zeigt eine Metaanalyse randomisierter kontrollierter Studien (RCTs), dass LGG hier nicht wirksam ist (4). Wir haben LGG dennoch ins Portfolio aufgenommen, weil er sich bei mehreren anderen Indikationen als wirksam erwiesen hat. In unserem GRADE-basierten Bewertungssystem erreicht LGG sogar die höchstmögliche Punktzahl für akuten Durchfall, gestützt durch zwei Metaanalysen von RCTs mit sehr konsistenten Ergebnissen (5,6). Auch bei Reizdarmsyndrom (IBS) gibt es starke Evidenz für seine Wirksamkeit (7,8).
Interessant ist auch, dass LGG bei ADHS und Manie untersucht wurde – auch wenn es sich hierbei bislang nur um erste, vorsichtige Hinweise handelt (9,10). Weitere potenzielle Anwendungsgebiete finden Sie auf unserer Website.
Namensänderung der Gattung Lactobacillus
Ein internationales Expertenteam hat vor einigen Monaten eine umfassende taxonomische Umstrukturierung der Bakteriengattung Lactobacillus vorgenommen (11). Diese Gattung umfasste bekannte Arten wie L. acidophilus, L. rhamnosus und L. brevis.
Genetische Analysen hatten schon länger gezeigt, dass die alte Lactobacillus-Gruppe zu heterogen war, um sinnvoll alle 261 Arten in einer einzigen Gattung zu belassen. In der neuen Klassifikation wurden 23 neue Gattungen eingeführt – alle beginnen mit dem Buchstaben „L“, sodass Abkürzungen weitgehend gleich bleiben. Auf verschiedenen Webseiten können Sie Tabellen mit alten und neuen Namen einsehen (12).
References
https://doi.org/10.1186/s10194-020-1078-9
https://doi.org/10.3390/jcm8091441
https://doi.org/10.1007/s15006-018-1052-5
https://doi.org/10.3390/nu10091319
https://doi.org/10.3748/wjg.v25.i33.4999
https://doi.org/10.1111/apt.15267
https://doi.org/10.1111/j.1365-2036.2011.04665.x
https://doi.org/10.1097/MCG.0000000000001054
https://doi.org/10.1038/pr.2015.51
https://doi.org/10.1111/bdi.12652
https://doi.org/10.1099/ijsem.0.004107
https://www.microbiometimes.com/the-lactobacillus-taxonomy-change-has-arrived-what-do-you-need-to-know/
8: Rollen des Mikrobioms bei Virusinfektionen und Erholung danach
Das Mikrobiom: vielfältige Rollen bei Virusinfektionen
Virusinfektionen werden auf unterschiedliche Weise vom Mikrobiom beeinflusst – mit sowohl fördernden als auch hemmenden Effekten (1). Viren können direkt von bestimmten bakteriellen Faktoren profitieren, um ihre Stabilität, Infektiosität und Virulenz zu steigern. Auch indirekt können Bakterien Viren unterstützen, indem sie die Expression regulatorischer T-Zellen fördern und dadurch die Immunabwehr dämpfen.
Andererseits kann das Mikrobiom Virusinfektionen auch entgegenwirken. Dies geschieht direkt durch Bindung, Absorption, Destabilisierung und verminderte Replikation von Viren oder indirekt durch die Stärkung der Immunantwort. Diese gegensätzlichen Effekte verdeutlichen die Komplexität der Interaktionen zwischen Wirt und Mikrobiom und die Bedeutung eines ausgewogenen Gleichgewichts.
Eine starke Immunantwort ist bei Virusinfektionen wünschenswert – doch sobald die Infektion überwunden ist, sollte die Immunreaktion gezielt heruntergefahren werden. Bei nicht übertragbaren Krankheiten ist eine Förderung entzündungshemmender regulatorischer T-Zellen wiederum besonders wünschenswert (2,3).
Erholung nach Virusinfektionen
Das Mikrobiom beeinflusst nicht nur den Verlauf von Virusinfektionen – umgekehrt wirken sich auch Virusinfektionen auf das Mikrobiom aus (1,4). Bei verschiedenen Viren, darunter Influenza- und Noroviren, wurden Veränderungen des Darmmikrobioms beobachtet. Diese Veränderungen stehen im Zusammenhang mit der Immunmodulation durch das Virus selbst, aber auch mit veränderter Nahrungsaufnahme während der Krankheitsphase (5).
Störungen des Darmmikrobioms nach einer Virusinfektion sind also nicht überraschend, können jedoch in manchen Fällen schwerwiegend und/oder chronisch sein. Bei infektiöser Gastroenteritis – auch wenn sie viraler Natur ist – kann z. B. das sogenannte postinfektiöse Reizdarmsyndrom (PI-IBS) entstehen (6,7). Dabei spielen gestörte Immunaktivität (einschließlich hoher Spiegel proinflammatorischer Zytokine), eine beeinträchtigte Darmbarriere und ein verändertes Mikrobiom eine Rolle.
Auch Infektionen, die außerhalb des Darms wirken – wie z. B. bakterielle Q-Fieber-Erkrankungen – können postinfektiöse Beschwerden wie Müdigkeit verursachen, wobei ebenfalls eine erhöhte proinflammatorische Zytokinaktivität eine Rolle spielt (8). Ähnliches gilt für Virusinfektionen wie das Epstein-Barr-Virus (9). Umgekehrt scheint das chronische Erschöpfungssyndrom (ME/CFS) oft eine virale Ursache zu haben und ist ebenfalls mit einer gestörten Immunregulation und einem veränderten Mikrobiom verbunden (10,11).
Virusinfektionen können also langfristige Auswirkungen haben – und die immunmodulierende Rolle der Darmbakterien scheint hierbei eine bedeutende Rolle zu spielen. Anders als bei akuten Virusinfektionen, aber vergleichbar mit nicht übertragbaren Erkrankungen, ist in der Erholungsphase eine Dämpfung der entzündlichen Immunaktivität eindeutig wünschenswert.
References
https://doi.org/10.3389/fimmu.2019.01551
https://doir.org/10.1136/bmj.j5145
https://doi.org/10.1016/j.jaci.2014.11.012
https://doi.org/10.1016/j.micinf.2017.09.002
https://doi.org/10.1128/mBio.03236-19
https://doi.org/10.1007/s11894-017-0595-4
https://doi.org/10.1097/MCG.0000000000000924
https://doi.org/10.1371/journal.pone.0155884
https://doi.org/10.1016/j.neucli.2017.02.002
https://doi.org/10.1007/s11011-019-0388-6
7: Immunsystem
Immune system
Das Darmmikrobiom spielt eine wichtige Rolle bei der Ausbildung und Funktion des Immunsystems sowie der erworbenen Immunität (1,2,3). Sowohl Antibiotika als auch Probiotika beeinflussen die Wirksamkeit von Impfungen (4,5), und sowohl das Mikrobiom als auch bestimmte Probiotika wirken sich auf den Verlauf von Virusinfektionen aus (6,7). Auffällig ist, dass bei Covid-19-Patienten fast jeder Fünfte an Durchfall, Erbrechen oder Bauchschmerzen litt (8) und dass das SARS-CoV-2-Virus im Stuhl und im niederländischen Abwasser nachgewiesen wurde (9,10,11).
Darüber hinaus wird der Verlust des Geruchssinns als Symptom von Covid-19 genannt (12). Interessanterweise wird dies mit dem Eindringen des Virus in das zentrale Nervensystem in Verbindung gebracht, wo es möglicherweise über das Atemzentrum auch bei Atemproblemen eine Rolle spielt (13,14).
Die Darm-Blut-Schranke und die Blut-Hirn-Schranke werden von denselben Faktoren beeinflusst – und das Mikrobiom spielt dabei eine Rolle (15,16). Auch wenn das Mikrobiom auf den ersten Blick nichts mit Covid-19 zu tun zu haben scheint, kann es durchaus eine wichtige Rolle spielen. Besonders immunologisch aktive Bakterien und die Funktion der Darmbarriere verdienen dabei besondere Aufmerksamkeit.
References
https://doi.org/10.1126/science.1223490
https://doi.org/10.1038/nm.2505
https://doi.org/10.1038/ni.3780
https://doi.org/10.1016/j.cell.2019.08.010
https://doi.org/10.3390/nu9111175
https://doi.org/10.3389/fcimb.2016.00041
https://doi.org/10.3389/fimmu.2016.00633
https://journals.lww.com/ajg/Documents/COVID_Digestive_Symptoms_AJG_Preproof.pdf
https://doi.org/10.1016/j.ijid.2020.02.050
https://doi.org/10.1001/jama.2020.3786
https://www.rivm.nl/nieuws/nieuwe-coronavirus-aangetreffen-in-rioolwater
https://www.entuk.org/loss-sense-smell-marker-covid-19-infection
https://doi.org/10.1021/acschemneuro.0c00122
https://doi.org/10.1002/jmv.25728
https://doi.org/10.1016/j.bbrc.2018.11.021
https://doi.org/10.1152/ajpgi.00048.2015
6: Darm-Hirn-Achse
Mikrobiom kann das Nervensystem direkt (!) beeinflussen
Dass es eine Verbindung zwischen Darm und Gehirn gibt, ist nicht neu (1). Seit 2014 sind bereits fast 2000 Publikationen zu diesem Thema erschienen. Im Februar 2020 veröffentlichte Nature eine Studie, die eine direkte Verbindung zwischen dem Mikrobiom und dem Nervensystem im Darm nachwies (2,3). Die Forschenden identifizierten einen Rezeptor, der ein integraler Bestandteil des enterischen Nervensystems ist, und zeigten, dass Mikroorganismen im Darm diesen Rezeptor direkt aktivieren können (3). Dies beeinflusst Funktionen des lokalen neuronalen Netzwerks, wie z. B. die Peristaltik, bietet jedoch durch die Verbindung über den Nervus vagus auch eine direkte Verbindung zwischen Mikrobiom und Gehirn.
Rolle des Mikrobioms bei Autismus
Es gibt starke Hinweise darauf, dass Autismus-Spektrum-Störungen mit der Darmgesundheit in Zusammenhang stehen. Autistische Kinder leiden häufig unter Magen-Darm-Beschwerden wie chronischem Durchfall oder Verstopfung (4,5) und gehören zu den am häufigsten an Gastroenterologen überwiesenen Patientengruppen (5). Bei autistischen Personen wurden Hinweise auf eine erhöhte Durchlässigkeit der Darmwand gefunden (6), ebenso wie erhöhte Werte eines bakteriellen Endotoxins (LPS) im Blut (7).
Eine kleine Studie mit Stuhltransplantationen bei autistischen Kindern führte nicht nur zu einer deutlichen Verbesserung der Darmbeschwerden, sondern auch zu signifikanten Verbesserungen der Verhaltenswerte (8). Dieser Effekt war auch zwei Jahre später noch nachweisbar (9). Auch neuere Pilotstudien mit Prä- und Probiotika zeigen vorsichtige Verbesserungen in den Verhaltensergebnissen (10,11).
References
https://doi.org/10.1152/physrev.00018.2018
https://www.nrc.nl/nieuws/2020/02/12/bacterien-communiceren-met-zenuwsysteem-in-de-darm-a3990193
https://doi.org/10.1038/s41586-020-1975-8
https://doi.org/10.1007/s10803-013-1973-x
https://doi.org/10.3748/wjg.v22.i46.10093
https://doi.org/10.3390/ijms20092115
https://doi.org/10.3748/wjg.v22.i1.361
https://doi.org/10.1186/s40168-016-0225-7
https://doi.org/10.1038/s41598-019-42183-0
https://doi.org/10.1186/s40168-018-0523-3
https://doi.org/10.3390/nu11040820
5: Allergien
Rolle von Probiotika bei Allergien
Über das Immunsystem besteht ein direkter Zusammenhang zwischen Allergien und dem Mikrobiom. Allergische Reaktionen sind IgE-vermittelt und immunologischer Natur [1], und es ist bekannt, dass das Mikrobiom eine wichtige Rolle bei der „Erziehung“ und der Grundregulation des Immunsystems spielt [2,3]. Der Zusammenhang mit dem Mikrobiom wird durch verschiedene Studien zu Asthma, atopischem Ekzem, Nahrungsmittelallergien und Heuschnupfen bestätigt [4,5].
Interventionen mit Prä- und Probiotika bei schwangeren Frauen und ihren Kindern zeigen sowohl präventive als auch therapeutische Effekte bei atopischem Ekzem [6,7] und Nahrungsmittelallergien [8,9]. Die Wirkungen sind stamm-spezifisch und lassen sich in die individuellen Mischungen von MiBlend übertragen.
Wahl zur „Lebensstil-Professionellen 2020“
Während des Kongresses der Vereinigung Arzt und Lebensstil am 3. April findet die Wahl zur „Lebensstil-Professionellen 2020“ statt. In diesem Jahr können neben Ärzten auch VERAHs, Apotheker, Lebensstilcoaches und Ernährungsberater nominiert werden. Wenn Sie jemanden im Sinn haben, können Sie sich bei der Vereinigung melden [10].
References
Akdis, C.A., Agache, I., 2014. Global atlas of allergy. European Academy of Allergy and Clinical Immunology
https://doi.org/10.1016/j.immuni.2017.04.008
https://doi.org/10.1111/imm.12896
https://doi.org/10.1016/j.jaci.2017.02.007
https://doi.org/10.1111/imr.12556
https://doi.org/10.1016/j.jaci.2015.04.031
https://doi.org/10.1001/jamapediatrics.2015.3943
https://doi.org/10.1097/MD.0000000000002562
https://doi.org/10.1016/j.aller.2019.04.009
https://www.artsenleefstijl.nl/activities/jaarcongres2020/
4: Depression
Beratungsunterstützung und Produktinformationen Update
Nach einigen technischen Herausforderungen sind nun alle Beschreibungen und Referenzen der Nahrungsergänzungsmittel und magistralen Zutaten vollständig ausgefüllt. Diese finden Sie, indem Sie auf das (i) neben einem Produkt oder einer Zutat in der Beratungsunterstützung oder auf der Rezept-Erstellungsseite klicken. Die Beschreibung bietet eine Zusammenfassung aller durchgeführten Studien mit dem betreffenden Produkt oder der Zutat, einschließlich der entsprechenden Referenzen.
Die Beratungsunterstützung wurde ebenfalls weiter verbessert. Bei den vorgeschlagenen Mengen der magistralen Zutaten wird jetzt auch die minimale und maximale Tagesdosis für jede Zutat berücksichtigt. Unverändert bleibt, dass das Ergebnis der Beratungsunterstützung auf den eingegebenen Werten für die verschiedenen Indikationen (Symptome, medizinische Vorgeschichte und Laborergebnisse) einerseits und der Stärke der Evidenz der Produkte/Zutaten bei diesen Indikationen andererseits basiert. In der neuen Version der Beratungsunterstützung wurde auch eine verfeinerte Abstufung der Evidenzstärke eingeführt, die systematisch (im GRADE-Stil [1]) gewichtet wurde. Derzeit arbeiten wir intensiv daran, in der nächsten Version der Beratungsunterstützung die Evidenzbewertungen für Sie sichtbar zu machen, sodass Sie noch besser nachvollziehen können, auf welchen Grundlagen die Empfehlungen basieren.
Probiotika möglicherweise hilfreich bei Depressionen
Seit einigen Jahren wird immer deutlicher, dass das Mikrobiom eine Rolle bei der Stimmung und Depression spielt; es wird von der Darm-Hirn-Achse gesprochen. Es gibt Zusammenhänge zwischen der Lebensqualität bzw. Depression und der Zusammensetzung, Struktur und Funktion des Mikrobioms [2,3]. Fäkaltransplantation von Patienten mit Major Depression Disorder (MDD) auf Mäuse oder Ratten führt zu Verhalten, das mit Depression in Verbindung gebracht wird [4,5]. Klinische Studien haben gezeigt, dass Interventionen mit Probiotika zu einer Reduzierung der Depression führen können [6-8].
Königliches Interesse am Mikrobiom
Am Dienstag, den 26. November, fand das Palastsymposium „The Microbiome“ statt, an dem König Willem-Alexander und Prinzessin Beatrix teilnahmen [9]. Die Redner waren Martin Blaser, Direktor des Human Microbiome Program, und Professor Max Nieuwdorp, Internist-Endokrinologe und Pionier der Fäkaltransplantationsforschung. Beide Vorträge sind nachzuhören [9]. Auch auf höchster Ebene wird mittlerweile dem Mikrobiom und seiner Bedeutung für die Gesundheit Aufmerksamkeit geschenkt.
References
https://en.wikipedia.org/wiki/The_Grading_of_Recommendations_Assessment,_Development_and_Evaluation_(GRADE)_approach
https://doi.org/10.1002/bies.201800027
https://doi.org/10.1038/s41564-018-0337-x
https://doi.org/10.1038/mp.2016.44
https://doi.org/10.1016/j.jpsychires.2016.07.019
https://doi.org/10.1016/j.nut.2015.09.003
https://doi.org/10.29219/fnr.v62.1218
https://doi.org/10.1016/j.clnu.2018.04.010
https://www.paleisamsterdam.nl/paleissymposium/paleissymposium-the-microbiome/
3: Diät, Darm und Osteoporose
Die Reaktion auf Nahrung ist stark individuell
Die Makronährstoffzusammensetzung der Nahrung erklärt nur 16-32% der Glukosereaktion auf Nahrung. Individuelle Faktoren wie die Zusammensetzung, Funktion und Struktur des Mikrobioms sind viel entscheidender. Dies zeigt die PREDICT-1-Studie, die mehr als 1000 Zwillinge und Nicht-Zwillinge intensiv verfolgte (https://doi.org/10.1093/cdn/nzz037.OR31-01-19, siehe hier die vollständige Präsentation).
Reizdarmsyndrom (RDS) verbessert sich mit Probiotika und Glutamin
Probiotika lindern Schmerzen und verbessern die allgemeine Symptomatik beim Reizdarmsyndrom (IBS), so eine Meta-Analyse von RCTs. Die Wirksamkeit hängt jedoch von der Zusammensetzung ab (https://doi.org/10.3748/wjg.v21.i10.3072). In vielen Fällen besteht beim Reizdarmsyndrom auch eine erhöhte Darmpermeabilität, insbesondere wenn Durchfall im Vordergrund steht. In diesen Fällen hat sich Glutamin als wirksam erwiesen (https://gut.bmj.com/content/68/6/996).
Probiotika möglicherweise nützlich bei Osteoporose
Das Mikrobiom spielt eine wichtige Rolle in der Darm-Knochen-Achse. Tierstudien geben erste Hinweise darauf, dass Probiotika einen schützenden Effekt gegen Osteoporose haben (https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5710820/). Bei älteren Menschen mit Knochenbrüchen führt die Supplementierung mit Probiotika zudem zu einer schnelleren Heilung der Knochen und weniger Schmerzen (http://doi.org/10.3920/BM2016.0067).
2: Saccharomices boulardii
Die Möglichkeiten der magistralen Zubereitung MiBlend vom Microbiome Center wurden erweitert. Ab sofort ist es möglich, einen kraftvollen neuen Stamm als MiBlend-Zutat zu verwenden: Saccharomices boulardii.
Boulardii verfügt über eine starke Evidenzbasis und stellt eine erhebliche Erweiterung der Mittel im Kampf gegen verschiedene Arten von Durchfall dar, wie z. B. antibiotikaassoziierter Durchfall, Reisedurchfall oder akuter und infektiöser Durchfall. Zudem hilft S. boulardii bei der Bekämpfung von Parasiten, pathogenen Bakterien und pathogenen Hefen sowie bei der Verringerung von Entzündungen.
In der Anamnese- und Beratungshilfe wird dieser Inhaltsstoff nun berücksichtigt und für jede Indikation ist die entsprechende Evidenz verfügbar.
Selection from the literature:
http://doi.org/10.1111/apt.13344
http://doi.org/10.3390/antibiotics6040021
http://doi.org/10.1016/j.tmaid.2005.10.003
http://doi.org/10.1542/peds.2013-3950
1: Atemweg, Harnweg, Depression
Mit den kalten, dunklen und nassen Monaten vor uns haben wir diese drei Konzepte aus dem Fachgebiet ausgewählt. Atemwegsinfektion Probiotika können die Häufigkeit und die Dauer von Atemwegsinfektionen bei Kindern verringern, wie aus dieser systematischen Übersichtsarbeit von 23 Studien mit 6269 Kindern hervorgeht (PMID: 27495104: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4979858/). Harnwegsinfektion Lactobacillus-haltige Produkte können wiederkehrende Harnwegsinfektionen bei Frauen möglicherweise verhindern. Der weitverbreitete Einsatz von Antibiotika hat weltweit zu einer Zunahme von E. coli-resistenten Isolaten bei Harnwegsinfektionen geführt. Ein vielversprechender, nicht-antibiotischer Ansatz ist der Einsatz von probiotischen Lactobazillen (PMID: 29602464; https://www.ncbi.nlm.nih.gov/pubmed/29602464). Depression Probiotika scheinen die Empfindlichkeit für Depressionen zu reduzieren. Eine beeinträchtigte Darmbarrierefunktion und Entzündungen sind mit depressiven Symptomen korreliert. Dies wird in verschiedenen Veröffentlichungen behandelt, wie z.B. in einer klinischen Studie zum Effekt des Konsums von probiotischen Nahrungsergänzungsmitteln auf depressive Symptome in einer Stichprobe von Teilnehmern mit leichter bis schwerer Depression (PMID: 31078831; https://www.ncbi.nlm.nih.gov/pubmed/31078831).