Kennisflitsen
Het Microbiome Center verzorgt met regelmaat kennisflitsen voor alle aangesloten artsen.
Hier vindt u een overzicht van de belangrijkste kennisflitsen tot nu toe.
#46: De methode van Microbiome Center: nu peer-reviewed en gepubliceerd
Op zoek naar de beste behandeling voor een patiënt
Elke zorgverlener streeft ernaar de beste behandeling voor elke patiënt te bieden. Het bepalen van wat “de beste” behandeling is, kan echter lastig zijn – vooral bij patiënten met multimorbiditeit, wat tegenwoordig de meest voorkomende situatie is (1). In veel moderne benaderingen van medische besluitvorming speelt wetenschappelijk evidence een centrale rol. Er bestaan verschillende kaders die zorgverleners helpen om evidence te gebruiken bij het kiezen van de meest passende behandeling. Twee van de bekendste zijn Evidence-Based Medicine (EBM) en Personalized Medicine (PM).
Zowel EBM als PM hebben hun eigen sterke punten, maar ook beperkingen. Zo gebruikt EBM gerandomiseerde gecontroleerde studies (RCT’s) als gouden standaard voor onderzoek, omdat dit de beste methode is om de meeste vormen van bias te elimineren (2). Tegelijkertijd laten RCT’s zich niet gemakkelijk vertalen naar patiënten in de dagelijkse praktijk en beschrijven ze slechts het gemiddelde effect, wat het effect bij de individuele patiënt niet voorspelt (3,4).
Deze verschillende beperkingen maken het moeilijk om de EBM- of PM-benadering volledig toe te passen in de klinische praktijk. Omdat chronische patiënten elk een uniek profiel hebben, en omdat het darmmicrobioom zowel zeer individueel is als betrokken bij veel chronische aandoeningen, zag Microbiome Center een grote behoefte aan een nieuwe aanpak.
De methode van het Microbiome Center: nu peer-reviewed en gepubliceerd
In 2019 ontwikkelde Microbiome Center, samen met een samenwerkingsverband van experts uit de immunologie, farmacologie, computationele wetenschappen, citizen science en klinische praktijk, een methodologie om de sterke punten van EBM en PM te combineren. Sindsdien hebben we deze methode geïmplementeerd, verfijnd, verbeterd en verder uitgebreid. Als behandelaar komt u dit tegen wanneer u onze advieshulp gebruikt. Dit is niet slechts een set vragenlijsten en knoppen, het is veel meer dan dat: het is een concrete uitwerking van een uitgebreide en zorgvuldig ontwikkelde filosofie en wetenschappelijke benadering.
Recentelijk zijn de filosofie en de wetenschappelijke methode achter onze aanpak peer-reviewed en gepubliceerd in een wetenschappelijk artikel. Het artikel is geschreven samen met verschillende coauteurs van diverse universiteiten en instituten en is gepubliceerd in het wetenschappelijke tijdschrift Beneficial Microbes (5). In het artikel worden de verschillende sterke punten en valkuilen van de EBM- en PM-methoden besproken, en plaatsen de auteurs deze in een breder perspectief vanuit de wetenschapsfilosofie om beide paradigma’s te integreren. De nieuwe benadering, genaamd Evidence-Based Personalized Medicine (EBPM), is gebaseerd op het filosofische wereldbeeld dat bekendstaat als pragmatisme.
Met deze publicatie is de fundamentele aanpak die Microbiome Center gebruikt nu peer-reviewed en erkend als een solide en innovatieve methode om patiënten te behandelen.
Meer inzichten lezen?
- Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
- Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
Referenties:
#45: Succesvolle pilot met Q-koortsvermoeidheidssyndroom (QVS) patiënten
Het microbioom bij QVS en andere Post-Acute Infectieuze Syndromen (PAIS)
In het kort
Bij patiënten met Post-Acute Infectieuze Syndromen (PAIS), zoals Q-koortsvermoeidheidssyndroom (QVS), ME/CFS en long covid, wordt consistent darmmicrobioom-dysbiose waargenomen. In een pilotproject met 85 QVS-patiënten (met een gemiddelde ziekteduur van 16 jaar) leidde gepersonaliseerde microbioomtherapie tot een verbetering van het algehele welzijn bij bijna 50% van de deelnemers, waarbij 1 op de 7 een duidelijke verbetering ervaarde. Vergelijkbare resultaten worden gezien bij andere PAIS-patiënten. Deze veelbelovende uitkomsten hebben het Microbiome Center ertoe aangezet om de komende maanden extra focus te leggen op PAIS in zowel onderzoek als klinische praktijk.
Het microbioom bij QVS en andere Post-Acute Infectieuze Syndromen (PAIS
Er zijn verschillende vormen van Post-Acute Infectieuze Syndromen (PAIS) bekend, waaronder bijvoorbeeld ME/CFS, long covid, post-behandeling ziekte van Lyme syndroom, post-Pfeiffer vermoeidheidssyndroom (post-EBV), postinfectieuze PDS, en Q-koortsvermoeidheidssyndroom (QVS). Deze vormen van PAIS worden allemaal gekenmerkt door chronische vermoeidheid, post-exertionele malaise, neurocognitieve problemen zoals hersenmist (brain fog), griepachtige symptomen, gewrichtspijn, PDS en een verscheidenheid aan andere klachten (1).
Interessant is dat wetenschappelijke studies darmmicrobioom-dysbiose hebben gevonden bij al deze verschillende vormen van PAIS (1), en er wordt gespeculeerd dat dysbiose mogelijk de onderliggende factor is bij alle PAIS-vormen. Mechanismen waarvan wordt gedacht dat ze een rol spelen zijn persisterende infectie (met de darm als reservoir van de ziekteverwekker), systemische en hersenontsteking, co-infecties (d.w.z. overgroei van pathogenen in de darm) en verstoorde microbioomfuncties zoals verminderde productie van butyraat en neurotransmitters (1).
Q-koortsvermoeidheidssyndroom (QVS) en gepersonaliseerde microbioombehandeling
Q-koorts wordt veroorzaakt door een infectie met de bacterie Coxiella burnetii (een zoönose). De grootste uitbraak van Q-koorts ooit geregistreerd vond plaats in Nederland in 2007-2010 en veel patiënten ontwikkelden Q-koortsvermoeidheidssyndroom (QVS). QVS is een vorm van PAIS en ook bij QVS is darmdysbiose vastgesteld. Sterker nog, de theorie dat het darmmicrobioom de gemeenschappelijke factor is bij alle PAIS-vormen wordt geïllustreerd door een studie die liet zien dat zowel ME/CFS als QVS dezelfde vorm van dysbiose hebben en hetzelfde verschil vertonen ten opzichte van gezonde individuen (2).
De door de overheid gesteunde steungroep genaamd Q-support herkende dat de prevalentie van PDS veel hoger is bij QVS-patiënten. Gecombineerd met de kennis over het microbioom als factor bij QVS, was dit aanleiding om samen met Microbiome Center een pilotproject te starten. In 2024 werden in totaal 85 QVS-patiënten behandeld met leefstijl- en voedingsinterventies, gecombineerd met gepersonaliseerde microbioombehandeling. Gemiddeld waren deze patiënten al 16 (!) jaar ziek.
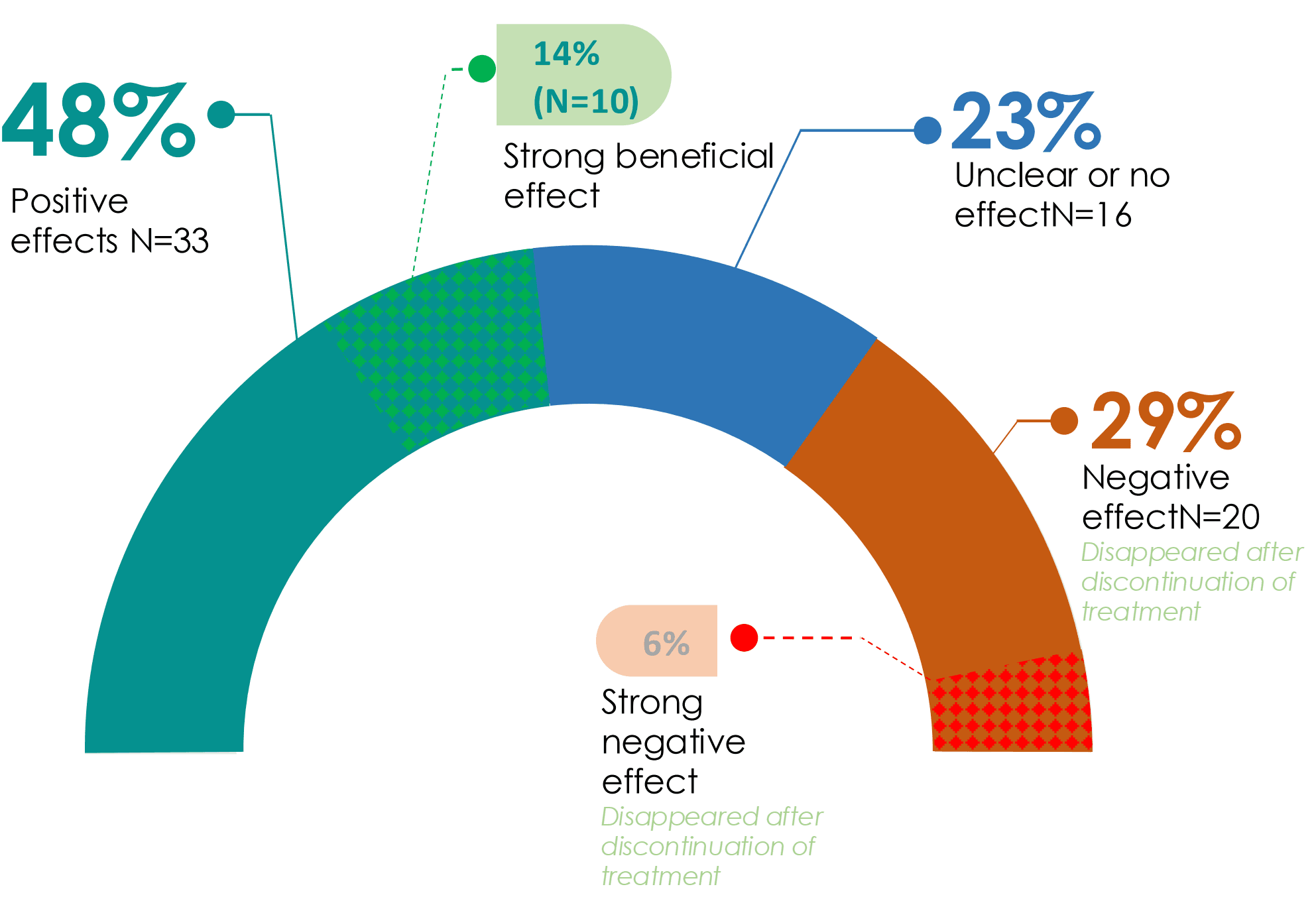
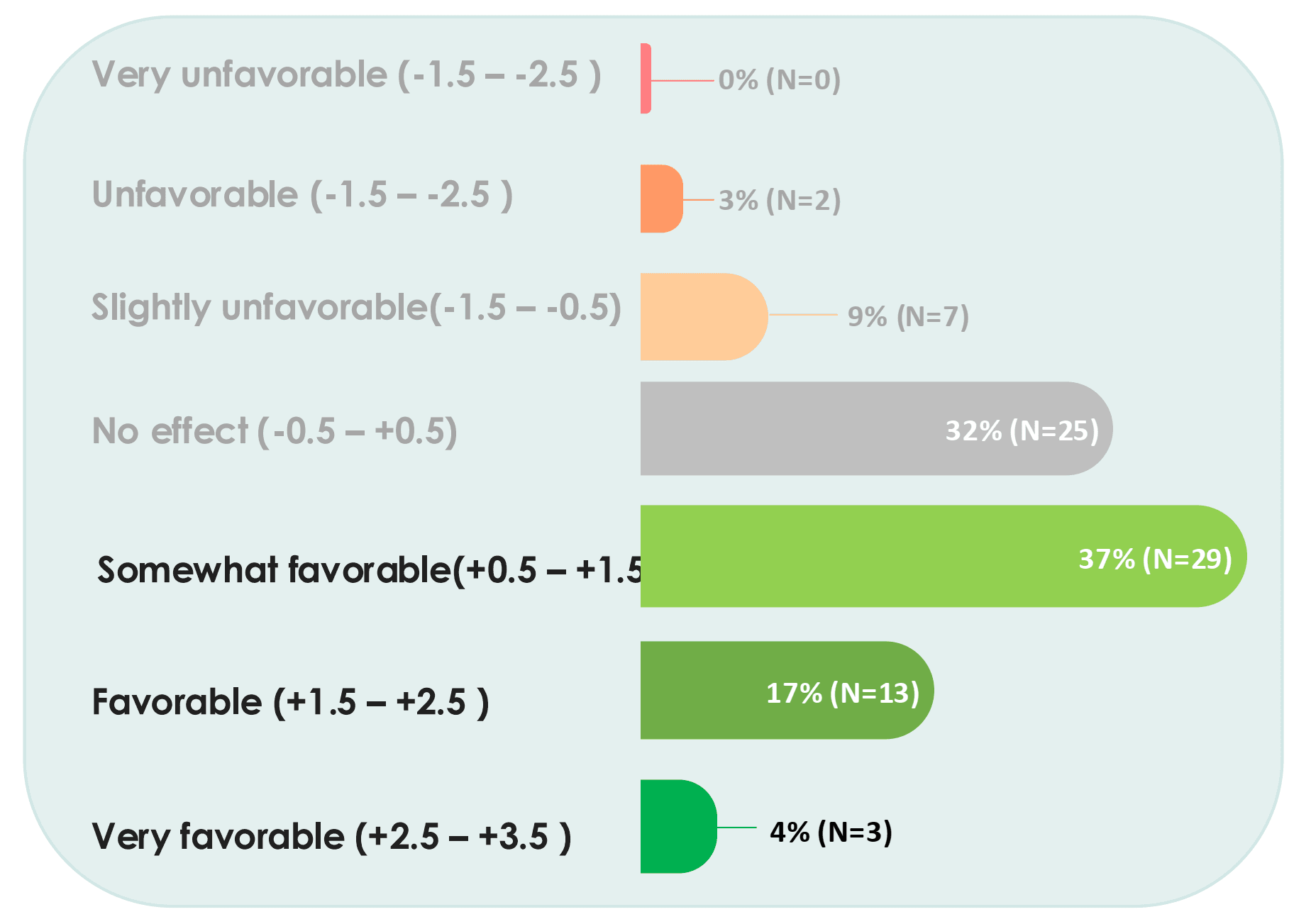
Het project liet zien dat veel patiënten tevreden waren met de behandeling. Na afronding van het pilotproject werd een post-hocanalyse uitgevoerd van de medische klachten en algehele welzijnsscores op basis van gegevens van 69 patiënten. Deze scores werden elke drie weken geregistreerd op het Microbiome Center-platform, wat de waarde van de ‘klachtenbeloop’-tool laat zien. Bijna 50% van de patiënten liet verbetering van het algehele welzijn zien en één op de zeven patiënten rapporteerde een grote verbetering. Sommige mensen zeiden letterlijk dat zij hun leven terug hadden. Ook rapporteerde 57% van de patiënten verbetering van de samengestelde scores van al hun klachten. Zoals verwacht verbeterde niet elke patiënt en sommigen rapporteerden enkele negatieve effecten, maar gelukkig (en zoals verwacht) bleek dat deze verdwenen als de behandeling werd gestaakt.
Met een gemiddelde ziekteduur van 16 jaar en patiënten die reeds allerlei behandelingen hadden geprobeerd, kan een positieve respons bij bijna de helft van de patiënten als een groot succes worden beschouwd.
Microbiome Center heeft PAIS tot thema gemaakt voor de komende maanden
Vanwege deze positieve resultaten hebben wij de geanonimiseerde gegevens geanalyseerd van alle patiënten die daartoe toestemming hebben gegeven en hun medische klachten hebben ingevuld tijdens hun behandeling met MyOwnBlend. In totaal gaven 82 patiënten in een opmerking aan te lijden aan één of meer PAIS-vormen. De meest gerapporteerde PAIS-vormen zijn ME/CFS en long covid. In de gegevens van deze PAIS-patiënten zien we vergelijkbare resultaten als bij de QVS-patiënten, namelijk 59% die een verbetering rapporteert en één op de zes die een grote positieve respons van hun algehele welzijn rapporteert.
Gestimuleerd door deze positieve resultaten heeft Microbiome Center besloten om PAIS tot thema te maken waarop wij ons de komende maanden zullen richten. PAIS komt immers veel voor en er zijn niet veel behandelingen beschikbaar, waardoor veel patiënten wachten op een behandeling die hen kan helpen. Binnen dit thema zullen wij samenwerken in onderzoeksverband om een meer rigoureuze wetenschappelijke studie te starten, zullen wij kijken naar specifieke ingrediënten, en zullen wij de data verder analyseren zodat wij deze scores nog verder kunnen verbeteren.
U kunt helpen!
Als u net zo enthousiast bent over deze eerste resultaten als wij, kunt u helpen. U kunt gepersonaliseerde microbioombehandeling als optie bespreken met uw PAIS-patiënten. Vooral als zij ook lijden aan buikproblemen, kan dit een behandeling zijn die hen kan helpen. Dit kan niet alleen hen mogelijk helpen, maar als zij bereid zijn het beloop van hun klachten op ons platform te registreren, kan het ook andere PAIS-patiënten helpen. We kunnen namelijk samen leren van de inzichten die worden verzameld en de behandeling verder verbeteren. Met een netwerk van meer dan 1000 behandelaars, die allemaal meerdere PAIS-patiënten in hun praktijk hebben, kunnen we gezamenlijk zeer snel leren en behandelingen voor PAIS-patiënten verbeteren.
- Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
Referenties:
- Meer inzichten lezen?
#44: Coeliakie en darmmicrobioom
Coeliakie is niet alleen genetisch
Coeliakie wordt vaak beschouwd als een genetische aandoening. Het is een chronische systemische auto-immuunziekte die wordt gekenmerkt door een verlies van tolerantie voor voedingsgluten. Hoewel de ziekte voorkomt bij personen met een genetische aanleg daarvoor, ontwikkelt niet iedereen met deze aanleg de ziekte, en is er aanzienlijke variatie in zowel de leeftijd van aanvang als in de ernst van de symptomen (1). De enige beschikbare behandeling is een glutenvrij dieet (GFD), maar 30-40% van de patiënten die een GFD volgen, blijft klachten ervaren (1). Een groot aantal studies toont aan dat het darmmicrobioom een belangrijke rol speelt bij de ontwikkeling van coeliakie (1,2). Zo is bekend dat darmdysbiose voorafgaat aan het ontstaan van de ziekte, terwijl genetisch voorbeschikte personen zonder dysbiose gezond blijven (3,4). Bovendien is bekend dat een GFD een gunstig effect heeft op de samenstelling en functie van het microbioom, maar het niet volledig herstelt (5). Er kan worden gesteld dat het gunstige effect van een GFD ten minste gedeeltelijk te danken is aan de invloed ervan op het darmmicrobioom, en niet enkel aan de afwezigheid van immuunstimulerende gluten-eiwitten. In overeenstemming hiermee concluderen wetenschappelijke studies dat het zinvol is om behandeling van het darmmicrobioom te overwegen bij patiënten met coeliakie.
Nieuwe probiotische stam verlicht symptomen van coeliakie en glutenovergevoeligheid
Helaas zijn er niet veel probiotica onderzocht op hun effect bij coeliakie, met slechts enkele uitzonderingen. De momenteel best bestudeerde probiotische stam bij coeliakie is Bifidobacterium longum ES1 (CETCT 7374). Ongeveer een dozijn in vitro– en dierstudies hebben het vermogen van deze stam aangetoond om gliadine af te breken en immuunreacties op gluten te moduleren (zie bijv. 6–8). Een kleine studie bij kinderen met pas vastgestelde coeliakie vergeleek een glutenvrij dieet met en zonder B. longum ES1. In de probioticagroep werden duidelijke verbeteringen gevonden in immuuncellen die bij de ziekte betrokken zijn (9). Bovendien waren de pro-inflammatoire cytokinen aanzienlijk lager in de groep die B. longum ES1 kreeg (9). Verder liet een open-labelstudie bij patiënten met niet-coeliakie glutenovergevoeligheid zien dat, vergeleken met alleen GFD, de groep met GFD + B. longum ES1 meer verbetering vertoonde in gastro-intestinale symptomen (10). Deze stam is nu beschikbaar op het Microbiome Center-platform. Hoewel het geen vervanging is voor een GFD, kan het patiënten met coeliakie of glutenovergevoeligheid helpen bij verdere verlichting van symptomen. Deze interessante probiotische stam heeft ook goede evidence voor een effect bij PDS, waaronder diarree en buikpijn (11,12), evenals bij verschillende andere indicaties. Voor meer informatie, zie de gedetailleerde beschrijving achter de i-knop op het Microbiome Center-platform.
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
Referenties:
- https://doi.org/10.3389/fmedt.2024.1413637
- https://doi.org/10.1007/s00430-017-0496-z
- https://doi.org/10.1073/pnas.2020322118
- https://doi.org/10.1128/spectrum.01468-24
- https://doi.org/10.3390/nu14102083
- https://doi.org/10.1021/jf201212m
- https://doi.org/10.1016/j.ijbiomac.2010.06.015
- https://doi.org/10.1189/jlb.1111581
- https://doi.org/10.1017/S0007114514000609
- https://doi.org/10.23736/S1121-421X.20.02673-2
- https://doi.org/10.1080/19490976.2024.2338322
- https://doi.org/10.3390/jcm9082353
#43: Nieuwe unieke stam, B. adolescentis SH001, een cross-feeder van Fecalibacterium prausnitzii en lactosemetaboliseerder
Introductie van een nieuwe en unieke stam: B. adolescentis SH001
Er zijn verschillende soorten Bifidobacterium op de markt als probiotica, zoals B. lactis, B. longum of B. breve. Een minder bekende bacteriesoort binnen het Bifidobacterium-geslacht is Bifidobacterium adolescentis. Deze soort is echter een van de meest voorkomende Bifidobacterium-soorten in het darmmicrobioom van volwassenen (1). Ze wordt geassocieerd met gezond ouder worden en komt in hogere hoeveelheden voor bij gezonde honderdjarigen (>100 jaar oud) dan bij typische ouderen (1). Interessant genoeg staat B. adolescentis bekend als een belangrijke cross-feeder voor Fecalibacterium prausnitzii, de meest voorkomende boterzuurproducerende soort in het darmmicrobioom (2). Daardoor speelt het een belangrijke rol in het vermogen van het darmecosysteem om boterzuur te produceren.
Enkele weken geleden heeft het Microbiome Center de B. adolescentis stam SH001 beschikbaar gemaakt. Deze stam is genetisch identiek aan de best bestudeerde stam, iVS-1. Hij werd geïsoleerd van een gezond persoon die een dieet kreeg met oplopende hoeveelheden galactooligosacchariden (GOS) (3). Interessant is dat GOS wordt gehydrolyseerd door β-galactosidase, ook wel bekend als lactase. Door deze stam te isoleren uit een GOS-rijke situatie, ontdekten de onderzoekers dat hij meer lactasegenen bevat dan welke andere geteste probiotische stam dan ook.
Lactase kan ook lactose afbreken, en in-vitro-onderzoek toont aan dat deze stam lactose zeer efficiënt kan metaboliseren (4). Belangrijk is dat dit gebeurt met de minste gasproductie in vergelijking met tientallen andere probiotische stammen, en een kleine RCT bevestigde dat het de symptomen van lactose-intolerantie significant vermindert (4). Diezelfde studie toont ook aan dat het buikpijn, een opgeblazen gevoel en winderigheid vermindert. Bovendien liet een andere RCT zien dat deze stam de darmbarrièrefunctie verbetert (5).
Samenvattend: deze unieke nieuwe probiotische stam kan dienen als belangrijke cross-feeder voor boterzuurproducenten, helpt bij de vertering van lactose en het verminderen van symptomen van lactose-intolerantie, en verbetert een lekkende darm. Zoals altijd is het bewijs opgenomen in de Advieshulp en meer informatie is te vinden achter de (i)-knop op ons platform.
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
Referenties:
#42: Onze eerste eigen stam, inzetbaar bij colitis ulcerosa, prostatitis, diverticulitis en diverse andere aandoeningen
Lancering van Microbiome Center’s eerste eigen stam: E. coli MC231
Twee weken geleden hebben we met een kleine feestelijke ceremonie onze eigen eerste stam gelanceerd. Deze stam, de Escherichia coli MC231, is geselecteerd uit een grote set potentiële stammen en heeft anderhalf jaar ontwikkeling gekost, inclusief genoombepaling, karakterisering, ontwikkeling van het productieproces, en stabiliteitstesten.

Microbiome Center’s kernteam viert de lancering van E. coli MC231
De stam E. coli MC231 is ten eerste gekozen omdat de bacteriesoort Escherichia coli een belangrijke rol speelt in het menselijk darm-microbioom, en ten tweede omdat deze specifieke stam genetisch vrijwel identiek is aan de goed onderzochte E. coli Nissle 1917 (ook bekend als Mutaflor©). Dat laatste betekent dat de wetenschappelijke evidence van de E. coli Nissle 1917 ook van toepassing is op de E. coli MC231. In tegenstelling tot de Nissle, is onze MC231 echter wel stabiel op kamertemperatuur.
Deze stam is onder andere uitgebreid onderzocht bij colitis ulcerosa en blijkt in meta-analyses van RCTs veel effectiever dan placebo, en een even goed effect te laten zien als het standaard medicijn 5-ASA (zie bijv. 1). Uit o.a. deze studies blijkt ook een duidelijk anti-inflammatoir effect (1). Een klein onderzoek geeft zelfs enige evidence dat deze stam effectief kan zijn bij de ziekte van Crohn (2), wat bij vrijwel geen enkel probioticum wordt gevonden. Daarnaast is er uitgebreide evidence voor een gunstig effect bij diverse darmproblemen, waaronder bijvoorbeeld diverticulitis (3). Interessant is dat deze stam ook effectief blijkt bij bepaalde aandoeningen buiten de darm. Eén voorbeeld is een vrij sterk recidive-remmend effect bij chronische bacteriële prostatitis (4). Een ander voorbeeld is evidence uit een RCT met deelnemers die acne, rosacea, of seborroïsch eczeem hadden en die duidelijk opknapten t.o.v. placebo (5).
De E. coli MC231 is beschikbaar en uiteraard opgenomen in de Advieshulp en meer informatie over de evidence kunt u vinden via het i-tje achter de stam.
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
References:
#41: Nieuwe stam: Lacticaseibacillus paracasei Lpc-37
Onderzoek naar Lacticaseibacillus paracasei Lpc-37 en zijn klinische toepassingen
Lacticaseibacillus paracasei Lpc-37 werd enkele decennia geleden geïsoleerd uit een zuivelproduct en is sindsdien uitgebreid onderzocht in zowel preklinische als klinische studies. Deze onderzoeken hebben plaatsgevonden met de stam in isolatie of in combinatie met andere probiotische stammen.
Een in wetenschappelijk onderzoek relatief onderbelicht gezondheidsaspect waarbij deze stam is geëvalueerd, betreft slaapkwaliteit. Twee gerandomiseerde placebo-gecontroleerde studies (RCT’s) waarin Lpc-37 als monostam werd onderzocht, lieten een positief effect op slaapkwaliteit zien (1,2). Deze studies werden uitgevoerd bij studenten in de aanloop naar een examen en bij gezonde volwassenen. In beide populaties werd een afname van slaapverstoringen waargenomen ten opzichte van de placebogroep. Daarnaast werd in dezelfde onderzoeken het effect op stress geëvalueerd, waarbij de eerste studie (1) geen significante verschillen vond en de tweede studie (2) wel een positief effect rapporteerde.
Een tweede opvallende indicatie die is onderzocht betreft autisme, waarbij Lpc-37 werd toegediend als onderdeel van een formulering met meerdere probiotische stammen en een prebioticum (3). Hoewel deze pilotstudie beperkingen kent (waaronder een kleine aantal deelnemers en een relatief hoog uitvalspercentage) zijn de bevindingen relevant. Er werd een verbetering waargenomen op een schaal die de ernst van autismespectrumstoornis-symptomen kwantificeert. Dit is bijzonder, aangezien interventies die dit effect laten zien schaars zijn. De studie ondersteunt het concept dat microbioomgerichte interventies een rol kunnen spelen bij autisme. Dit sluit aan bij recente onderzoeken naar de rol van het darmmicrobioom bij autisme, waaronder een multicohortstudie gepubliceerd in Scientific Reports (4). Om deze bevindingen verder te belichten, organiseren wij een webinar over dit thema waarbij ook casuïstiek uit de praktijk besproken wordt. Dit themawebinar over autisme vindt plaats op 17 maart (Engelstalig) en 1 april (Duitstalig) van 19:30-21:00u.
Daarnaast toont een grootschalige RCT met Lpc-37 als monostam een positief effect op de preventie van diarree en koorts (5) en op diverse andere indicaties zoals antibiotica-geassocieerde diarree, cognitieve functies en pathogenen. Voor meer informatie over deze stam en de wetenschappelijke evidence, raadpleeg de aanvullende documentatie via het i-icoon bij dit ingrediënt.
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
References:
#40: De ecologische realiteit van het microbioom en gefaseerde behandeling
In een ecologie gebeurt alles tegelijkertijd
Er zijn verschillende voorbeelden van behandelprotocollen die een gefaseerde of stapsgewijze benadering gebruiken. Een voorbeeld hiervan is de zogenaamde “5R”-aanpak, waarbij de behandeling van de darmgezondheid uit vijf fasen bestaat: “remove”, “replace”, “reinoculate”, “repair”, and “rebalance” (1). De eerste stap (verwijderen) omvat het verwijderen van pathogenen, terwijl pas in de derde stap (opnieuw enten) probiotica worden gebruikt.
Vaak krijgen we de vraag of pathogenen niet eerst moeten worden verwijderd voordat er begonnen wordt met gepersonaliseerde probiotica. Het antwoord is eenvoudig: nee. Het darmmicrobioom is een ecologie, en in een ecologie gebeurt alles tegelijkertijd. Als pathogenen worden verwijderd, worden andere microben ook beïnvloed. Zelfs als antimicrobiële behandelingen alleen de ongewenste microbensoorten zouden doden (wat niet het geval is, ook niet met fytotherapeutica), laat hun verwijdering een open niche achter die door andere soorten wordt opgevuld. Dit gebeurt heel snel, omdat bacteriën zich binnen enkele minuten tot uren repliceren (2).
Laten we eens inzoomen op het feit dat veel protocollen één of twee maanden wachten met de opnieuw-enten-stap, terwijl bekend is dat bacteriën zich in minuten tot uren repliceren. We kunnen een bekend voorbeeld van een ecologie als metafoor gebruiken: een bos. Eén of twee maanden wachten tussen het verwijderen en ‘opnieuw enten’ bij behandelingen van het darmmicrobioom is vergelijkbaar met het platbranden van een bos om ongewenste bomen te verwijderen en vervolgens tientallen jaren te wachten met het planten van nieuwe bomen. De open niches zullen lang voordat je begint met ‘opnieuw enten’ worden opgevuld door nieuwe soorten.
Terug naar gepersonaliseerde probiotica. Naast het feit dat één of twee maanden wachten tussen het verwijderen en ‘opnieuw enten’ niet logisch is in een ecologie van soorten die zich binnen minuten tot uren repliceren, is het ook niet logisch als we naar de effecten van probiotica kijken. De meeste probiotische stammen die beschikbaar zijn bij het Microbiome Center hebben namelijk niet slechts één effect. Vaak kunnen de stammen zowel pathogenen remmen als de gewenste microbioomfuncties verbeteren, zoals de productie van boterzuur, evenals het verbeteren van specifieke klinische resultaten. Het is dus niet het één of het ander.
Veel protocollen die een gefaseerde of stapsgewijze aanpak gebruiken, zijn ontwikkeld door supplementproducenten. Hoewel het hen kan helpen om producten voor elke fase te verkopen, ondersteunt de biologische realiteit deze werkwijze niet. Een meer realistisch perspectief is om het microbioom als een ecologie te beschouwen, en te beseffen dat in een ecologie alles tegelijkertijd gebeurt. Het is dus logisch om ook alles tegelijkertijd én gepersonaliseerd te behandelen.
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/en/medici/kennisflits/
References:
#39: Grip op de bloeiende markt van gepersonaliseerd advies
De vele valkuilen van gepersonaliseerd advies
In het tijdperk van AI komen er steeds meer bedrijven op die gepersonaliseerd dieetadvies en/of aanbevelingen voor voedingssupplementen aanbieden op basis van fecesanalyse en soms op basis van een vragenlijst. Hoewel we enthousiast zijn over het concept van personalisatie, lijkt het er helaas op dat de meeste van deze bedrijven in enkele belangrijke valkuilen trappen.
Sturen op een bepaalde relatief aantal werkt niet
Ten eerste gebruiken bedrijven vaak simpelweg de relatieve aantallen van bacteriesoorten of -geslachten en vergelijken deze met de relatieve aantallen die gevonden worden in gezonde cohorten, om zo te proberen de relatieve overvloed te sturen. Dit negeert het feit dat nog niemand in staat is geweest om gezonde grenzen van relatieve aantallen per soort te definiëren, omdat verschillende microbiomen gezond kunnen zijn (1). In plaats daarvan gedraagt het darmmicrobioom zich als een ecologie waarin de samenstelling afhangt van de omstandigheden, zoals de genetische opmaak van de gastheer, levensstijl, dieet, enz. (2). Het is daarom beter om te kijken naar functionele aspecten van het microbioom (bijv. algehele boterzuurproductie, remming van pathogenen of darmbarrièrefunctie). In tegenstelling tot enkel de relatieve aantallen te gebruiken, bieden deze functionele aspecten wel aanknopingspunten voor behandeling, wat dan ook de reden is waarom Microbiome Center en Biovis deze aanpak hanteren.
De meeste voedingsadviezen zijn gebaseerd op onjuiste aannames en zwakke evidence
Ten tweede is de kracht van de evidence achter veel voedingsadviezen uiterst zwak. Veel is gebaseerd op observationele studies, die vatbaar zijn voor een groot aantal soorten bias en verstorende factoren. Ook hier speelt de nogal reductionistische benadering vaak een rol. Zo wordt er in observationele studies doorgaans van uitgegaan dat het mogelijk is om een voedingscomponent in isolatie te bestuderen, wat het sterk interactieve karakter van voeding negeert. Bovendien negeert dit ook dat het bekend is dat de ene persoon bijvoorbeeld een piek in de bloedsuikerspiegel heeft na het eten van een koekje en niet van een banaan, terwijl een tweede persoon juist het tegenovergestelde ervaart (3). Met andere woorden, het is onmogelijk om te concluderen dat bijvoorbeeld een banaan ongezond is omdat het een piek in de bloedsuikerspiegel veroorzaakt, omdat elk individu anders reageert. Dus elk voedingsadvies dat simplistisch een bepaalde voedingscomponent aan bepaalde effecten koppelt, strookt niet met de realiteit van onze fysiologie. Daarom stellen wij dat een betere aanpak is om eerst te erkennen dat met de extreem complexe en persoonsgebonden reacties op voeding de enige generaliseerbare kennis over voeding logica is: eet voedsel dat dicht bij staat waarop onze fysiologie is geëvolueerd. Dit betekent echt voedsel dat minimaal bewerkt is, zoals groenten, vis, fruit, vlees, noten, zaden, water, kruiden, enz. Ten tweede is het verstandig voor iedereen om te leren de persoonlijke reacties op verschillende voedingsmiddelen en eetpatronen te herkennen – meer gepersonaliseerd wordt het niet!
Vermijd supplementaanbevelingen die gebaseerd zijn op aannames, alleen op soortniveau of zonder referenties
Ten derde adverteren veel bedrijven vaak met gepersonaliseerde aanbevelingen voor probiotische supplementen. Helaas zijn deze aanbevelingen in veel gevallen niet gebaseerd op direct klinische evidence voor de producten, maar eerder op allerlei aannames over het stimuleren van taxa die laag zijn in de fecesanalyse. Hier geldt de eerste valkuil: gezondheid kan niet eenvoudig worden gekoppeld aan relatieve aantallen. Bovendien zijn de aanbevelingen voor probiotica gebaseerd op bacteriesoorten in deze producten, wat het feit negeert dat effecten stam-specifiek zijn (verschillende stammen van dezelfde bacteriesoort kunnen verschillende effecten hebben). Het aanbevelen van een product op basis van soort is als een dierenwinkel die aanbeveelt om “een hond” te kopen, zonder de verschillen tussen bijvoorbeeld een buldog en een labrador te erkennen (beide dezelfde soort). Bovendien is deze manier van redeneren nogal reductionistisch en dat werkt niet in een complexe ecologie zoals het darmmicrobioom. Daarom is het beter om probiotica te selecteren op basis van direct klinisch bewijs met de exacte stam. Dit vermijdt aannames over mechanismen en kijkt direct naar klinische resultaten. Ten slotte tonen veel aanbieders niet op welke evidence hun aanbevelingen zijn gebaseerd, waardoor het moeilijk is te beoordelen of het advies realistisch is.
Conclusie: gebruik evidence-based gepersonaliseerd advies
Wij geloven dat elk gepersonaliseerd advies voor behandeling van het microbioom gebaseerd moet zijn op (1) direct mechanistische en klinische evidence, (2) studies die gebruik maken van de exacte stam, (3) doseringen zoals gebruikt in de studies, en (4) volledige transparantie over de onderliggende evidence.
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/en/medici/kennisflits/
Referenties:
#38 Nieuwe glutathion-producerende stam, nieuwe indicaties
Limosilactobacillus fermentum ME-3
Onlangs is een nieuwe probiotische stam, Limosilactobacillus fermentum ME-3, toegevoegd aan de lijst met bouwstenen die je kunt gebruiken. Deze probiotische stam werd geïsoleerd uit de ontlasting van een gezond kind en behoort tot de zeldzame lactobacillen die over een volledig glutathionsysteem beschikken, waarmee ze deze krachtige antioxidant kunnen produceren (1,2). Interessant is dat in-vitro-, preklinisch en klinisch onderzoek aantonen dat deze stam, in verschillende toedieningsvormen (zoals supplementen, kefir, gefermenteerde geitenmelk en kaas), daadwerkelijk oxidatieve stress op systemisch niveau vermindert (2-5). Daarnaast is er bewijs dat het kan bijdragen aan het verminderen van insulineresistentie (6-8). Verder is aangetoond dat L. fermentum ME-3 verschillende pathogenen kan remmen, waaronder Helicobacter pylori (9-10).
Deze stam is nu beschikbaar als bouwsteen met een typische dagelijkse dosering van 2×10¹⁰ cfu/d (bij 3 g/d). Voor meer informatie en alle studies kun je de i-button raadplegen op ons online platform.
Oxidatieve stress en H. pylori-infectie
Vanwege de unieke eigenschappen van L. fermentum ME-3 om oxidatieve stress te verminderen en H. pylori te remmen, zijn er twee nieuwe vragen toegevoegd aan de tweede stap van de Advice Aid (medische achtergrond).Vermoed je dat jouw cliënt last heeft van oxidatieve stress? Of heb je hier aanwijzingen voor vanuit Biovis mitochondriale diagnostiek? Dan kun je dit nu invullen in de Advice Aid, waarna de nieuwe L. fermentum ME-3-bouwsteen mogelijk wordt geadviseerd. Zijn er aanwijzingen voor een H. pylori-infectie? Dan kun je dit nu ook meenemen in de Advice Aid.
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/en/medici/kennisflits/
References
https://doi.org/10.1080/08910600902815561
https://doi.org/10.1134/S0003683810050030
https://doi.org/10.1186/1475-2891-4-22
https://doi.org/10.1515/biol-2015-0021
https://doi.org/10.2478/s11536-008-0022-1
https://doi.org/10.1186/s12937-016-0213-6
https://doi.org/10.31038/EDMJ.2019324
https://doi.org/10.1002/mnfr.201901018
https://doi.org/10.1111/j.1365-2672.2006.02857.x
https://doi.org/10.1080/08910600802408178
#37: L. crispatus in vaginale preparaten
Afgelopen maand bracht het Amerikaanse bedrijf Seed Health een nieuw vaginaal probioticum op de markt dat meerdere stammen van Lactobacillus crispatus bevat (1). Hun nieuwe vaginale product, VS-01™ ($99,- voor 8 tabletten), kreeg veel aandacht op sociale media (2). Ook andere vaginale producten op basis van L. crispatus zijn in ontwikkeling. Zo werken de bedrijven MGH en Biose Industrie aan een product (LBP) dat meerdere L. crispatus-stammen bevat (3).
Deze ontwikkelingen tonen duidelijk aan dat L. crispatus-preparaten als een veelbelovende aanpak worden beschouwd voor de behandeling van vaginale gezondheidsproblemen, en dat bedrijven aanzienlijk investeren in de ontwikkeling van vaginale oplossingen. Dit sluit aan bij wetenschappelijk onderzoek dat aantoont dat L. crispatus een sleutelrol speelt in de vaginale gezondheid (4).
Met deze innovaties volgen de bovengenoemde producten (die niet in Europa beschikbaar zijn) een concept dat het Microbiome Center al twee jaar geleden implementeerde. Als pionier in de wetenschap ontwikkelde Microbiome Center in samenwerking met een Nederlandse apotheker in 2022 vaginale zetpillen met twee verschillende L. crispatus-stammen. Deze zetpillen zijn beschikbaar als magistrale bereiding (30 zetpillen voor € 88,-). Je kunt deze direct voorschrijven (zonder gebruik van de Advice Aid) via je account. Klik hiervoor op de “Voorschriften”-knop op de homepage en selecteer vervolgens “Magistraal product” op het bestelformulier.
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
References
- https://seed.com/vaginal-synbiotic
- https://www.instagram.com/thealist.us/reel/C7PJXuGpstc/
- https://www.microbiometimes.com/the-clinical-journey-of-a-novel-lbp-for-bacterial-vaginosis-developed-by-mgh-biose-industrie/
- https://doi.org/10.3389/fcimb.2021.631972
- https://www.youtube.com/watch?v=FHGtPdBsLv4
36: Toegevoegde acacia vezels en optie om prebiotica te beperken in Advice Aid
Acacia Senegal vezels
Op veel verzoek hebben we acaciavezels toegevoegd als nieuw ingrediënt. Deze vezel wordt vaak gebruikt als onderdeel van microbiomebehandelingen, omdat het de groei van boterzuur-producerende bacteriën zou stimuleren. Acaciavezels (ook bekend als Arabische gom) worden als voedingssupplement verkocht met een typische dagelijkse dosering van 5-10 g/d. In de MyOwnBlend is de nominale dagelijkse dosis om praktische redenen vastgesteld op 5 g/d. Opvallend is echter dat de meeste wetenschappelijke studies veel hogere doseringen hanteren, meestal 25 g/d of meer. Dit betekent dat voor de meest gangbare doseringen het wetenschappelijke bewijs voor veel indicaties relatief beperkt is.
Desondanks suggereren verschillende onderzoeken dat acaciavezels effectief kunnen zijn bij: Obstipatie (1,2) Opgeblazen gevoel (3) Prikkelbare darm syndroom (PDS/IBS) (lichte positieve trend, maar niet statistisch significant) (1) Metabole disfunctie (insulineresistentie) (4,5) Colitis ulcerosa (5) Parodontitis (6) Stimuleren van boterzuurproductie bij hoge doseringen (7) Meer informatie over deze nieuwe bouwsteen is te vinden via de i-button op ons platform.
Beperk prebiotica in de Advice Aid
Sommige patiënten reageren sterk op prebiotica. Als dit wordt verwacht, kunnen de hoeveelheden worden verlaagd en kunnen er handmatig alternatieven worden toegevoegd bij het voorschrijven. Op verzoek van artsen hebben we deze optie nu ook geïntegreerd in de Advice Aid.Dit is geïmplementeerd voor alle niet-probiotische ingrediënten, waaronder prebiotica zoals PHGG of 2’-fucosyllactose, maar ook andere niet-probiotische componenten zoals glutamine. In stap 2 van de Advice Aid (medische achtergrond) is de nieuwe vraag “Beperk niet-probiotica” toegevoegd. Als je score 1, 2 of 3 selecteert, wordt de maximale dagelijkse dosis van niet-probiotica in de MyOwnBlend respectievelijk beperkt tot 5 g/d, 3 g/d of 1 g/d. Bij score 4 worden niet-probiotische ingrediënten volledig uitgesloten, en zal de MyOwnBlend alleen probiotische ingrediënten bevatten.
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
References
1. https://doi.org/10.1007/s00394-024-03398-8
2. https://pesquisa.bvsalud.org/portal/resource/pt/emr-140096
3. https://doi.org/10.3390/nu13010194
4. https://doi.org/10.4236/fns.2022.134031
5. https://doi.org/10.31989/ffhd.v7i3.325
6. https://doi.org/10.1016/j.sdentj.2017.10.006
7. https://doi.org/10.1038/sj.ki.5000028
35: Urineweginfecties
Probiotica voor urineweginfecties
Lange tijd werd gedacht dat de urinewegen steriel waren. Onderzoek van het afgelopen decennium heeft echter aangetoond dat er een microbiome in de urinewegen bestaat, het zogenaamde urobiome (1). Urineweginfecties (UWI’s) behoren tot de meest voorkomende infecties, vooral bij vrouwen. In de VS heeft zelfs één op de drie vrouwen onder de 24 jaar antibiotica voorgeschreven gekregen voor een UWI (1). De kans op herhaling is hoog, tot wel 30% binnen zes maanden. Het veelvuldig gebruik van antibiotica draagt bij aan antibioticaresistentie en kan de samenstelling van zowel het darm- als het urobiome veranderen, waardoor het risico op terugkerende infecties en andere infecties toeneemt (1,2).
Vooral vrouwen hebben vaak last van UWI’s, waarbij zowel de darm-blaas- als de vagina-blaas-as een rol spelen. Dit komt doordat zowel het darm- als het vaginale microbioom een bron kan zijn van ziekteverwekkers die UWI’s veroorzaken (2). Het gezond houden van deze twee microbiomen is essentieel om overgroei van opportunistische pathogenen, die UWI’s kunnen veroorzaken, te voorkomen. Klinische studies tonen aan dat specifieke orale en vaginale probiotica het risico op UWI’s kunnen verlagen (2).
Hoewel de behandeling van het darmmicrobioom steeds bekender wordt en fecale analyses kunnen helpen bij het opsporen van mogelijke pathogenen voor gepersonaliseerde microbiomebehandelingen, is het vaginale microbioom minder goed onderzocht. In tegenstelling tot het darmmicrobioom wordt een gezond vaginaal microbioom gekenmerkt door een zeer lage diversiteit. Een hoge diversiteit in het vaginale microbioom wordt juist geassocieerd met dysbiose en overgroei van pathogenen (3). Een vaginaal microbioom dat wordt gedomineerd door Lactobacilli (met name Lactobacillus crispatus) wordt als gezond beschouwd en kan de groei van UWI-veroorzakende pathogenen zoals E. coli remmen (4). Een gerandomiseerde gecontroleerde studie (RCT) met een vaginaal toegediende probiotica die een L. crispatus-stam bevatte, liet een verminderd risico op terugkerende UWI’s zien, vooral wanneer de probiotische stam het vaginale microbioom succesvol koloniseerde (5).
Om deze reden bevatten de magistrale vaginale zetpillen, ontwikkeld door Microbiome Center in samenwerking met onze apotheker, twee verschillende L. crispatus-stammen. Afhankelijk van de aanwezigheid van dysbiose in de darm of vagina, kun je patiënten met UWI’s behandelen met een gepersonaliseerde darmmicrobioombehandeling en/of vaginale zetpillen. De gepersonaliseerde darmmicrobioombehandeling kan worden voorgeschreven via de Advice Aid op ons platform. De vaginale zetpillen kunnen direct worden voorgeschreven via de knop “Nieuw” en vervolgens door de categorie “Magistraal product” bovenaan te selecteren.
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
References:
https://doi.org/10.1016/j.micres.2022.127010
https://doi.org/10.3390/diagnostics11010007
https://doi.org/10.1097/LGT.0000000000000643
https://doi.org/10.1128/microbiolspec.UTI-0025-2016
https://doi.org/10.1093/cid/cir183
34: Sporenvormende bacteriën
Sporenvormende bacteriën als probiotica
Recentelijk hebben verschillende bedrijven die probiotische producten op de markt brengen, de aandacht gevestigd op sporenvormende probiotische bacteriën. Maar wat zijn sporenvormers en wat zijn hun voordelen?
De meeste probiotica op de markt bestaan uit Lactobacilli en/of Bifidobacteria, waaronder bekende stammen zoals Lactobacillus rhamnosus GG en Bifidobacterium animalis subsp. lactis BB-12. Probiotische stammen worden meestal geselecteerd op basis van hun overlevingskansen in het maag-darmkanaal (GI) en hun houdbaarheid, omdat deze factoren de grootste uitdagingen vormen voor de bacteriën.
In tegenstelling tot Lactobacilli en Bifidobacteria kunnen sommige bacteriesoorten zogenaamde endosporen vormen. Dit zijn metabolisch inactieve cellen met een extreem sterke buitenwand, waardoor ze extreme omstandigheden kunnen doorstaan en zelfs miljoenen jaren kunnen overleven (1). Dit maakt direct een van de belangrijkste voordelen van sporenvormende bacteriën duidelijk: ze hebben een uitstekende houdbaarheid, kunnen hoge temperaturen weerstaan (sommige sporenvormende probiotica worden zelfs gebruikt in thee of gebak) en overleven goed in het maag-darmkanaal. De endosporen worden in de darm weer geactiveerd en kunnen daar hun gunstige effecten uitoefenen. Bovendien behoren deze sporenvormers tot andere bacteriegenera dan de gangbare probiotica, en hebben deze probiotische soorten en stammen specifieke eigenschappen.
De meest bekende en onderzochte sporenvormende soorten zijn Bacillus subtilis, B. coagulans en B. clausii (1). De collectie van het Microbiome Center bevat goed onderzochte stammen van elk van deze soorten, zoals B. subtilis R-179, B. coagulans Unique IS-2 en B. clausii UBBC-07. Deze stammen zijn onder andere bestudeerd voor de behandeling van colitis ulcerosa en SIBO (2,3), verstopping en PDS (prikkelbare darm syndroom) (4,5) en diarree en luchtweginfecties (6,7).
Minder bekende sporenvormende probiotische bacteriën zijn onder andere B. mesentericus en Clostridium butyricum, die beide deel uitmaken van de Butyrate Generator bouwsteen. C. butyricum kan boterzuur (butyraat) produceren, en dit werkingsmechanisme zorgt voor een sterk ontstekingsremmend effect en maakt deze bouwsteen effectief bij colitis ulcerosa (8). Daarnaast wordt verwacht dat dit ook de reden is waarom onze eigen data-analyses consequent hebben aangetoond dat deze bouwsteen effectief is tegen allergieën, aangezien allergieën verband houden met ontregelde immuunreacties en butyraat deze kan moduleren.
Conclusie
Er bestaan verschillende sporenvormende probiotische soorten. De best onderzochte stammen van bekende Bacillus-soorten, evenals enkele minder gangbare stammen, zijn beschikbaar als bouwstenen op het Microbiome Center platform.
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
References:
https://doi.org/10.3390/ijms23063405
https://doi.org/10.12998/wjcc.v6.i15.961
https://doi.org/10.1155/2020/4181748
https://doi.org/10.1007/s12602-019-09542-9
https://doi.org/10.3920/BM2017.0129
https://doi.org/10.3920/BM2012.0034
https://doi.org/10.2147/tcrm.2007.3.1.13
https://doi.org/10.3748/wjg.v21.i19.5985
33: Nieuw ingrediënt, nieuwe vragen
Bifidobacterium lactis HN019
Onlangs is er een nieuwe bouwsteen toegevoegd aan de lijst met opties die je kunt gebruiken voor gepersonaliseerde microbiomebehandelingen. Deze bouwsteen bevat Bifidobacterium lactis HN019, een uitgebreid bestudeerde probiotische stam die oorspronkelijk is geïsoleerd uit yoghurt. Meerdere hoogwaardige RCT’s tonen aan dat deze stam effectief is tegen parodontitis (1-3).
Daarnaast heeft een meta-analyse van klinische studies aangetoond dat HN019 ook effectief is in het stimuleren van de cellulaire immuniteit bij ouderen (4). Dit omvat de fagocytische capaciteit van polymorfonucleaire cellen (het vernietigen van binnendringende ziekteverwekkers via fagocytose) en de tumor dodende activiteit van natuurlijke killercellen (het elimineren van tumorcellen). Bovendien hebben grootschalige klinische studies aangetoond dat HN019 effectief is bij het voorkomen van luchtweginfecties en ijzertekort bij kinderen (5-7).
Deze stam is ook onderzocht op andere effecten, waaronder verstopping, winderigheid en ontstekingsremmende eigenschappen. Alle informatie over het beschikbare bewijs voor deze stam is te vinden op ons webplatform door te klikken op de i-knop achter deze bouwsteen.
Bijgewerkte Advice Aid-vragen
Met de toevoeging van de B. lactis HN019-bouwsteen zijn er nieuwe indicaties toegevoegd aan de lijst met medische achtergronden. Dit omvat parodontitis, cellulaire immuniteit en ijzertekort.
Daarnaast is de vraag over opgeblazen gevoel/winderigheid in de klachtenlijst opgesplitst in twee aparte vragen. Hoewel deze klachten aan elkaar gerelateerd zijn, zijn ze niet hetzelfde en rechtvaardigt het wetenschappelijke bewijs van verschillende bouwstenen deze scheiding. Zo laat het bewijs voor B. lactis HN019 zien dat deze stam een effect heeft op winderigheid, maar niet op een opgeblazen gevoel.
Door voortdurend het wetenschappelijke bewijs en de Advice Aid-vragen te evalueren, zorgt het Microbiome Center voor een continu verbeteringsproces. Zo kun jij jouw patiënten de best mogelijke behandeling bieden.
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
References:
https://doi.org/10.1111/jcpe.12995
https://doi.org/10.1371/journal.pone.0238425
https://doi.org/10.1007/s00784-022-04744-y
https://doi.org/10.3390/nu9030191
https://doi.org/10.1371/journal.pone.0012164
https://doi.org/10.3920/BM2022.0041
https://doi.org/10.1097/MPG.0b013e3181d98e45
32: Migraine
De rol van het darmmicrobioom bij migraine
Veel gezondheidsproblemen worden in verband gebracht met het darmmicrobioom, zelfs als deze problemen zich elders in het lichaam bevinden en er geen directe link met de darm wordt vermoed. Migraine is een goed voorbeeld hiervan. Het feit dat PDS (prikkelbare darm syndroom) 2 tot 4 keer vaker voorkomt bij migrainepatiënten dan bij gezonde controles, is al een eerste aanwijzing dat het darmmicrobioom een rol speelt (1,2).
Een mechanisme dat zowel bij migraine als bij het darmmicrobioom betrokken lijkt te zijn, is het falen van verschillende anatomische barrières, waaronder de darm-bloedbarrière, de bloed-hersenbarrière en de bloed-hersenvochtbarrière. Het microbioom kan al deze barrières beïnvloeden (3,4). Interessant is dat de bloed-hersenbarrière bestaat uit endotheelcellen, en onderzoek bij kinderen heeft aangetoond dat endotheeldisfunctie voorkomt bij migrainepatiënten (5). Aangezien het microbioom ook invloed heeft op de bloed-hersenvochtbarrière, is het relevant dat migraine wordt gekenmerkt door meningeale ontsteking, waarbij ontstekingssignalen zich via het hersenvocht verspreiden (6).
De belangrijkste farmaceutische behandelingen van migraine zijn serotonine-agonisten. Dit is gebaseerd op overtuigend mechanistisch onderzoek sinds de jaren 50, waarin werd aangetoond dat serotonine een cruciale rol speelt bij migraine (7). Serotonine wordt in het lichaam gesynthetiseerd uit het aminozuur tryptofaan, en het is bekend dat het darmmicrobioom het tryptofaanmetabolisme beïnvloedt (8,9). Een verstoorde balans van andere tryptofaanmetabolieten, zoals kynurenine, wordt in verband gebracht met migraine en PDS (9).
Een overgroei van Helicobacter pylori en andere pathogenen wordt eveneens geassocieerd met migraine (8-10). Zowel deze factoren als de eerder genoemde verstoringen kunnen positief worden beïnvloed door probiotica, en een aantal RCT’s hebben aangetoond dat specifieke probiotica effectief kunnen zijn bij de behandeling van migraine (11).
Al deze inzichten laten zien dat het de moeite waard is om het darmmicrobioom in overweging te nemen bij de behandeling van migrainepatiënten. Een eenvoudige manier om snel te achterhalen of een verstoord microbioom een rol kan spelen bij een specifieke patiënt, is het gebruik van de Bristol Stool Chart (BSC) en de vragenlijst over gastro-intestinale klachten. Vaak is het nodig om door te vragen, omdat veel patiënten terughoudend zijn om over hun ontlasting te praten en de link tussen de darm en migraine niet direct zien.
Ben je geïnteresseerd in deze eenvoudige tool? Dan kun je de BSC en vragenlijst gratis ontvangen in het Nederlands, Duits of Engels door te reageren op deze e-mail. Als er gastro-intestinale klachten aanwezig zijn, kan een fecale analyse inzicht geven in welke microbiome functies verstoord zijn (bijvoorbeeld een lekkende darm, pathogenen, ontstekingen, etc.). Op basis hiervan kan een evidence-based gepersonaliseerde microbiomebehandeling worden ingezet om deze verstoringen gericht aan te pakken.
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
References:
https://doi.org/10.1002/brb3.2291
https://doi.org/10.1155/2022/8690562
https://doi.org/10.1177/1535370217743766
https://doi.org/10.1111/ejn.15878
https://doi.org/10.1111/ped.14946
https://doi.org/10.1186/s10194-021-01353-0
https://doi.org/10.1152/physrev.00034.2015
https://doi.org/10.1186/s10194-020-1078-9
https://doi.org/10.3390/ijms221810134
https://doi.org/10.2147/NDT.S144955
https://doi.org10.1080/1028415X.2020.1764292
31: Bewijsupdates
Bewijs wordt continu bijgewerkt
Om de best mogelijke behandelingsopties aan te bieden, werkt Microbiome Center voortdurend het bewijs van alle beschikbare ingrediënten bij.
Een recent voorbeeld is de toevoeging van bewijs voor Bacillus clausii UBBC-07. Nieuwe studies zijn gepubliceerd over de effecten op infecties van de bovenste luchtwegen, de preventie van door radiotherapie geïnduceerde mucositis, en colitis ulcerosa (1-3). Een goed uitgevoerde RCT met 90 kinderen toonde aan dat behandeling met B. clausii UBBC-07, vergeleken met placebo, leidde tot een aanzienlijke vermindering van het gemiddelde aantal, de duur en de ernst van infecties van de bovenste luchtwegen (1). Een andere RCT onderzocht of deze stam de bijwerkingen van radiotherapie bij hoofd- en halskankerpatienten kan verminderen, met name mucositis (2). Het werd gevonden dat de tijd tot het begin van mucositis langer was, de duur van mucositis korter was en, het meest opvallend, dat de ernst van mucositis aanzienlijk minder was. Een derde RCT bij IBD-patiënten toonde een voordeel van B. clausii UBBC-07 op de ziekteactiviteitsscore en ontstekingsmarkers in vergelijking met placebo bij patiënten met colitis ulcerosa, maar niet bij patiënten met de ziekte van Crohn. Dit toont het belang van het maken van een onderscheid tussen deze twee verschillende ziekten binnen het IBD-cluster.
Een ander voorbeeld van een stam met recent toegevoegd bewijs is Bacillus coagulans Unique IS-2. Deze stam werd ook onderzocht op zijn effect bij colitis ulcerosa, met soortgelijke bevindingen als de eerder genoemde B. clausii UBBC-07 studie (4). Interessant is dat er al bewijs was dat B. coagulans Unique IS-2 effectief is bij constipatie, en een nieuwe goed uitgevoerde RCT bevestigt dat deze stam een groot effect heeft op constipatie (5).
Deze en andere bewijsupdates worden voortdurend verwerkt en toegevoegd aan de Advice Aid, zodat de voorgestelde gepersonaliseerde preparaten altijd zijn gebaseerd op de best beschikbare kennis en het meest complete overzicht van het wetenschappelijke bewijs. Alle studies zijn te vinden onder de i-knop van elk ingrediënt.
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
References:
30: Vaginale zetpillen
De rol van het vaginale microbioom bij vaginale klachten
Vaginale klachten komen veel voor in de huisartsenpraktijk. Een Nederlandse publicatie uit 2002 vermeldt dat 40% van de ondervraagde vrouwen in de voorgaande week vaginale afscheiding had (1). Internationaal onderzoek toont aan dat, hoewel er grote variatie tussen landen is, de prevalentie van bacteriële vaginose in westerse landen varieert van 5-20% (2).
Net als de darmen, huid of longen heeft de vagina een eigen, specifiek microbioom en veel vaginale klachten worden in verband gebracht met een verstoord vaginaal microbioom. Zo is de belangrijkste oorzaak van abnormale vaginale afscheiding, bacteriële vaginose, gekarakteriseerd door vaginale dysbiose die voorafgaat aan de klachten (3). Wanneer bacteriële vaginose leidt tot klachten, wordt dit doorgaans behandeld met antibiotica, maar dit heeft een hoog terugvalpercentage (2). Dit is niet verrassend, aangezien antibiotica het vaginale microbioom nog verder kunnen verstoren.
Naast vaginale klachten speelt het vaginale microbioom ook een rol bij de vruchtbaarheid. De kans op een succesvolle zwangerschap is groter wanneer er een gezond, Lactobacillus-gedomineerd vaginaal microbioom aanwezig is (4,5).
Omdat veel vaginale klachten verband houden met vaginale dysbiose, is een interventie die zich richt op het vaginale microbioom gewenst. Om deze reden heeft Microbiome Center, samen met de apotheker en een aantal artsen in ons netwerk, vaginale zetpillen ontwikkeld. Deze bevatten drie probiotische stammen in hoge dosering, waaronder twee Lactobacillus crispatus-stammen. Deze bacteriesoort wordt sterk geassocieerd met een gezond vaginaal microbioom (3). De zetpillen kunnen online worden voorgeschreven als een set van 30 stuks en worden magistrale bereid door de apotheker.
Als u meer wilt leren over het vaginale microbioom, de rol ervan bij vaginale klachten zoals bacteriële vaginose en vulvovaginale candidiasis en bij vruchtbaarheid, en hoe vaginale zetpillen kunnen worden gebruikt, kunt u deelnemen aan ons online webinar (in het Nederlands) op 20 april 2023 van 19:30-21:00 uur.
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
References:
1. https://www.henw.org/artikelen/vaginale-klachten
2. https://doi.org/10.1016/j.ejogrb.2019.12.035
3. https://doi.org/10.3389/fcimb.2021.631972
29: De microbiome-migraine verbinding
Het darmmicrobiome speelt een rol bij migraine
Migraine is een invaliderende, veelvoorkomende aandoening die ongeveer 15% van de bevolking treft. Het is algemeen bekend dat veel migrainepatiënten last hebben van misselijkheid of braken, maar andere gastro-intestinale klachten komen ook vaak voor. Bijvoorbeeld, migrainepatiënten hebben 2-4 keer vaker last van prikkelbare darm syndroom (IBS) dan gezonde mensen (1,2). Dit is een sterke aanwijzing dat darmgezondheid verband houdt met migraine.
De afgelopen jaren zijn verschillende mechanismen geïdentificeerd die een rol kunnen spelen in de microbiome-migraine verbinding. Zo worden bij migrainepatiënten verstoorde anatomische barrières, zoals de darm-bloed- en bloed-hersenbarrière, waargenomen, wat kan leiden tot systemische en neuro-inflammatoire reacties (3,4). Insuline-signalisering is ook verstoord bij migrainepatiënten en het is bekend dat het microbiome deze direct kan beïnvloeden (4,5).
Daarnaast is het algemeen bekend dat verstoorde serotonine-signalisering een belangrijke rol speelt in de pathogenese van migraine (6). Belangrijk is dat de stofwisseling van de precursor tryptofaan via de serotonine-, indool- of kynureninepaden wordt beïnvloed door het darmmicrobiome (7). Het is bijvoorbeeld bekend dat metabolieten uit het kynureninepad de NMDA-receptor beïnvloeden, die een rol speelt in de corticale spreidingsdepressie van migraine. Interessant is dat verschillende tryptofaanmetabolieten ook verstoord zijn bij IBS-patiënten.
Een ander potentieel mechanisme dat is geïdentificeerd, is pathogeen overgroei. Bijvoorbeeld, Heliobacter pylori-infectie wordt geassocieerd met migraine (7). Bovendien is er ook overgroei van andere pathogene bacteriën en gisten gevonden bij migrainepatiënten (8). Aangezien veel pathogene bacteriële soorten in staat zijn om histamine te synthetiseren, is het interessant dat histamine-overgevoeligheid ook een rol speelt bij migraine (9).
Samenvattend, de identificatie van deze mechanismen suggereert dat, als een migrainepatiënt ook gastro-intestinale klachten heeft, een functiegerichte fecale analyse kan helpen om te identificeren welke paden bij die persoon betrokken kunnen zijn. Op basis hiervan en andere klachten en medische problemen kan een gerichte interventie worden samengesteld.
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
Referenties:
- https://doi.org/10.1002/brb3.2291
- https://doi.org/10.1155/2022/8690562
- https://doi.org/10.1177/1535370217743766
- https://doi.org/10.1111/ped.14946
- https://doi.org/10.1016/j.molcel.2020.03.005
- https://doi.org/10.1152/physrev.00034.2015
- https://doi.org/10.3390/ijms221810134
- https://doi.org/10.2147/NDT.S144955
- https://doi.org/10.1186/s10194-019-0984-1
28: Nieuw ingrediënt: gepasteuriseerde Akkermansia muciniphila
Gepasteuriseerde Akkermansia muciniphila, een postbioticum
In ongeveer één op de acht stoelganganalyses is Akkermansia muciniphila sterk verminderd (minder dan 1×105 CFU/g) en in een grotere groep is het substantieel verminderd. Dit is een aanwijzing voor een verstoorde slijmlaag, die een belangrijk onderdeel vormt van de darmbarrière. A. muciniphila staat bekend om het verbeteren van de integriteit van de darmepitheelcellen en de dikte van de slijmlaag en speelt een rol in de gastheerimmunoregatie, waardoor het de darmgezondheid bevordert (1). Interessant genoeg kunnen belangrijke delen van de gunstige effecten van A. muciniphila worden herleid tot Amuc_1100, een specifiek pili-achtig eiwit geïsoleerd uit het buitenste membraan van A. muciniphila (2). Dit is de reden waarom gepasteuriseerde A. muciniphila net zo effectief is als levende cellen, zoals aangetoond in onder andere de eerste menselijke studie tot nu toe (3). Omdat A. muciniphila gepasteuriseerd is en het actieve ingrediënt dus niet uit levende bacteriën bestaat, wordt het een postbioticum genoemd (4).
De eerder genoemde RCT toont aan dat suppletie met gepasteuriseerde A. muciniphila leidt tot verlagen van insulineresistentie, evenals gewichts- (en lichaamsvet)verlies (3). Dit effect wordt ondersteund door bewijs uit talrijke dierstudies, zoals bijvoorbeeld getoond in een systematische review van tien dierstudies (5). Deze en andere therapeutische effecten (bijv. op colitis of allergieën) worden gekoppeld aan de ontstekingsremmende en darmbarrière-herstellende effecten, zoals aangetoond in zowel de RCT als vele dierstudies (3, en bijv. 6, 7). Dit omvat stimulatie van slijmproductie en een verhoogde dikte van de slijmlaag (6).
Per 1 februari is gepasteuriseerde A. muciniphila beschikbaar als nieuw bouwblok dat je kunt selecteren als ingrediënt voor MyOwnBlend. Meer informatie over dit postbioticum en de effecten ervan is te vinden onder de (i)-knop op ons platform.
We organiseren een webinar om verdere achtergrondinformatie te geven over de rol van A. muciniphila in gezondheid en ziekte op 23 februari en 21 maart van 19:30-21:00u. Als je geïnteresseerd bent om deel te nemen, kun je op deze e-mail antwoorden, inclusief de datum van voorkeur.
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
Referenties:
- https://doi.org/10.1111/1751-7915.13410
- https://doi.org/10.1371/journal.pone.0173004
- https://doi.org/10.1038/s41591-019-0495-2
- https://doi.org/10.1038/s41575-021-00440-6
- https://doi.org/10.3390/microorganisms9051098
- https://doi.org/10.12182/20220160304
- https://doi.org/10.3389/fmicb.2019.02259
27: Nieuwe stam effectief bij acne en cariës
Nieuwe stam: Lacticaseibacillus rhamnosus SP1
Wanneer we interessante ingrediënten tegenkomen voor microbiomebehandelingen, proberen we deze beschikbaar te stellen zodat de mogelijkheden voor het behandelen van patiënten blijven uitbreiden. We hebben nu de stam Lacticaseibacillus rhamnosus SP1 toegevoegd, die onder andere is bestudeerd voor de effecten op acne en cariës. Het is belangrijk om te vermelden dat veel effecten stam-specifiek zijn en dat er veel verschillende stammen binnen de L. rhamnosus-soort bestaan. Het moet worden opgemerkt dat niet alle stammen van deze soort hetzelfde effect zullen hebben als deze stam, genaamd SP1.
Een klein maar goed uitgevoerd gerandomiseerd gecontroleerd onderzoek (RCT) met L. rhamnosus SP1 toont aan dat het leidt tot verbeterde of merkbaar verbeterde acne-symptomen vergeleken met placebo (1). Bovendien toonde deze studie aan dat het gebruik van L. rhamnosus SP1 een duidelijke afname van de expressie van insuline-achtige groeifactor 1 (IGF1) veroorzaakte in huidsmonsters van de probiotische groep vergeleken met placebo, wat bewijs is voor een effect op insuline-signalisering. Inderdaad, toenemend bewijs toont aan dat een verstoorde darmmicrobiota geassocieerd is met acne, deels vanwege het effect op insuline-signalisering, maar klinische proeven met probiotische interventies zijn schaars (2). Dit maakt L. rhamnosus SP1 op zichzelf al een interessante toevoeging.
Een andere studie die met deze stam werd uitgevoerd is een groot RCT (en een subgroepanalyse daarvan) die het effect van deze stam onderzocht op de preventie van cariës bij kleuters. De resultaten laten zien dat L. rhamnosus SP1, vergeleken met placebo, effectief cariës voorkomt (3,4). Een andere RCT over mondgezondheid levert bewijs voor een effect op Candida-geassocieerde denture stomatitis (5). Deze studie biedt ook direct bewijs voor een remmend effect op (orale) candida.
Meer informatie over deze stam en zijn effecten is te vinden onder de (i)-knop op ons platform.
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
References:
- https://doi.org/10.3920/BM2016.0089
- https://doi.org/10.3390/microorganisms10071303
- https://doi.org/10.1177/0022034515623935
- https://doi.org/10.1007/s00784-020-03712-8
- https://doi.org/10.1111/adj.12692
26: Correlatie tussen depressie en Enterobacter
Boven alles is Microbiome Center een netwerkorganisatie met als doel de leercyclus drastisch te verkorten. Dit betekent dat jij, de artsen in ons netwerk, evidence-based gepersonaliseerde microbiomebehandelingen kunt voorschrijven en tegelijkertijd nieuwe kennis kunt genereren. Het analyseren van geanonimiseerde data (bijvoorbeeld resultaten van fecesanalyse) met toestemming van de patiënt kan nieuwe inzichten opleveren die toekomstige patiënten ten goede kunnen komen door nog betere behandelingen mogelijk te maken. Onze recente data-analyse heeft zo’n inzicht opgeleverd, namelijk een correlatie tussen de overgroei van Enterobacter spp. en vatbaarheid voor somberheid (d.w.z. depressie of een gedeprimeerde stemming).
In de totale cliëntenpopulatie is de prevalentie van een gedeprimeerde stemming ongeveer 18%. Bij cliënten die hoge niveaus van mogelijk pathogene Enterobacter-soorten in hun fecesanalyse-resultaten hebben, is de prevalentie van een gedeprimeerde stemming echter bijna twee keer zo hoog, namelijk 29%. Dit suggereert dat deze potentiële ziekteverwekker geassocieerd is met depressie.
Een literatuuronderzoek toont vergelijkbare bevindingen, zij het minder expliciet, waarbij blijkt dat patiënten met bipolaire depressie hogere niveaus van Enterobacter spp. hebben vergeleken met gezonde controles (1). Dit werd ook gevonden bij patiënten met depressie op latere leeftijd (2). De onderzoekers van de eerste studie beschrijven ook een associatie tussen verhoogde ontstekingsactiviteit en overgroei van Enterobacter spp. Ontsteking wordt geassocieerd met depressie (3). Samenvattend suggereren onze bevindingen en de literatuur dat verhoogde Enterobacter spp. ontsteking kunnen veroorzaken en daardoor depressie kunnen veroorzaken. Dit is een nuttig inzicht, omdat specifieke probiotische stammen bekend staan om potentiële ziekteverwekkers zoals Enterobacter spp. te remmen en ontsteking te verlagen, en dus nuttig kunnen zijn bij cliënten met depressie.
Dit is slechts één voorbeeld van hoe we inzichten genereren terwijl we cliënten helpen. Samen leren we van de praktijk en verbeteren we de behandelingen continu. Als je meer wilt weten, laat het ons dan weten, of woon de webinars bij over data-analyse (14 november, in het Nederlands) of depressie (14 december, in het Nederlands). Deze webinars worden begin 2023 herhaald in het Engels.
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
Referenties:
https://doi.org/10.3389/fpsyt.2019.00784
https://doi.org/10.3389/fnagi.2022.885393
https://doi.org/10.1111/ejn.14631
https://doi.org/10.1016/j.clnu.2018.09.010
25: L. plantarum DR7, artritis en microbiële butyraat
Nieuwe stam: Lactiplantibacillus plantarum DR7
Er is een nieuwe stam toegevoegd aan de lijst waaruit je kunt kiezen, de L. plantarum DR7. Deze stam is geïsoleerd uit vers koeienmelk in Maleisië (1). Het heeft ontstekingsremmende effecten, zowel aangetoond in preklinische als klinische studies (2-4), en stimuleert de AMPK-activiteit (5). AMPK (adenosine 5′-monofosfaat-geactiveerde proteïnekinase) is een cellulaire energiemeter en een verlaagde AMPK-activiteit wordt onder andere in verband gebracht met insulineresistentie (6). In feite is een van de werkingsmechanismen van het welbekende antidiabeticum metformine via activatie van AMPK (7). Behandeling met metformine heeft effecten op veel aandoeningen, waaronder het verminderen van angst, wat vermoedelijk te maken heeft met het effect op AMPK (8). Interessant is dat een kwalitatief hoogwaardig gerandomiseerd gecontroleerd onderzoek (RCT) laat zien dat deze AMPK-stimulerende L. plantarum DR7-stam inderdaad stress en angst vermindert (4). Daarnaast kan deze stam ademhalingspathogenen in vitro remmen en is aangetoond dat het effectief is in het verminderen van de incidentie en ernst van infecties van de bovenste luchtwegen in een RCT (4,9). Extra bewijs en informatie over deze stam is te vinden in de beschrijving van dit ingrediënt in ons systeem.
Rheumatoïde artritis gekoppeld aan lage niveaus van microbiële butyraat
Een zeer verfijnde studie, gepubliceerd in Science Advances in februari dit jaar, heeft aangetoond dat darmbutyraat-metaboliserende soorten een rol spelen bij reumatoïde artritis (10). Hier verwijst de term “butyraat-metaboliserend” zowel naar de productie als het verbruik van butyraat, en de onderzoekers vonden dat het aantal butyraat-consumerende soorten veel hoger was bij reumatoïde artritis-patiënten die nog niet behandeld waren dan bij gezonde controles. In feite waren maar liefst 51 van de 55 reumatoïde artritis-geassocieerde butyraat-metaboliseerders butyraat-consumenten, waarvan er 46 in hogere aantallen aanwezig waren bij reumatoïde artritis-patiënten. Dit suggereert dat in reumatoïde artritis het niveau van microbiële butyraat dat beschikbaar is voor de gastheer aanzienlijk wordt verlaagd. Vervolgens valideerden de onderzoekers de bevinding van de scheve verhouding tussen butyraat-producerende/consumptie soorten in een onafhankelijke cohort. In deze tweede cohort werd ook aangetoond dat zowel de fecale als serumspiegels van butyraat verlaagd waren bij reumatoïde artritis-patiënten in vergelijking met gezonde controles. Ten slotte toonden de onderzoekers aan dat suppletie van butyraat in een dierenmodel voor artritis leidde tot een aanzienlijk lagere incidentie (11% vs. 85%) en ernst van artritis in vergelijking met de controle-groep. Samen bieden deze bevindingen sterk bewijs voor een rol van butyraat-metaboliserende soorten bij reumatoïde artritis. Dit suggereert dat interventies met butyraat-producerende soorten zoals Anaerobutyricum soehngenii of Clostridium butyricum, beide beschikbaar via ons platform, mogelijk voordelig kunnen zijn.
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
Referenties:
- https://doi.org/10.1089/jmf.2007.0144
- https://doi.org/10.3920/BM2019.0200
- https://doi.org/10.3920/BM2018.0135
- https://doi.org/10.3168/jds.2018-16103
- https://doi.org/10.3920/BM2019.0058
- https://doi.org/10.1152/ajpendo.1999.277.1.E1
- https://doi.org/10.1007/s00125-017-4342-z
- https://doi.org/10.1007/s11011-015-9677-x
- https://doi.org/10.3390/microorganisms9030528
- https://doi.org/10.1126/sciadv.abm1511
24: Internationalisatie, zomerbries, fibromyalgie
Internationalisatie
Bij de oprichting in 2018 begon het Microbiome Center haar dienst in Nederland. Sindsdien hebben steeds meer artsen uit andere landen ons gevonden en wilden ze gepersonaliseerde microbiome-behandeling in hun praktijk gebruiken. Vanaf 2021 hebben we onze service daarom uitgebreid naar andere Europese landen. Tegenwoordig is de service van het Microbiome Center beschikbaar voor artsen in zes landen, waaronder Duitsland, Zwitserland en België. Om alle nieuwe collega’s in ons netwerk te kunnen bedienen, zullen de ‘Kennisflitsen’ die we periodiek sturen vanaf nu in het Engels worden geschreven en heet het ‘Insights flash’.
Zomerbries: hebben scheten een microbiome?
De zomertijd biedt ruimte voor wat plezier, en daarom stelden we onszelf de vraag of scheten een microbiome zouden hebben. Er zit ook wat serieus in deze vraag, omdat bekend is dat microbiota-transmissie optreedt tussen mensen die dicht bij elkaar wonen, maar er is weinig bekend over de daadwerkelijke transmissieroutes (1-3). Gezien het feit dat ieder van ons gemiddeld ongeveer tien keer per dag wind laat (4), is er verrassend weinig onderzoek naar de microbiële samenstelling van scheten. In feite konden we maar één publicatie vinden, die nauwelijks een studie genoemd kan worden. Een onderzoeker testte of hij bacteriën uit de scheten van een collega kon kweken, en dat kon hij inderdaad (5). Gezien het feit dat veel bacteriën niet te kweken zijn, zou het niet verrassend zijn als scheten veel meer levende microben bevatten en mogelijk een rol spelen in microbiële transmissie.
Microbiome en fibromyalgie
Hoewel het aantal en de kwaliteit van studies nog relatief laag zijn, is het bekend dat het darmmicrobiome en het profiel van microbiële metabolieten bij fibromyalgiepatiënten (FM) veranderd is in vergelijking met gezonde individuen (6,7). Een recent gepubliceerde studie voegt nieuwe inzichten toe aan dit zelden bestudeerde onderwerp. Onderzoekers vonden veranderingen in de niveaus van secundaire galzuren en de abundantie van bacteriesoorten die bekend staan om het metaboliseren van galzuren bij FM-patiënten in vergelijking met gezonde controles (8). De secundaire galzuur genaamd alfa-muricholzuur werd vijf keer minder aangetroffen bij FM-patiënten dan bij gezonde controles en een lager niveau werd geassocieerd met een verhoogde ernst van symptomen zoals pijn, vermoeidheid, onrustige slaap en cognitieve klachten. Dit inzicht kan nieuwe wegen openen om FM-patiënten te behandelen, bijvoorbeeld met probiotische stammen die in staat zijn om alfa-muricholzuur te produceren.
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
Referenties:
1. https://doi.org/10.1038/s41564-019-0409-6
2. https://doi.org/10.1038/s41559-020-1220-8
3. https://doi.org/10.1126/science.aaz3834
4. https://doi.org/10.1007/BF02087912
5. https://doi.org/10.1136/bmj.323.7327.1449
6. https://doi.org/10.1186/s12891-020-03201-9
7. https://pubmed.ncbi.nlm.nih.gov/32116215/
8. https://doi.org/10.1097/j.pain.0000000000002694
23: Nieuwe stam, nieuw prebioticum
Nieuwe stam: L. sakei probio65
Recent hebben we een unieke stam kunnen toevoegen aan het assortiment waaruit u kunt kiezen, de Latilactobacillus sakei probio65. Deze bacterie is geïsoleerd uit kimchi en heeft een uitstekende maagdarmoverleving (1). Er is veel onderzoek gewijd aan het effect van L. sakei probio65 op atopisch eczeem. Dit omvat in vitro en preklinisch onderzoek (zie bijv. 1-3), maar ook twee goed uitgevoerde RCT’s (4,5). Laatstgenoemde laten vrij sterke effecten zien op diverse aspecten van atopisch eczeem. Verder laat in vitro onderzoek een vrij sterk remmend effect zien op diverse pathogenen (1). Interessant is daarnaast dat deze stam α-glucosidase en α-amylase activiteit kan remmen (6,7). Dit zijn enzymen die koolhydraten afbreken en remming van deze enzymen wordt gezien als een manier om diabetes te behandelen en is het werkingsmechanisme van het diabetesmedicijn acarbose (6). Een diermodel liet inderdaad een verbetering van bloedsuiker zien na toediening van L. sakei probio65 (6), wat een indicatie is dat deze stam ook bij metabool syndroom en diabetes van nut kan zijn. Overige evidence en informatie over dit building block kunt u vinden bij de beschrijving van dit ingrediënt in ons systeem.
Op 28 juni zullen we de effecten bij atopisch eczeem uitgebreider toelichten in onze webinar over allergie.
Nieuw prebioticum: PHGG
Veel vezels en prebiotica zijn onderzocht in vrij hoge doseringen. Dertig gram per dag is niet ongebruikelijk. Daarnaast laat de literatuur en praktijk zien dat de meest bekende prebiotica, FOS en GOS, regelmatig ongewenste neveneffecten geeft zoals opgeblazen gevoel of buikpijn. Een van de uitzonderingen hierop is gedeeltelijk gehydrolyseerde guar gum (PHGG). PHGG is naast de gebruikelijke hogere dagdoseringen ook onderzocht in een dosering van circa 5 gram per dag. Guar gum wordt gewonnen uit de guarboon en is van zichzelf extreem viskeus, wat de reden is dat het enzymatisch gedeeltelijk gehydrolyseerd wordt (8). Er is m.n. in de jaren ’80 en ‘90 zeer veel onderzoek gedaan naar het effect op glucoserespons en insulineresistentie (met verschillende doseringen), wat consistent een gunstig effect laat zien (zie bijv. 9 en 10). Hierdoor is PHGG dus een goede keuze als ingrediënt bij patiënten met metabool syndroom, (pre)diabetes, of andere aanwijzingen van insulineresistentie. Daarnaast is er veel onderzoek gedaan dat een gunstig effect liet zien op buikklachten zoals diarree, constipatie, buikpijn, en IBS (zie bijv. 8,11,12). Ook voor SIBO laat een goed uitgevoerd onderzoek een gunstig effect zien (13), wat PHGG tot een goede aanvulling bij SIBO-behandeling maakt. Overige evidence en informatie over dit building block kunt u vinden bij de beschrijving van dit ingrediënt in ons systeem.
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
Referenties:
- https://doi.org/10.1089/jmf.2007.0144
- https://doi.org/10.1111/jam.12229
- https://doi.org/10.5021/ad.2014.26.2.150
- https://doi.org/10.1016/j.anai.2010.01.020
- https://doi.org/10.1007/s12602-020-09654-7
- https://doi.org/10.3390/biology10040348
- https://doi.org/10.1111/jfbc.12230
- https://doi.org/10.1007/s10620-005-2713-7
- https://doi.org/10.1111/j.1464-5491.1987.tb00843.x
- https://doi.org/10.5144/0256-4947.1990.525
- https://doi.org/10.3390/nu11092170
- https://doi.org/10.4318/tjg.2010.0121
- https://doi.org/10.1111/j.1365-2036.2010.04436.x
22: SIBO behandeling en -ervaring
We hebben het in een eerdere kennisflits over SIBO (small Intestinal bacteriel overgrowth) gehad, een voor velen relatief onbekend verschijnsel wat in de praktijk heel veel voorkomt. Gastro-intestinale (en systemische) klachten door een verhoogd aantal atypische bacteriën in de dunne darm (1,2). Patiënten klagen over een opgeblazen gevoel en buikpijn, erger na het eten. Ook kunnen zij last hebben van aanhoudend boeren en flatulentie, diarree of obstipatie, verstoorde vetopname, vitaminedeficiënties (o.a. B12), een verstoorde darmbarrière en verstoorde immuunactiviteit (2).
Het advies bij chronische buikklachten om extra vezels te nemen, verergert bij SIBO de klachten omdat het de bacteriële overgroei versterkt. Ook veel klassieke probiotische stammen werken vaak averechts.
Wat kunt u bij SIBO doen?
Door het gepersonaliseerde karakter van MiBlend is het mogelijk om gericht die probiotica in te zetten waarvan studies aantonen dat zij SIBO-klachten kunnen verminderen (3). Van diverse MiBlend stammen is klinisch onderzoek bekend dat een goed effect bij SIBO laat zien. Hoe u daar als behandelaar gebruik van kunt maken is simpel: als u bij het recept de SIBO-variant kiest (in het recept keuzevakje voor 1 of 2 maanden), ontvangt de patiënt een speciale MiBlend met een thermosfles en een aangepaste gebruiksaanwijzing die de effectiviteit hoog in de dunne darm verbetert.
SIBO behandel-ervaringen
Uiteindelijk draait het om de praktijk, dus wij hebben de eerste ervaringen opgevraagd. We kwamen meteen al veel positieve patiëntverhalen tegen. Een opvallende is de mevrouw die ondanks een gezonde leefstijl toch last bleef houden van moeheid, obstipatie en huidklachten. Pas na SIBO behandeling bleek ze te verbeteren. Meer informatie kunt u vinden in de bijgevoegde casusbeschrijving.
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
Referenties:
https://doi.org/10.1016/j.gtc.2017.09.008
https://doi.org/10.1016/j.advms.09.001
https://doi.org/10.1097/MCG.0000000000000814
21: SIBO - Small Intestinal Bacterial Overgrowth
Elke behandelaar komt het tegen: Small Intestinal Bacterial Overgrowth (SIBO). Gastro-intestinale (en systemische) klachten door een verhoogd aantal atypische bacteriën in de dunne darm (1,2). Maar het wordt lang niet altijd herkend.
Patiënten met SIBO klagen vaak over een opgeblazen gevoel en buikpijn, erger na het eten. Ook kunnen zij last hebben van aanhoudend boeren en flatulentie, diarree of obstipatie, verstoorde vetopname, vitaminedeficiënties (o.a. B12), een verstoorde darmbarrière en verstoorde immuunactiviteit (2).
Bij chronische buikklachten wordt vaak geadviseerd extra vezels te nemen in de vorm van supplementen of vezelrijke voeding, maar dit verergert bij SIBO de klachten omdat het de bacteriële overgroei versterkt. De praktijkervaring leert dat veel klassieke probiotische stammen vaak averechts werken. Vanuit die optiek wordt SIBO soms behandeld met antibiotica zoals rifaximine (2,3). Hoewel dit verlichting kan geven, kan het ook zorgen voor verdere verstoring van het microbioom en kan het leiden tot C. difficile infectie en AB-resistentie. Aanbevolen wordt daarom te interveniëren op de oorzaken: verbeteren van motiliteit, lagere inname van korte koolhydraten en vasten (1,4,5).
Daarnaast kunnen ook, mits goed gekozen, probiotica worden ingezet: een meta-analyse van klinische studies laat zien dat bepaalde probiotica SIBO-klachten kunnen verminderen (6). Maar niet alle stammen zijn geschikt. Onder de ingrediënten die beschikbaar zijn voor MyOwnBlend, zijn verschillende stammen waarvoor klinisch onderzoek beschikbaar is dat effect bij SIBO laat zien. Dit betreft o.a. de Bacillus coagulans Unique IS-2 (7) en de Enterococcus faecium i.c.m. Bacillus subtilis (8). De evidence achter de verschillende stammen kunt u vinden bij de beschrijving van de ingrediënten in ons systeem.
Verschillende collega’s hebben in het afgelopen half jaar vaak een combinatie van specifieke stammen ingezet bij SIBO en daar veel positieve reacties op gekregen. Wanneer u in de Advieshulp aangeeft dat er sprake is van klachten die passen bij SIBO komen deze stammen naar voren in de voorgestelde receptuur. Sinds kort wordt de SIBO-aanpak verder ondersteund met de mogelijkheid om de probiotica semi-gefermenteerd in te nemen. De patiënt ontvangt dan bij MyOwnBlend een thermosfles met een aangepaste gebruiksaanwijzing die de effectiviteit hoog in de dunne darm verbetert. De eerste gebruikservaringen zijn positief.
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
Referenties:
- https://doi.org/10.1016/j.gtc.
2017.09.008 - https://doi.org/10.1016/j.
advms.09.001 - https://doi.org/10.1007/
s11894-019-0671-z - https://doi.org/10.1586/
17474124.2016.1110017 - https://doi.org/10.1146/
annurev-nutr-071816-064634 - https://doi.org/10.1097/MCG.
0000000000000814 - https://www.ncbi.nlm.nih.gov/
pmc/articles/PMC4311312/ - https://doi.org/10.3748/wjg.
v25.i17.2110
20: Probiotica bij angst en gespannenheid
Probiotica bij angst en gespannenheid
Recent hebben we de Lactiplantibacillus plantarum P-8 toegevoegd aan ons portfolio. Een goed uitgevoerde RCT laat zien dat deze stam effectief is tegen angst en gespannenheid (1). In hetzelfde onderzoek werd ook evidence voor een effect tegen stress gezien, zij het iets minder sterk (1). Dat dit probioticum een gunstig effect heeft op angst en gespannenheid past bij de groeiende stapel onderzoeken die laten zien dat het microbioom een rol speelt bij angst, gespannenheid, en depressie (2) en dat probiotica dit kan verbeteren (3). Er wordt vermoed dat dit effect onder andere te maken heeft met de invloed van het microbioom en probiotica op ontstekingsactiviteit (2,4). Ook bij de L. plantarum P-8 zijn anti-inflammatoire effecten gezien in onderzoek met de losse stam of in combinatie met andere stammen (1,5,6). Ook is er evidence in diermodellen dat deze stam effect heeft op oxidatieve stress (7,8), een aspect dat ook met angst, gespannenheid en depressie is geassocieerd (9,10). Tot slot is het interessant dat onderzoek met de L. plantarum P-8 laat zien dat deze stam secretoir IgA kan verhogen (11,12), omdat bekend is dat stress kan leiden tot verlaagde sIgA excretie (13). Er kan geconcludeerd worden dat het microbioom meerdere mechanismen beïnvloedt die een rol spelen bij angst en gespannenheid en dat probiotica dit kan moduleren.
Overige evidence en informatie over deze stam kunt u vinden bij de beschrijving van dit ingrediënt in ons systeem.
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
Referenties:
- https://doi.org/10.1016/j.
clnu.2018.09.010 - https://doi.org/10.1016/j.cpr.
2020.101943 - https://doi.org/10.1016/j.
neubiorev.2019.03.023 - https://doi.org/10.1002/jnr.
24476 - https://doi.org/10.1007/
s00394-020-02437-4 - https://doi.org/10.1111/1751-
7915.13661 - https://doi.org/10.1007/
s00394-020-02437-4 - https://doi.org/10.3390/
ani10040548 - https://doi.org/10.1080/
10715762.2018.1475733 - https://doi.org/10.4161/oxim.
2.2.7944 - https://doi.org/10.1016/j.nut.
2013.11.018 - https://doi.org/10.1016/j.
intimp.2015.07.024 - https://doi.org/10.3389/fnint.
2013.00086
19: Voeding & probiotica, en uitnodiging Long-Covid
Voeding en / of probiotica: wanneer het meest kansrijk?
Regelmatig krijgen wij de vraag of het aanpassen van voeding en leefstijl niet al voldoende is om het microbioom te herstellen. Inderdaad is bekend dat een aanpassing van het voedingspatroon binnen één of enkele dagen de samenstelling van het microbioom kan veranderen, net bijvoorbeeld als blootstelling aan stress (1,2). Onderzoek laat echter ook zien dat de effecten per persoon verschillen. Net zoals een gezond microbioom weerbaar is tegen perturbaties, kan ook een verstoord microbioom stabiel zijn en weinig beïnvloed worden door interventies (3). Dit wordt stabiliteit of resilience (veerkracht) genoemd (3,4,5). Het microbioom vormt een complex ecosysteem dat enigszins te vergelijken is met een bos. Regenval, een insectenplaag, of een bosbrand beïnvloeden de samenstelling van de vegetatie in een bos, maar het ecosysteem als zodanig herstelt meestal weer na zo’n pertubatie. Soms zijn de verstoringen in een ecosysteem zo groot dat het niet terugkomt in een gezonde toestand die vergelijkbaar is met de uitgangssituatie. Het microbioom heeft dan een nieuw stabiel, maar dysbiotisch evenwichtspunt bereikt dat moeilijk terug te brengen is naar een gezond evenwichtspunt (3). Als voeding en leefstijl onvoldoende effect hebben, dan is een interventie met gepersonaliseerde probiotica een aanpak die overwogen kan worden om van het ongezonde naar een gezond evenwichtspunt te komen (4,6).
PASC (Long-Covid) en het microbioom: uitnodiging
In Kennisflits #10 besteedden we al aandacht aan de relatie tussen Covid-19 en het darm-microbioom (7). Inmiddels is er meer onderzoek gepubliceerd waaruit een belangrijke rol van het microbioom en darmpermeabiliteit blijkt (8). Er wordt zelf gehypothetiseerd dat het microbioom een rol kan spelen bij de bestrijding van virussen zoals SARS-CoV-2 (9).
De laatste maanden wordt duidelijk dat relatief veel Covid-patiënten langdurige, postinfectieuze klachten hebben. Hoewel hiervoor vaak de term Long-Covid wordt gebruikt, is “post-acute sequelae of COVID-19” (PASC) een betere beschrijving (10). Postinfectieuze klachten zijn niet uniek voor Covid-19; bij de meeste bacteriële en virale infecties ontwikkelen zich chronische klachten in een subgroep van de geïnfecteerde patiënten (10). Er is een groot aantal mechanismen waarvan vermoed wordt dat ze een rol spelen bij PASC (referentie 8 geeft een uitstekende overzicht) en één daarvan is een verstoord darm-microbioom.
We vermoeden dat microbioom-interventie in bepaalde gevallen ondersteunend kan zijn aan het herstelproces. Wij zijn benieuwd naar uw ervaringen en willen graag samen met u leren of en hoe microbioom-therapie bijdraagt aan het herstel van PASC.
Heeft u PASC-patiënten in uw praktijk bij wie ook microbioom-verstoring of buikklachten in het spel zijn? Dan willen wij u uitnodigen om contact met ons op te nemen en uw ervaringen met ons te delen. Als u geen tijd heeft om e.a. op te schrijven, bellen mag ook. Wij maken een overzicht van de casussen en ervaringen van u en uw collega’s om hier nieuwe inzichten uit te extraheren en met alle collega’s te delen. Op deze manier kunnen we samen de cyclus ervaring-kennis-toepassing zo kort mogelijk maken. Ook als u suggesties heeft over hoe we dit aan kunnen pakken en met welke partijen we hierin kunnen samenwerken, horen we graag van u. Wij zijn zeer benieuwd of we samen zoiets aan de gang kunnen krijgen.
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
Referenties:
- https://doi.org/10.1038/
nature12820 - https://doi.org/10.1371/
journal.pone.0129996 - https://doi.org/10.1038/
nrmicro.2017.58 - https://doi.org/10.1136/
gutjnl-2020-321747 - https://doi.org/10.1038/
nature11550 - https://doi.org/10.3389/fmicb.
2020.572921 - https://www.microbiome-center.
nl/Medici/Kennisflits/ - https://doi.org/10.3389/fimmu.
2021.708149 - https://www.
nationalgeographic.nl/ darmflora-zou-ingezet-kunnen- worden-in-strijd-tegen- virussen - https://doi.org/10.3389/fmicb.
2021.698169
18: Nieuwe verpakking voor "onderhouds"-recepten
Nieuwe verpakkingsvorm
Regelmatig ontvangen we vragen over het vervolgtraject na een MyOwnBlend-behandeling. Ons advies tot nu toe was om een eerder voorgeschreven recept te herhalen en dat naar behoefte te laten gebruiken. De houdbaarheidsdatum van 3 maanden maakte het voor patiënten echter lastig dit voor langere tijd te gebruiken. Om dit op te lossen hebben we een nieuwe verpakkingsvorm ontwikkeld. Deze bestaat uit 12 vacuüm-gesealde pouches (zakjes) van elk 100 gram. De pouches kunnen ingevroren worden tot 1 jaar, en per stuk naar behoefte uit de vriezer gehaald worden. Vraag de patiënt hierbij om de instructies voor ontdooien in de bijsluiter te volgen om te zorgen dat de probiotische bacteriën in de pouches het ontdooien goed doorstaan (d.w.z. niet vochtig worden door te snelle opening). Na opening is een pouch nog 2 maanden houdbaar. Deze optie is voor u vanaf vandaag beschikbaar. Het is alleen mogelijk de pouches voor te schrijven na voorafgaande behandeling. Zie bijgevoegd de bijsluiter voor verdere details.
Aanvragen voor herhaalrecepten door patiënten
Uit onze servicegesprekken met patiënten hebben we geleerd dat diverse patiënten de behoefte hebben aan een makkelijke manier om hun behandelende arts te verzoeken om een herhaalrecept. Om aan deze wens tegemoet te komen hebben we op de homepage van patiënten een knop toegevoegd waarmee zij een verzoek voor een herhaalrecept kunnen plaatsen. Daarna is het aan u, als behandelend arts, om dit verzoek al dan niet te honoren. Als u zo’n verzoek ontvangt, ziet u op uw homepage een oranje notificatieknop. Als u hierop klikt kunt u het verzoek accepteren of afwijzen, waarmee u uw digitale handtekening onder het magistrale recept zet.
Ook voor u hebben we het eenvoudiger gemaakt om een eerder samengesteld recept te herhalen. In het overzicht van alle recepten (te benaderen via de knop ‘Recepten’ in het menu aan de linker kant) staat achter alle recepten die in aanmerking komen een herhaal-icoontje. Ook op de detailpagina van een recept wordt dan een herhaal-knop getoond. Als u op de herhaal-knop klikt, komt u op de bekende pagina voor het maken van een recept, waarop alle ingrediënten zijn vooringevuld. Daarbij kunt u kiezen voor alle beschikbare verpakkingsvormen, waaronder de bovengenoemde pouches. Ook kunt u indien gewenst de receptuur bijstellen.
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
17: Nieuwe stammen, mechanismen
Twee nieuwe stammen in één building block
Recent hebben we weer een nieuw building block toegevoegd dat ditmaal uit twee nieuwe stammen bestaat: een Enterococcus faecium en een Bacillus subtilisstam. Deze twee stammen zijn de actieve ingrediënten van een medicijn dat in Azië op de markt is en daar veel onderzocht is. Zo laat een meta-analyse van 53 RCTs zien dat deze combinatie van stammen effectief is bij colitis ulcerosa (1). Deze meta-analyse biedt bovendien directe evidence voor een effect bij ontsteking. Ook laten RCT’s onder andere evidence zien voor een effect op buikpijn en IBS (2,3), en small intestinal bacterial overgrowth (SIBO)(4), en geeft een retrospectief onderzoek evidence voor een effect bij antibiotica-geassocieerde diarree (5). Overige evidence en informatie over dit building block kunt u vinden bij de beschrijving van dit ingrediënt in ons systeem.
Belangrijke mechanismen achter chronische aandoeningen
In de vorige kennisflits kwam aan bod dat bijna 10 miljoen Nederlanders één of meerdere chronische aandoeningen hebben. Twee belangrijke mechanismen bij chronische aandoeningen zijn insuline resistentie en systemische laaggradige ontsteking. Deze mechanismen zijn het meest bekend bij het metabool syndroom en diabetes type 2, maar daar blijft het niet bij. Ze spelen bij (vrijwel) àlle chronische aandoeningen een rol. Ter illustratie, enkele (misschien onverwachte) voorbeelden hiervan zijn depressie (6-8), reuma (9,10), en ME/CVS (11,12). Zowel insuline resistentie als systemische laaggradige ontsteking hangen direct samen met het microbioom (13-16). Er kan dan ook geconcludeerd worden dat het zinvol is om in het therapeutisch regime bij alle chronische ziekten rekening te houden met deze twee belangrijke mechanismen en de rol van het microbioom.
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
Referenties:
- https://doi.org/10.12998/wjcc.
v6.i15.961 - https://doi.org/10.1111/nmo.
12544 - http://www.kjg.or.kr/journal/
view.html?uid=3648&vmd=Full - https://doi.org/10.3748/wjg.
v25.i17.2110 - https://doi.org/10.1097/MD.
0000000000020631 - https://doi.org/10.1016/j.
expneurol.2019.01.016 - https://doi.org/10.3389/fpsyt.
2019.00057 - https://doi.org/10.1017/
S0033291719001454 - https://doi.org/10.1002/art.
38986 - https://doi.org/10.1038/
nrrheum.2016.136 - https://doi.org/10.1073/pnas.
1607571113 - https://doi.org/10.3389/fnbeh.
2018.00078 - https://doi.org/10.1016/j.
ar2017.10.003 - https://doi.org/10.1177/
0884533615609896 - https://doi.org/10.1016/j.
cmet.2017.09.008 - https://doi.org/10.4049/
jimmunol.1601621
16: Buikklachten, gezond ouder worden
Buikklachten bij chronische aandoeningen
Het merendeel van de Nederlanders, bijna 10 miljoen mensen, heeft één of meer chronische aandoeningen (1). Er zijn ruim 3.7 miljoen Nederlanders met een MDL-aandoening bekend bij de huisarts en het grootste deel daarvan (2.5 miljoen) betreft buikklachten zoals buikpijn en constipatie (2). In veel gevallen gaan chronische ziekten gepaard met buikklachten en dit kan een indicatie zijn dat het microbioom een rol speelt. Zo komen buikklachten zoals constipatie, reflux, en diarree vaker voor bij hoofdpijn (3), hebben migrainepatiënten relatief vaak IBS (4), en heeft ongeveer de helft van alle diabetes patiënten buikklachten (5,6). Veel patiënten zijn terughoudend met praten over buikklachten of ervaren zaken als buikpijn, diarree, of constipatie door jarenlange gewenning als normaal. Het heeft zin om te vragen naar buikklachten, want dit kan snel inzicht geven of het microbioom mogelijk een rol speelt en dat kan een nieuw perspectief geven om langdurige klachten te behandelen. Vragen naar buikklachten past in elk spreekuur. Eenvoudige hulpmiddelen hiervoor (zoals de Bristol stool chart en een lijst vragen) heeft MC beschikbaar.
Gezond ouder worden met een uniek microbioom
Een recente publicatie laat zien dat een unieker microbioom correleert met betere gezondheid in ouderen (7). Verschillende cohorts werden gebruikt en deze lieten zien dat de uniekheid van het microbioom toeneemt met de leeftijd en dat de mate waarin dat gebeurt veelzeggend is. De mate van uniekheid bleek gecorreleerd aan bepaalde metabolieten die in eerdere studies geassocieerd waren aan zeer hoge leeftijd. Bovendien was de mate van uniekheid van het microbioom direct gecorreleerd aan verschillende indicatoren van gezondheid bij ouderen (medicijngebruik, eigen indruk van gezondheid, grootte van de levensruimte, loopsnelheid). Alles bij elkaar biedt dit onderzoek vrij sterke indicaties dat het microbioom een bepalende rol speelt bij gezond ouder worden.
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
Referenties:
- https://www.
volksgezondheidenzorg.info/ onderwerp/chronische- aandoeningen-en- multimorbiditeit/cijfers- context/huidige-situatie - https://www.
volksgezondheidenzorg.info/ onderwerp/maag-darm-en- leveraandoeningen/prevalentie# node-aantal-personen-met-mdl- aandoening-bekend-bij-huisarts - https://doi.org/10.1111/j.
1468-2982.2007.01486.x - https://doi.org/10.5056/jnm.
2013.19.3.301 - https://doi.org/10.1046/j.
1464-5491.1999.00135.x - https://doi.org/10.1080/
003655200750024317 - https://doi.org/10.1038/
s42255-021-00348-0 (als preprint beschikbaar via https://doi.org/10.1101/2020. 02.26.966747)
15: Nieuw ingrediënt; psoriasis
Nieuw ingrediënt
Op verzoek van verschillende collega’s hebben we 2′-fucosyllactose (2’FL) toegevoegd aan de lijst van ingrediënten waaruit u kunt kiezen. 2’FL is een zogenaamde ‘human milk oligosaccharide’ en is van nature aanwezig in moedermelk. Dergelijke moedermelkoligosaccharides dragen bij aan de ontwikkeling van het microbioom en de afstemming van het immuunsysteem. Er wordt gedacht dat deze effecten ook bij volwassenen optreden en 2′-fucosyllactose is veilig bevonden bij volwassenen (1). Interessant aspect aan deze stof is dat er preklinische aanwijzingen zijn dat Akkermansia muciniphila kan groeien op 2’FL (2-4), wat suggereert dat 2’FL één van de weinige stoffen is die deze belangrijke bacteriesoort kan stimuleren. Akkermansia muciniphila is een voor de gezondheid belangrijke bacteriesoort die mucine afbreekt en daarmee een gezonde darmwand stimuleert en is vaak sterk verlaagd bij ziekten (5,6). Het is misschien dan ook niet onverwacht dat preklinische evidence laat zien dat 2’FL de darmbarrièrefunctie verbetert (7,8). Verder is er enige evidence uit humane studies voor een effect op ontstekingsremming (9), allergieën (10), en luchtweginfecties (11). Overige evidence en informatie kunt u vinden bij de beschrijving van dit ingrediënt in ons systeem.
Rol van darm-microbioom bij psoriasis
Hoewel psoriasis bekend staat als huidziekte, zijn er diverse aanwijzingen dat het darm-microbioom een rol speelt (12,13). Dit hangt waarschijnlijk samen met het gegeven dat er bij psoriasis sprake is van een verstoord immuunsysteem en laaggradige ontsteking (14,15). Veel van de comorbiditeiten die bij psoriasis gevonden worden (zoals diabetes type 2, niet-alcoholische leververvetting, depressie, hart- en vaatziekten, en de ziekte van Crohn (14,15)) hangen dan ook samen met de kernfactoren van het metabool syndroom: systemische laaggradige ontsteking en insulineresistentie. Ook laatstgenoemde wordt bij psoriasis gevonden (16,17). Het is bekend dat het darm-microbioom een belangrijke rol speelt bij deze onderliggende mechanismen, o.a. door het effect op de darmpermeabiliteit. Dit past bij de observatie dat de darmbarrièrefunctie is bij psoriasis verminderd (18). Dit alles suggereert dat microbioomtherapie zoals probiotica van nut kan zijn bij psoriasis. Pilotstudies laten inderdaad gunstige effecten zien op ontstekingsmarkers en de ernst van de symptomen bij psoriasispatiënten (19,20).
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
Referenties:
- https://doi.org/10.1017/S0007114516003354
- https://doi.org/10.3920/BM2016.0185
- https://doi.org/10.3390/nu12051284
- https://doi.org/10.1038/s41598-020-71113-8
- https://doi.org/10.26355/eurrev_201909_19024
- https://doi.org/10.1016/j.micpath.2016.02.005
- https://doi.org/10.3389/fcimb.2018.00372
- https://doi.org/10.3390/nu12092808
- https://doi.org/10.3945/jn.116.236919
- https://doi.org/10.1007/s00394-016-1180-6
- https://doi.org/10.1097/MPG.0000000000001520
- https://doi.org/10.1016/j.berh.2020.101494
- https://doi.org/10.3390/pathogens9060463
- https://doi.org/10.1016/S0140-6736(14)61909-7
- https//doi.org/10.3390/ijms20061475
- https//doi.org/10.3390/ijerph15071486
- https//doi.org/10.1016/j.jaad.2015.01.004
- https//doi.org/10.3390/microorganisms7110550
- https//doi.org/10.4161/gmic.25487
- https//doi.org/10.2340/00015555-3305
14: Nieuwe stammen, Multiple Sclerosis
Twee nieuwe stammen
Microbiome Center zoek continu wereldwijd naar interessante andere stoffen en stammen die u kunt inzetten bij microbioomtherapie. We hebben twee nieuwe sporenvormende probiotische stammen toegevoegd aan het palet waar u uit kunt kiezen. De eerste is een Bacillus clausii die door de spoorvormende eigenschappen zeer stabiel is en een uitstekende maag-darm overleving heeft (1). Deze stam is klinisch onderzocht bij diarree (2,3). Ook zijn er voorzichtige aanwijzingen voor een mogelijk effect bij uremie (4) en voor een remmend effect op de pathogene bacterie Bacillus cereus (5).
De tweede stam is een Bacillus coagulans. Deze stam laat in een goed uitgevoerde RCT een groot effect zien op constipatie (6). Ook zijn er meerdere klinische onderzoeken waaruit een gunstig effect bij IBS naar voren komt (7-9). Voor de hieraan gerelateerde klacht buikpijn is ook evidence voor een positief effect, zij het wat minder consistent (7-12). Daarnaast zijn enige aanwijzingen uit klinische studies dat deze stam effectief is bij o.a. SIBO (13) en bacteriële vaginose (oraal gebruik) (14).
Meer informatie over deze en alle andere ingrediënten vindt u in het MC behandelnetwerk onder de (i)-knop bij de ingrediënten.
Meer aanwijzingen voor rol microbioom bij multiple sclerosis
Er waren al diverse aanwijzingen dat het darm-microbioom een rol speelt bij de etiologie van multiple sclerosis (MS), zoals stoffen van bacteriële oorsprong in het bloed en de aanwezigheid van bacteriën in de hersenen van overleden patiënten (15). Een recent verschenen onderzoek voegt hier een nieuwe aanwijzing aan toe. Bij MS-patiënten werd immunoglobuline A (IgA) aangetroffen in cerebrospinale vloeistof (16). Ook werden B-cellen met IgA expressie in de hersenen van overleden patiënten aangetroffen, met name op locaties met laesies. Opvallend was dat de B-cellen met IgA expressie in de cerebrospinale vloeistof wel op darmbacteriën reageren, maar niet op antigenen uit het brein. Dit duidt erop dat deze B-cellen uit de darm afkomstig zijn en gemigreerd zijn naar de cerebrospinale vloeistof.
Dit onderzoek suggereert dat tijdens de actieve fase van MS B-cellen die op darmbacteriën reageren migreren naar en actief zijn in cerebrospinale vloeistof en de hersenen. Het lijkt aannemelijk dat hier een belangrijke rol ligt voor een darmbarrière. Immuun-modulerende probiotische stammen kunnen hier mogelijk een rol spelen, en enkele eerste dier- en klinische onderzoeken met probiotica laten eerste voorzichtig positieve effecten zien (17).
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
Referenties:
- https://doi.org/10.3389/fmicb.
2020.01010 - https://doi.org/10.3920/
BM2018.0094 - https://doi.org/10.3920/
BM2012.0034 - https://doi.org/10.1007/
s12602-019-09540-x - https://doi.org/10.4014/mbl.
1903.03005 - https://doi.org/10.1007/
s12602-019-09542-9 - https://doi.org/10.3920/
BM2017.0129 - https://doi.org/10.1038/
s41598-019-48554-x - https://www.ncbi.nlm.nih.gov/
pmc/articles/PMC4129566/ - https://doi.org/10.5812/ircmj.
17(4)2015.23844 - https://www.ncbi.nlm.nih.gov/
pmc/articles/PMC4285933/ - https://www.researchgate.net/
publication/282188545_ Efficacy_of_Bacillus_ coagulans_strain_unique_IS-2_ in_the_treatment_of_patients_ with_acute_diarrhea - https://www.ncbi.nlm.nih.gov/
pmc/articles/PMC4311312/ - https://doi.org/10.1007/
s12088-011-0233-z - https://microbiome-center.nl/
Medici/MS,-Parkinson,- Alzheimer/ - https://doi.org/10.1126/
sciimmunol.abc7191 - https://doi.org/10.1186/
s12974-019-1611-4
13: Zorgpolissen 2021
In de maand waarop de meeste Nederlanders hun zorgpolis nog eens nakijken, leek het ons goed om informatie te geven over de vergoedingen van zorgverzekeraars voor microbioomtherapie.
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
12: Welke stammen
Welke stammen kunt u toepassen?
Soms krijgen wij de vraag welke ingrediënten in ons portfolio voor u beschikbaar zijn om te gebruiken in persoonlijke bereidingen. Daarom hierbij een kort het overzicht met een greep uit de beschikbare ingrediënten:
- Het portfolio bevat bijvoorbeeld een Clostridium butyricum stam die boterzuur kan maken, anti-inflammatoire effecten heeft, en o.a. effectief is bij colitis ulcerosa.
- Ook kunt u gebruik maken van de bekende gist Saccharomyces boulardii die effectief is tegen pathogenen en parasieten en mede daarom van nut bij diarree.
- Er is een Propionibacterium freundenreichii stam die a. vitamine K2 produceert.
- Er zijn specifieke Bifidobacterium bifidum, brevis, en Lactobacillus acidophilus stammen die zijn geselecteerd voor hun effect op verminderen van darmpermeabiliteit en anti-inflammatoire effect, en die insulineresistentie kunnen verminderen.
- Eén van de ingrediënten bevat het aminozuur L-glutamine, wat de darmbarrièrefunctie verbetert en o.a. onderzocht is voor het verminderen van bijwerkingen van chemotherapie.
- Er is de bekende LGG (Lactobacillus rhamnosus GG) die effectief is bij IBS en diarree, maar ook onderzocht bij bijvoorbeeld manie en ADHD.
Naast deze en andere ingrediënten zoeken wij continu wereldwijd naar interessante andere stoffen en stammen die u kunt inzetten bij microbioomtherapie:
- Binnenkort breiden we het portfolio bijvoorbeeld uit met een Bacillus coagulans en Bacillus clausii stam, o.a. onderzocht bij vaginose, IBS, en SIBO.
- Ook zijn we bezig om een Bacillus subtilis en Enterococcus faecium stam die gezamenlijk in een groot aantal klinische studies onderzocht zijn bij colitis ulcerosa, maar ook bij bijvoorbeeld
beademingspneumonie.
Meer informatie over de beschikbare ingrediënten en referenties naar de literatuur vindt u in het MC behandelnetwerk onder de (i)-knop bij de ingrediënten.
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
11: Diabetes
Onderzoek naar microbioom bij diabetes type 1
Het zal weinigen ontgaan zijn dat professor Max Nieuwdorp van het Amsterdam UMC ruim een miljoen euro subsidie heeft ontvangen van het Diabetes Fonds voor microbioomonderzoek bij patiënten met diabetes type 1 (T1DM) (1). Eerder onderzoek heeft al laten zien dat het microbioom van T1DM patiënten afwijkt van gezonde personen, o.a. door een verlaagd aantal boterzuurvormende bacteriën (2,3). Daarnaast zijn er wat voorzichtige aanwijzingen dat probioticagebruik geassocieerd is met een lager risico op T1DM en betere glycemische regulering bij T1DM patiënten (4,5). Ook het Amsterdam UMC deed al een verkennend onderzoek naar fecestransplantatie bij T1DM patiënten en zal hierover deze maand publiceren in het vakblad Gut (1). De toekenning van deze subsidie is een duidelijke bevestiging dat de toenemende inzichten over de sterke relatie tussen chronische ziekten en darmgezondheid waardevol zijn voor patiënten en behandelaars.
Microbioom bij insuline resistentie en diabetes type 2
Er zijn diverse sterke aanwijzingen dat het microbioom een rol speelt bij insulineresistentie en type 2 diabetes mellitus (6,7). Het is bijvoorbeeld opvallend dat metformine – het eerstelijns medicijn bij diabetes type 2 – alleen bij orale inname werkt (8). Metformine lijkt (mede) via de darm te werken en is bijvoorbeeld geassocieerd met een toename van de mucine-metaboliserende Akkermansia muciniphila en van boterzuurvormende bacteriesoorten (9-11). Diabetes type 2 en insulineresistentie gaan gepaard met systemische laaggradige ontsteking (12). Er zijn aanwijzingen dat het metabole en het immuunsysteem onderling sterk verweven zijn, vermoedelijk doordat sterke afweer evolutionair voordelig is maar veel energie kost (13). Er is bijvoorbeeld evidence dat cytokinen rechtstreeks als metabole hormonen werken (13). Gezien de effecten die probiotische stammen kunnen hebben op het immuunsysteem, maar ook op darmpermeabiliteit en boterzuurproductie, is het daarom niet onverwacht dat meta-analyses van RCT’s concluderen dat probiotica o.a. de Hb1Ac en HOMA-IR kunnen verlagen (14,15).
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
Referenties
- https://www.diabetesfonds.nl/
over-diabetes/nieuws/miljoen- euro-voor-onderzoek- poeptransplantatie-bij- diabetes-type-1 - https://doi.org/10.1155/2020/
3936247 - https://doi.org/10.3389/fendo.
2020.00125 - https://doi.org/10.1001/
jamapediatrics.2015.2757 - https://doi.org/4172/2329-
8901.1000188 - https://doi.org/10.1210/er.
2017-00192 - https://doi.org/10.1172/
JCI129194 - https://doi.org/10.1111/j.
1464-5491.1992.tb01716.x - https://doi.org/10.1007/
s00125-015-3844-9 - https://doi.org/10.1038/
nature15766 - https://doi.org/10.2337/dc16-
1324 - http://www.njmonline.nl/njm/
getarticle.php?v=71&i=4&p=174 - https://doi.org/10.1038/
nature21363 - https://doi.org/10.20452/pamw.
3156 - https://doi.org/10.1186/
s12967-020-02213-2
10: Covid-19, Alzheimer
Interactie tussen bacteriën en SARS-CoV-2
Uit diverse onderzoeken en ook uit RIVM gegevens is bekend dat obesitas, diabetes en hart- en vaatziekten het risico op een ernstig verloop van Covid-19 verhogen (1,2). Enkele weken geleden verscheen een intrigerende review (3) waarin synergistisch effect wordt gezien tussen het nieuwe coronavirus en lipopolysaccharide (LPS, een endotoxine van bacteriële oorsprong). Beiden verlagen de expressie van de ACE2 receptor in de longen waardoor het angiotensine-systeem ontregeld wordt. Uit onderzoek met een varkenscoronavirus is bekend dat de combinatie van dat virus en LPS in varkens leidt tot ernstig acuut ademhalingssyndroom (SARS), terwijl blootstelling aan elk afzonderlijk veel mildere symptomen geeft. Ook wordt bij o.a. diabetes verhoogde darmpermeabiliteit gezien (4), wat leidt tot verhoogde LPS in de circulatie en daarmee geassocieerde insulineresistentie (5). Dit review (3) is daarmee een nieuwe aanwijzing dat verbeteren van de darmbarrièrefunctie een zinvol therapeutisch doel lijkt om patiënten met cardiometabole ziekten te beschermen.
Mycobioom bij Alzheimer
Eerdere onderzoeken hebben al laten zien dat er verschillen in microbioom-samenstelling zijn tussen Alzheimerpatiënten en gezonde personen (6,7). Deze onderzoeken keken uitsluitend naar bacteriën, maar het menselijk microbioom bestaat ook uit tal van andere typen micro-organismen zoals schimmels, archea, protisten, en virussen. Een nieuwe publicatie concludeert dat er bij mensen met milde cognitieve achteruitgang ook verschillen zijn in de samenstelling van schimmels (het mycobioom) (8). Ook vergeleken de onderzoekers de invloed van twee voedingspatronen met elkaar. Alleen een aangepast Mediterraan-ketogeen dieet blijkt het mycobioom te beïnvloeden bij patiënten met milde cognitieve achteruitgang. Dit sluit aan bij eerder onderzoek waarin dit dieet leidde tot verbetering van markers van de ziekte van Alzheimer. Een ander recent onderzoek met een diermodel van Alzheimer laat overtuigend zien dat fecestransplantatie van gezonde muizen naar zieke muizen leidt tot minder afzetting van amyloïde-β plaques, verlaagde ontstekingsmarkers, en vermindering van cognitieve achteruitgang (9). Deze twee onderzoeken breiden de groeiende stapel uit van evidence dat het ziekteproces achter de ziekte van Alzheimer via de darm is te beïnvloeden.
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
Referenties
- https://doi.org/10.1016/j.dsx.
2020.04.044 - https://www.rivm.nl/
documenten/wekelijkse-update- epidemiologische-situatie- covid-19-in-nederland - https://doi.org/10.7554/eLife.
61330 - https://doi.org/10.1186/1475-
2891-13-60 - https://doi.org/10.2337/db06-
1491 - https://doi.org/10.1038/
s41598-017-13601-y - https://doi.org/10.1038/
s41598-018-38218-7 - https://doi.org/10.1016/j.
ebiom.2020.102950 - https://doi.org/10.1136/
gutjnl-2018-317431
9: Migraine, LGG, naamswijziging Lactobacillus
Probiotica bij migraine
Er zijn diverse aanwijzingen voor een relatie tussen het darm-microbioom en migraine (1). Een recente systematische review van placebo-gecontroleerde onderzoeken vond twee studies die voldeden aan de inclusiecriteria, waarvan één een vrij groot effect en de ander geen effect vond van probiotica (2). Ook uit ervaringen is bekend dat migrainepatiënten soms heel veel baat hebben bij probiotica. Sommige patiënten die al van alles geprobeerd hebben, rapporten dat hun migraine-aanvallen vrijwel verdwenen zijn nadat ze probiotica zijn gaan gebruiken. Een aardig voorbeeld van een studie die dit type observaties beschrijft bij ruim 1000 patiënten is deze, waarbij de ernst van de klachten flink verminderde (3).
Nieuwe stam: LGG
Aan het portfolio van probiotica dat u kunt voorschrijven is een nieuwe stam toegevoegd: de Lacticaseibacillus rhamnosus GG, ’s werelds meest onderzochte probiotische bacteriestam. Als u zich afvraagt of er een spelfout in de geslachtsnaam zit, lees dan even het laatste berichtje in deze kennisflits. Het feit dat deze stam, ook wel bekend als LGG, zo veel onderzocht is (ruim 1100 publicaties in Pubmed), betekent zeker niet dat hij overal effectief voor is. Een veel onderzochte indicatie is bijvoorbeeld eczeem, maar een meta-analyse van RCTs laat zien dat de LGG daarbij niet effectief is (4). We hebben de LGG uiteraard toegevoegd omdat er diverse indicaties zijn waarbij hij wél effectief is. De LGG haalt in ons GRADE-gebaseerde beoordelingssysteem zelfs de hoogst haalbare score voor acute diarree vanwege twee meta-analyses van RCTs met zeer consistente resultaten (5,6). Ook bij IBS is er sterke evidence dat de LGG effectief is (7,8). Interessant is dat de LGG ook onderzocht is bij ADHD en manie, hoewel dit slechts eerste voorzichtige aanwijzingen betreffen (9,10). Daarnaast zijn er nog diverse andere indicaties, die u kunt terugvinden in de informatie op onze website.
Naamswijziging van het bacteriegeslacht Lactobacillus
Een team van internationale experts heeft enkele maanden gelden een naamswijziging doorgevoerd van het bacteriegeslacht Lactobacillus (11). Dit geslacht bevatte diverse bekende bacteriesoorten, zoals de L. acidophilus, L. rhamnosus, en L. brevis. Er waren al langere tijd aanwijzingen uit o.a. genetische analyses dat de taxonomische heterogeniteit binnen het oude Lactobacillus geslacht te groot was om redelijkerwijze alle 261 bacteriesoorten te kunnen groeperen. In de nieuwe indeling zijn er 23 nieuwe geslachten geïntroduceerd, die wel allemaal met de letter L beginnen, zodat afkortingen niet veranderen. Er zijn diverse websites met een overzicht waarin de oude en nieuwe namen opgezocht kunnen worden (12).
Meer inzichten lezen?
Volg ons op LinkedIn: https://www.linkedin.com/company/microbiome-center/
Of lees eerdere kennisflitsen op: https://microbiome-center.nl/medici/kennisflits/
Referenties
- https://doi.org/10.1186/
s10194-020-1078-9 - https://doi.org/10.3390/
jcm8091441 - https://doi.org/10.1007/
s15006-018-1052-5 - https://doi.org/10.3390/
nu10091319 - https://doi.org/10.3748/wjg.
v25.i33.4999 - https://doi.org/10.1111/apt.
15267 - https://doi.org/10.1111/j.
1365-2036.2011.04665.x - https://doi.org/10.1097/MCG.
0000000000001054 - https://doi.org/10.1038/pr.
2015.51 - https://doi.org/10.1111/bdi.
12652 - https://doi.org/10.1099/ijsem.
0.004107 - https://www.microbiometimes.
com/the-lactobacillus- taxonomy-change-has-arrived- what-do-you-need-to-know/
8: Microbioom en virusinfecties
Microbioom diverse rollen bij virusinfecties
Virusinfecties worden op verschillende manieren beïnvloed door het microbioom, variërend van een stimulerend tot een remmend effect (1). Virussen kunnen op directe wijze gebruik maken van bepaalde bacteriële factoren om een verhoogde stabiliteit, infectiegraad, en virulentie te krijgen en kunnen indirect geholpen worden doordat bepaalde bacteriën expressie van regulerende T cellen stimuleren en daarmee de afweer onderdrukken. Anderzijds kan het microbioom virusinfecties ook tegengaan. Dit kan op een directe manier door binding, absorptie, destabilisatie, en verminderde replicatie van virussen, en indirect door het versterken van de afweerreactie van het immuunsysteem. Deze tegengestelde effecten van het microbioom benadrukken de complexiteit van de interactie tussen gastheer en microbioom en het belang van een goede balans. Een sterke immuunrespons is immers gewenst bij virusinfecties, maar nadat de infectie overwonnen is, is juist demping van de immuunrespons gewenst. Ook bij niet-overdraagbare ziekten is stimulering van ontstekingsremmende regulerende T cellen juist zeer wenselijk (2,3).
Herstel na virusinfecties
Het microbioom beïnvloedt niet alleen virusinfecties, virusinfecties beïnvloeden op meerdere manieren ook het microbioom (1,4). Bij diverse virussen, waaronder het griep- en norovirus, zijn veranderingen van het darm-microbioom gevonden. Dit is o.a. gelinkt aan de immuunmodulatie door het virus, maar ook aan veranderingen in voedselinname gedurende de ziekteperiode (5). Verstoringen in het darm-microbioom na een virusinfectie zijn dus niet onverwacht, maar soms zijn deze van ernstigere en/of chronische aard. Bij infectieuze gastro-enteritis, ook met virale oorzaak, kan bijvoorbeeld het zogenaamde postinfectieus prikkelbare darm syndroom (PI-IBS) ontstaan (6,7). Hierbij spelen onder andere een verstoorde immuunactiviteit (waaronder een hoog niveau van pro-inflammatoire cytokines), een verlaagde darmpermeabiliteit, en verstoord darm-microbioom een rol. Bij virussen die vooral buiten de darm actief zijn, komen eveneens postvirale klachten zoals vermoeidheid voor en speelt een verhoogd niveau van pro-inflammatoire cytokines een rol (8). Omgekeerd lijkt het chronisch vermoeidheidssyndroom (ME/CVS) vaak een virale oorsprong te kennen en ook hier is sprake van een verschoven immuun activiteit en verstoord darm-microbioom (9,10). Virusinfecties kunnen dus langdurige consequenties hebben en de immuunmodulerende rol van bacteriën in de darm lijkt hierbij van belang. Anders dan tijdens acute virusinfecties, maar vergelijkbaar met niet-overdraagbare ziekten, lijkt de wenselijke aanpassing eenduidig: remmen van de inflammatoire activiteit van het immuunsysteem.
Referenties
- https://doi.org/10.3389/fimmu.
2019.01551 - https://doir.org/10.1136/bmj.
j5145 - https://doi.org/10.1016/j.
jaci.2014.11.012 - https://doi.org/10.1016/j.
micinf.2017.09.002 - https://doi.org/10.1128/mBio.
03236-19 - https://doi.org/10.1007/
s11894-017-0595-4 - https://doi.org/10.1097/MCG.
0000000000000924 - https://doi.org/10.1371/
journal.pone.0155884 - https://doi.org/10.1016/j.
neucli.2017.02.002 - https://doi.org/10.1007/
s11011-019-0388-6
7: Immuunsysteem
Immuunsysteem.
Het microbioom in de darm speelt een belangrijke rol in de educatie en functie van het immuunsysteem en de verworven immuniteit (1,2,3). Zowel antibiotica als probiotica beïnvloeden de effectiviteit van vaccinaties (4,5) en het microbioom en bepaalde probiotica hebben invloed op het verloop van virusinfecties (6,7). Opvallend is dat bij Covid-19 patiënten bijna één op de vijf patiënten last had van diarree, overgeven, of buikpijn (8) en dat het SARS-CoV-2 virus is aangetroffen in ontlasting en in het Nederlands rioolwater (9,10,11). Daarnaast wordt verlies van reukzin genoemd als symptoom van Covid-19 (12). Intrigerend is dat dit in verband wordt gebracht met het doordringen van het virus tot het centrale zenuwstelsel, waar het via het ademhalingscentrum mogelijk ook een rol speelt bij ademhalingsproblemen (13,14). De darm-bloed barrière en bloed-brein barrière worden beïnvloed door dezelfde factoren, en het microbioom speelt hierin een rol (15,16). Hoewel het microbioom op het eerste gezicht niets te maken lijkt te hebben met Covid-19, kan het dus wel degelijk een rol spelen en met name immunogeen werkende bacteriën en darmbarrièrefunctie verdienen daarbij aandacht.
Referenties
- https://doi.org/10.1126/
science.1223490 - https://doi.org/10.1038/nm.
2505 - https://doi.org/10.1038/ni.
3780 - https://doi.org/10.1016/j.
cell.2019.08.010 - https://doi.org/10.3390/
nu9111175 - https://doi.org/10.3389/fcimb.
2016.00041 - https://doi.org/10.3389/fimmu.
2016.00633 - https://journals.lww.com/ajg/
Documents/COVID_Digestive_ Symptoms_AJG_Preproof.pdf - https://doi.org/10.1016/j.
ijid.2020.02.050 - https://doi.org/10.1001/jama.
2020.3786 - https://www.rivm.nl/nieuws/
nieuwe-coronavirus- aangetroffen-in-rioolwater - https://www.entuk.org/loss-
sense-smell-marker-covid-19- infection - https://doi.org/10.1021/
acschemneuro.0c00122 - https://doi.org/10.1002/jmv.
25728 - https://doi.org/10.1016/j.
bbrc.2018.11.021 - https://doi.org/10.1152/ajpgi.
00048.2015
6: Zenuwstelsel en psyche
Microbioom kan zenuwstelsel rechtstreeks (!) beïnvloeden
Dat er een relatie is tussen de darmen en het brein is niet nieuw (1). Sinds 2014 verschenen er al bijna 2000 publicaties. In februari 2020 publiceerde Nature onderzoek waarin een directe link tussen het microbioom en het zenuwstelsel in de darm werd aangetoond (2,3). De onderzoekers hebben een receptor geïdentificeerd die intrinsiek onderdeel van het zenuwstelsel in de darm is en toonden aan dat micro-organismen in de darm deze receptor rechtstreeks tot expressie kunnen brengen (3). Dit heeft invloed op functies van het lokale neurale netwerk, zoals peristaltiek, maar via de verbinding van de nervus vagus biedt deze receptor ook een directe link tussen het microbioom en het brein.
Rol microbioom in autisme
Er zijn sterke vermoedens dat autisme spectrum stoornis gerelateerd is aan de darmgezondheid. Autistische kinderen hebben vaak darmklachten zoals chronische diarree of constipatie (4,5) en behoren tot de groep kinderen die het vaakst worden doorverwezen naar een MDL-arts (5). Er zijn bij autistische mensen aanwijzingen voor een vergrote doorlaatbaarheid van de darmwand (6) en er worden verhoogde waarden van een endotoxine van bacteriële oorsprong (LPS) in het bloed aangetroffen (7). Een klein onderzoek met poeptransplantatie bij autistische kinderen resulteerde niet alleen in sterk verminderde darmklachten sterk, maar ook in flink verbeterde gedragsscores (8). Dit effect was twee jaar later nog steeds aanwezig (9). Ook recente pilot studies met pre- en probiotica laten voorzichtige verbeteringen in gedragsscores zien (10,11).
Referenties
- https://doi.org/10.1152/
physrev.00018.2018 - https://www.nrc.nl/nieuws/
2020/02/12/bacterien- communiceren-met-zenuwstelsel- in-de-darm-a3990193 - https://doi.org/10.1038/
s41586-020-1975-8 - https://doi.org/10.1007/
s10803-013-1973-x - https://doi.org/10.3748/wjg.
v22.i46.10093 - https://doi.org/10.3390/
ijms20092115 - https://doi.org/10.3748/wjg.
v22.i1.361 - https://doi.org/10.1186/
s40168-016-0225-7 - https://doi.org/10.1038/
s41598-019-42183-0 - https://doi.org/10.1186/
s40168-018-0523-3 - https://doi.org/10.3390/
nu11040820
5: Allergieën
Rol van probiotica bij allergieën
Er is via het immuunsysteem een direct verband tussen allergieën en het microbioom. Allergische reacties zijn IgE gemedieerd en van immunologische aard [1] en het is bekend dat het microbioom betrokken is bij de educatie van en de grondtoon van het immuunsysteem [2,3]. De relatie met het microbioom wordt bevestigd door verschillende typen onderzoeken bij astma, constitutioneel eczeem, voedingsallergieën, en hooikoorts [4,5]. Interventies met pre- en probiotica bij zwangere vrouwen en hun kinderen blijken preventieve en curatieve effecten te hebben bij constitutioneel eczeem [6,7] en voedingsallergieën [8,9]. De effecten zijn stam-specifiek en dit valt te vertalen naar de persoonlijke bereidingen in MyOwnBlend.
Verkiezing van de ‘Leefstijlprofessional 2020’
Tijdens het congres van Vereniging Arts en Leefstijl (3 april) wordt de verkiezing van de ‘Leefstijlprofessional 2020’ gehouden. Dit jaar kunnen daar naast artsen ook POH’s, apothekers, leefstijlcoaches en diëtisten voor genomineerd worden. Als u iemand in gedachten heeft, kunt u zich bij de vereniging melden [10].
Referenties
- Akdis, C.A., Agache, I., 2014. Global atlas of allergy. European Academy of Allergy and Clinical Immunology
- https://doi.org/10.1016/j.
immuni.2017.04.008 - https://doi.org/10.1111/imm.
12896 - https://doi.org/10.1016/j.
jaci.2017.02.007 - https://doi.org/10.1111/imr.
12556 - https://doi.org/10.1016/j.
jaci.2015.04.031 - https://doi.org/10.1001/
jamapediatrics.2015.3943 - https://doi.org/10.1097/MD.
0000000000002562 - https://doi.org/10.1016/j.
aller.2019.04.009 - https://www.artsenleefstijl.
nl/activiteiten/ jaarcongres2020/
4: Depressie
Advies-hulp en productinformatie update
Na enkele technische uitdagingen, zijn nu alle beschrijvingen en referenties van de supplementen en magistrale ingrediënten compleet ingevuld. Deze vindt u door op de (i) naast een product of ingrediënt te klikken in de Advies-hulp of op de Recepten-aanmaak-pagina. De beschrijving biedt een samenvatting van alle onderzoeken die gedaan zijn met het betreffende product of ingrediënt, inclusief de bijbehorende referenties.
Ook is de Advies-hulp verder verbeterd. Bij de voorgestelde hoeveelheden van de magistrale ingrediënten wordt nu ook rekening gehouden met de minimale en maximale dagdosis voor elk ingrediënt. Onveranderd is dat de uitkomst van de Advieshulp is gebaseerd op de ingevulde scores voor de verschillende indicaties (klachten, medische achtergrond, en lab uitslagen) enerzijds en op de sterkte van de evidence van de producten/ingrediënten bij deze indicaties anderzijds. In de nieuwe versie van de Advies-hulp is ook een verfijndere gradatie aangebracht voor de sterkte van de evidence, wat op een systematische (op GRADE geïnspireerde manier [1]) gewogen is. Momenteel werken we er hard aan om bij de volgende versie van de Advies-hulp de evidence scores voor u zichtbaar te maken, zodat u nog beter kunt zien waarop het advies gebaseerd is.
Probiotica mogelijk nuttig bij depressie
Sinds enkele jaren begint duidelijk te worden dat het microbioom een rol speelt bij stemmingen en depressie; er wordt gesproken over de darm-brein-as. Er zijn relaties met de kwaliteit van leven cq. depressie en de samenstelling, structuur, en functie van het microbioom [2,3]. Feces-transplantatie van patiënten met major depression disorder (MDD) naar muizen of ratten resulteert in gedrag dat geassocieerd is met depressie [4,5]. Klinische studies hebben laten zien dat interventies met probiotica kunnen zorgen voor vermindering van depressie [6-8].
Koninklijke interesse voor het microbioom
Op dinsdag 26 november vond het Paleissymposium ‘The Microbiome’ plaats, waar Koning Willem-Alexander en Prinses Beatrix bij aanwezig waren [9]. Sprekers waren Martin Blaser, directeur van het Human Microbiome Program, en professor Max Nieuwdorp, internist-endocrinoloog en pionier in fecestransplantatie onderzoek. Beide lezing zijn na te luisteren [9]. Ook op het hoogste niveau wordt inmiddels aandacht geschonken aan het belang van het microbioom voor de gezondheid.
Referenties
- https://en.wikipedia.org/wiki/
The_Grading_of_ Recommendations_Assessment,_ Development_and_Evaluation_( GRADE)_approach - https://doi.org/10.1002/bies.
201800027 - https://doi.org/10.1038/
s41564-018-0337-x - https://doi.org/10.1038/mp.
2016.44 - https://doi.org/10.1016/j.
jpsychires.2016.07.019 - https://doi.org/10.1016/j.nut.
2015.09.003 - https://doi.org/10.29219/fnr.
v62.1218 - https://doi.org/10.1016/j.
clnu.2018.04.010 - https://www.paleisamsterdam.
nl/paleissymposium/ paleissymposium-the- microbiome/
3: Voeding, darmen en osteoporose
De reactie op voeding is sterk individueel
De macronutriënten-samenstelling van voeding blijkt slechts 16-32% van de glucoserespons op voeding te verklaren, individuele factoren zoals de samenstelling, functie en structuur van het microbioom zijn veel bepalender. Dit blijkt uit de PREDICT-1 studie die ruim 1000 tweelingen en niet-tweelingen intensief volgde (https://doi.org/10.1093/cdn/
Prikkelbaredarmsyndroom (PDS) verbetert met probiotica en glutamine
Probiotica verlichten pijn en algemene symptoomscore bij PDS (IBS), concludeert een meta-analyse van RCT’s. Wel hangt de effectiviteit af van de samenstelling (https://doi.org/10.3748/wjg.
Probiotica mogelijk nuttig bij osteoporose
Het microbioom speelt een belangrijke rol in de darm-bot as. Dierstudies bieden eerste aanwijzingen dat probiotica een beschermend effect hebben tegen osteoporose (https://www.ncbi.nlm.nih.gov/
2: Saccharomyces boulardii
De mogelijkheden van de magistrale bereiding MyOwnBlend van Microbiome Center zijn uitgebreid. Vanaf vandaag is het mogelijk om gebruik te maken van een krachtige nieuwe stam als MyOwnBlend ingrediënt: Saccharomides boulardii.
De S. boulardii heeft een sterk evidence dossier en vormt een forse uitbreiding van de wapens tegen diverse typen diarree, zoals antibiotica-geassocieerde diarree, reizigersdiarree, of acute en infectieuze diarree. Ook helpt de S. Boulardii mee bij het bestrijden van parasieten, pathogene bacteriën en pathogene gisten, en bij het verminderen van inflammatie.
In de anamnese- en advieshulp zal dit ingrediënt vanaf nu meegenomen worden en is voor iedere indicatie de evidence te vinden.
Selectie uit de literatuur:
http://doi.org/10.1111/apt.
http://doi.org/10.3390/
http://doi.org/10.1016/j.
http://doi.org/10.1542/peds.
1: Luchtwegen, urinewegen, depressiviteit
Met de koude, donkere en natte maanden op komst hebben we deze drie noties uit het vakgebied geselecteerd.
Luchtweginfectie
Probiotica kan de incidentie en de duur van luchtweginfecties bij kinderen verminderen, dat blijkt uit deze systematische review van 23 trails met 6269 kinderen (PMID: 27495104: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4979858/ ).
Urineweginfectie
Lactobacillus bevattende producten kunnen terugkerende urineweginfecties bij vrouwen mogelijk voorkomen. Het wijdverbreide gebruik van antibiotica heeft wereldwijd geleid tot een toename van E. coli-resistente isolaten bij urineweginfecties. Een veelbelovende niet-antibioticabenadering is het gebruik van probiotische lactobacillen (PMID: 29602464; https://www.ncbi.nlm.nih.gov/pubmed/29602464 ).
DepressieProbiotica blijken de gevoeligheid voor depressie te reduceren. Een verminderde darmbarrièrefunctie en ontsteking zijn gecorreleerd met depressieve symptomen. Dit wordt besproken in diverse publicaties, zoals een klinische studie naar het effect van consumptie van probiotische supplementen op depressieve symptomen in een steekproef van deelnemers met milde tot ernstige depressie (PMID: 31078831; https://www.ncbi.nlm.nih.gov/
pubmed/31078831 ).